Clear Sky Science · ar
الكركمين يثبط عملية التحلل السكري عبر EP300 في سرطان الخلايا الحرشفية الفموي
قوة التوابل ضد سرطان الفم
الكركم، التوابل الصفراء الزاهية الشائعة في الكاري، يحتوي على مركب يُدعى الكركمين وقد أثار اهتمام الأطباء والعلماء منذ زمن طويل. تستكشف هذه الدراسة كيف قد يبطئ الكركمين نمو سرطان الخلايا الحرشفية الفموي، وهو شكل شائع وغالبًا ما يكون مدمرًا من سرطانات الفم، عن طريق قطع مصدر الوقود المفضل لخلايا السرطان بهدوء: السكر. قد يساعد فهم هذه المعركة الطاقية الخفية في تحويل مكوّن مألوف من المطبخ إلى مساعد مفيد إلى جانب العلاجات السرطانية القياسية.
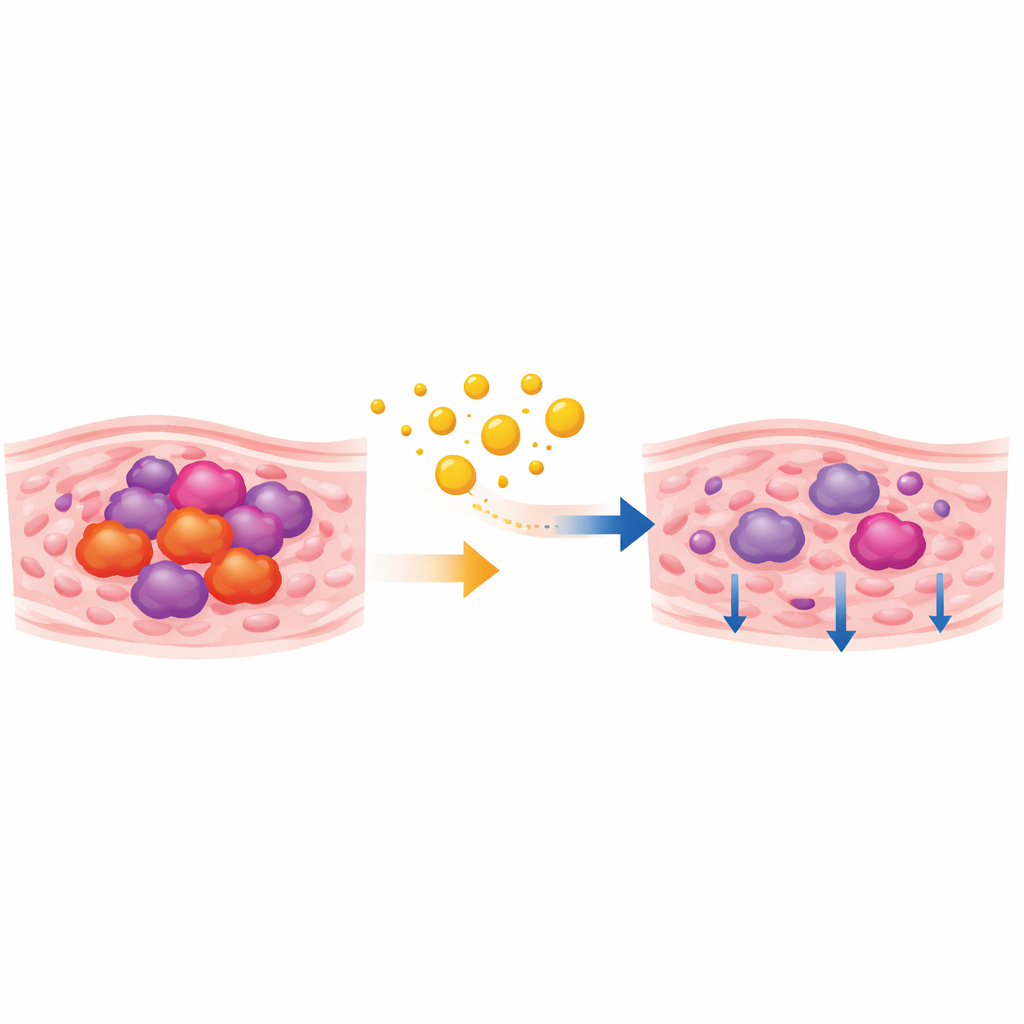
شهية السرطان للحلوى
خلايا السرطان لا تستخدم الطاقة كما تفعل الخلايا السليمة. حتى عندما يتوفر الكثير من الأكسجين، تعتمد العديد من الأورام إلى حد كبير على مسار سريع لكنه هدَّار لتفكيك السكر، غالبًا ما يُسمى تأثير واربرغ. في هذا الوضع، تمتص خلايا السرطان كميات كبيرة من الجلوكوز وتحوّله بسرعة إلى لاكتات. تمنحهم هذه الاستراتيجية مواد خام للنمو وغزو الأنسجة المجاورة وتشكيل بيئة داعمة حول الورم. يعتمد سرطان الخلايا الحرشفية الفموي، الذي يشكل نحو 90% من سرطانات الفم، بشكل كبير على هذا الأيض الجشع للسكر، مما يجعل استخدام الطاقة هدفًا جذابًا للعلاجات الجديدة.
ما يفعله الكركمين لخلايا السرطان
زرع الباحثون سطرين خلويين بشريين من سرطان الفم وخلايا فموية طبيعية في المختبر، ثم عالجوها بجرعات مختلفة من الكركمين. قاسوا مدى نمو الخلايا وتشكيلها للمستعمرات وحركتها لسد "جَرْح" اصطناعي في طبق. في كلا سطرَي الخلايا السرطانية، خفّض الكركمين بشدة النمو وتكوّن المستعمرات والهجرة بطريقة تعتمد على الجرعة، بينما كانت الجرعات المنخفضة إلى المتوسطة قليلة التأثير على الخلايا الفموية الطبيعية. عندما فحص الفريق كمية الجلوكوز التي استهلكتها الخلايا وكمية اللاكتات التي أفرجت عنها، وجدوا أن الكركمين خفّض باستمرار كلا المقياسين في الخلايا السرطانية لكنه ترك الخلايا الطبيعية إلى حد بعيد دون تغيير. يشير هذا النمط إلى أن الكركمين يبطئ بشكل انتقائي محرك حرق السكر الذي تعتمد عليه خلايا السرطان.
مفتاح جزيئي في صلب القصة
لفهم كيف يخفّض الكركمين هذا الاستخدام الطاقي، ركز العلماء على بروتين يُدعى EP300. يساعد EP300 على التحكم في تشغيل أو إيقاف جينات معينة عبر إضافة وسوم كيميائية صغيرة إلى بروتينات أخرى، بما في ذلك تلك التي تدير عمليات الأيض الخلوية. أظهرت أعمال سابقة أن EP300 نشط بشكل غير معتاد في سرطانات الفم ويرتبط بزيادة استخدام الجلوكوز وسلوك أكثر عدوانية. في هذه الدراسة، خفّض علاج الكركمين مستويات EP300 في الخلايا السرطانية. عندما زاد الفريق EP300 اصطناعيًا، استهلكت الخلايا السرطانية مزيدًا من الجلوكوز وأنتجت مزيدًا من اللاكتات—والمهم أن هذا الارتفاع في EP300 ألغى جزئيًا قدرة الكركمين على إبطاء التحلل السكري. تشير هذه التجارب إلى أن EP300 يعمل كمفتاح جزيئي رئيسي يربط بين الكركمين وضبط طاقة خلايا السرطان.
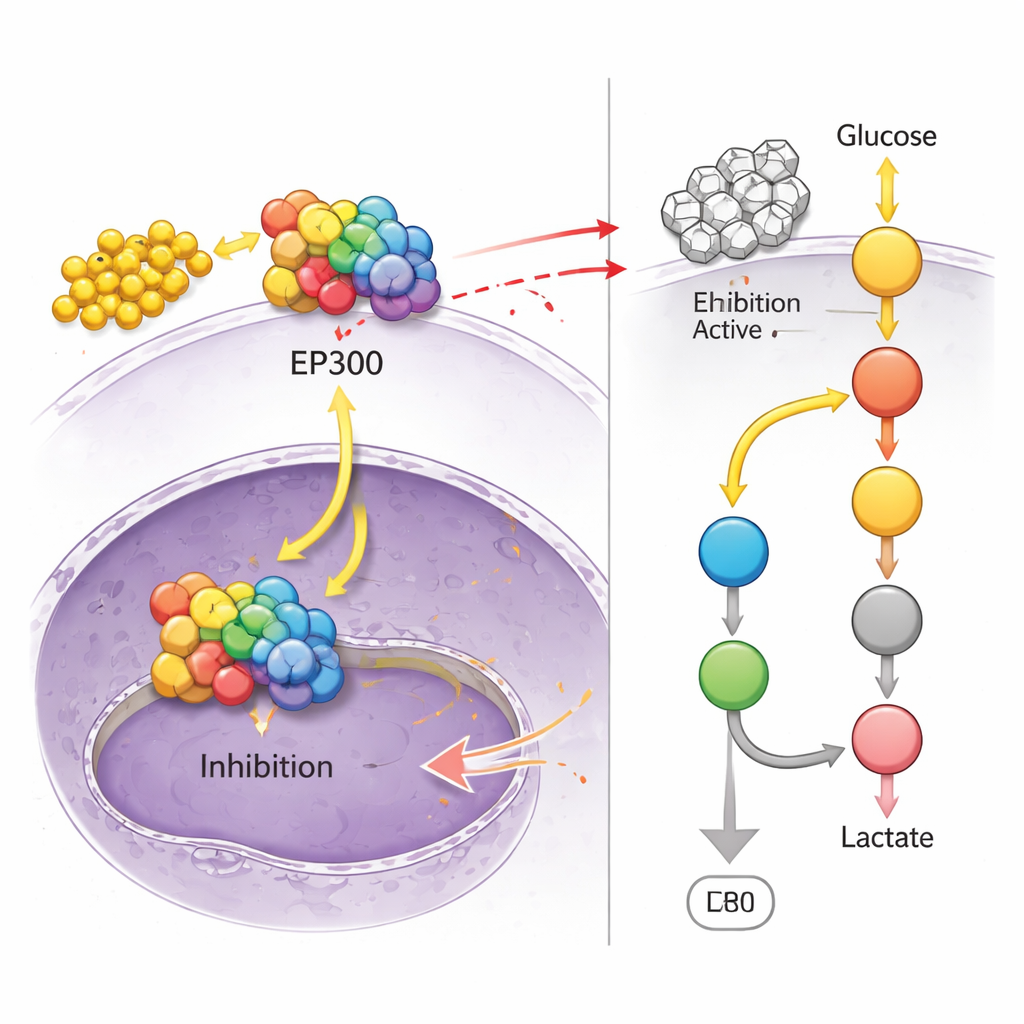
إغلاق خط أنابيب السكر
فحص الباحثون بعد ذلك عدة بروتينات رئيسية تنقل وتعالج الجلوكوز داخل الخلايا: GLUT1 الذي يدخل السكر إلى الخلية، وPKM2 وLDHA اللذان يساعدان على تحويله إلى لاكتات. باستخدام اختبارات تعبير الجينات وقياسات البروتين، وجدوا أن EP300 يرفع مستويات هؤلاء الثلاثة من مساعدي التحلل السكري. خفّض الكركمين مستوياتهم، لكن عندما تم إجبار EP300 على الارتفاع مجددًا، تم عكس هذا الانخفاض جزئيًا. دعمت تحليلات الشبكات للوصلات البروتينية الفكرة القائلة بأن EP300 يقع بالقرب من مركز شبكة من الإنزيمات المعالجة للسكر. مجتمعة، تشير البيانات إلى أن الكركمين يتداخل مع EP300، وEP300 بدوره يتحكم في فريق صغير من الإنزيمات التي تبقي خط أنابيب التحلل السكري جاريًا في خلايا السرطان.
ما الذي قد يعنيه هذا للمرضى
بعبارات بسيطة، تظهر هذه الدراسة أن الكركمين يمكن أن يضعف خلايا سرطان الفم عبر خفض بروتين التحكم الرئيسي EP300، الذي يعزز عادة قدرتها على حرق السكر بسرعة. مع تراجع EP300، تفقد خلايا السرطان بعض ميزتها الطاقية: تنمو أبطأ، تنتشر أقل، وتنتج كمية أقل من حمض اللاكتيك الذي يساعدها على البقاء. رغم أن هذه النتائج مستمدة من زرعات خلوية في المختبر وأن هناك حاجة لمزيد من العمل في الحيوانات والبشر، فإنها تقدم خارطة طريق واضحة: قد يوفر الجمع بين الكركمين أو مركبات ذات صلة وعلاجات أخرى تستهدف أيض الورم يومًا ما خيارات ألطف وأكثر دقة للأشخاص المصابين بسرطان الفم.
الاستشهاد: Tan, W., Zhang, C., Han, L. et al. Curcumin inhibits glycolysis via EP300 in oral squamous cell carcinoma. Sci Rep 16, 11702 (2026). https://doi.org/10.1038/s41598-026-44496-3
الكلمات المفتاحية: سرطان الفم, الكركمين, تمثيل سرطاني, EP300, تثبيط التحلل السكري