Clear Sky Science · ar
الأليزارين يحفز آلية متعددة الاتجاهات لمضاد السرطان في خلايا سرطان عنق الرحم وسرطان البروستاتا
لماذا صبغة نباتية مهمة في مكافحة السرطان
العديد من أدوية السرطان الحديثة مستلهمة من جزيئات تنتجها النباتات منذ ملايين السنين. تبحث هذه الدراسة في الأليزارين، صبغة حمراء لامعة توجد في نباتات طبية تقليدية، وتطرح سؤالاً بسيطاً ذو دلالات كبيرة: هل يمكن لهذا المركب الطبيعي القديم، بمفرده أو بالاشتراك مع دواء آخر، أن يساعد في وقف اثنين من أكثر أنواع السرطان شيوعاً في العالم — سرطان عنق الرحم وسرطان البروستاتا؟
مركب نباتي يواجه أوراماً عنيدة
اختبر الباحثون الأليزارين على خليتين بشريتين ورميتين معروفيتين: خلايا هيلّا من سرطان عنق الرحم وخلايا DU145 من سرطان البروستاتا. نَمَت هذه الخلايا في الأطباق التقليدية ثنائية البعد وكذلك كمجموعات ثلاثية البعد مدمجة تشبه الأورام الحقيقية بشكل أفضل. عبر مدى من الجرعات، خفّض الأليزارين بشكل حاد عدد الخلايا الحية القادرة على الانقسام. عند جرعات أعلى، نادراً ما تمكنت الخلايا السرطانية من تشكيل مستعمرات جديدة، مما أظهر أن قدرتها على النمو طويل الأمد تضررت بشدة. والأهم من ذلك، أن الفريق فحص أيضاً الخلايا الليفية الطبيعية ووجد أن هذه الخلايا السليمة كانت أقل حساسية بكثير للأليزارين، مما يشير إلى درجة من الانتقائية لصالح استهداف الخلايا السرطانية.
تشغيل زر الانتحار الخلوي
لم يقُمْ الأليزارين بإبطاء الخلايا فحسب؛ بل دفعها نحو الموت المبرمج. لاحظ العلماء العلامات الكلاسيكية للاستماتة، برنامج "الانتحار" الداخلي للخلايا التالفة. أظهرت الخلايا السرطانية المعالجة بالأليزارين تنشيط إنزيمات الموت الأساسية المسماة الكاسبازات، وتفتت الحمض النووي، وتغيّرات مميزة في شكل الخلية وبنيتها النووية. ارتفعت أيضاً علامات مرتبطة باستجابة تلف الحمض النووي، مثل تنشيط ATM وH2A.X، بالتوازي مع مستوى الاستماتة. في الوقت نفسه، غيّر الأليزارين بروتيناً اسمه Bcl-2، المعروف عادة بمساعدة الخلايا على مقاومة الموت، بطريقة جعلت الخلايا السرطانية أكثر عرضة للموت.
الهجوم على مصانع الطاقة ومسارات الإجهاد
تحت المجهر الإلكتروني بدت الخلايا المعالجة بالأليزارين متوترة بشدة. أصبحت الميتوكوندريا — مصانع الطاقة الصغيرة داخل الخلايا — متورمة، وفقدت بنيتها الداخلية الطبيعية، وظهرت فيها فراغات تشبه الحويصلات. أظهرت القياسات أن الجهد الكهربائي عبر غشاء الميتوكوندريا انهار وأن مستويات أنواع الأكسجين التفاعلية، وهي شكل من أشكال "الصدأ الخلوي" الكيميائي العدواني، ارتفعت بشكل حاد. كما زادت الخلايا من عملية البلعمة الذاتية (autophagy)، وهي عملية تهضم فيها الخلية مكوناتها في محاولة للتعامل مع الإجهاد، ثم تحولت تدريجياً من هذا الوضع النجاة إلى الاستماتة الكاملة مع ارتفاع الجرعة. وبالتوازي، تدخل الأليزارين في مسارين رئيسيين للنمو والبقاء داخل الخلايا السرطانية، المعروفين بمسارات الإشارة PI3K/Akt وMAPK/ERK، والتي تكون غالباً مفرطة النشاط في الأورام ومرتبطة بمقاومة الدواء.
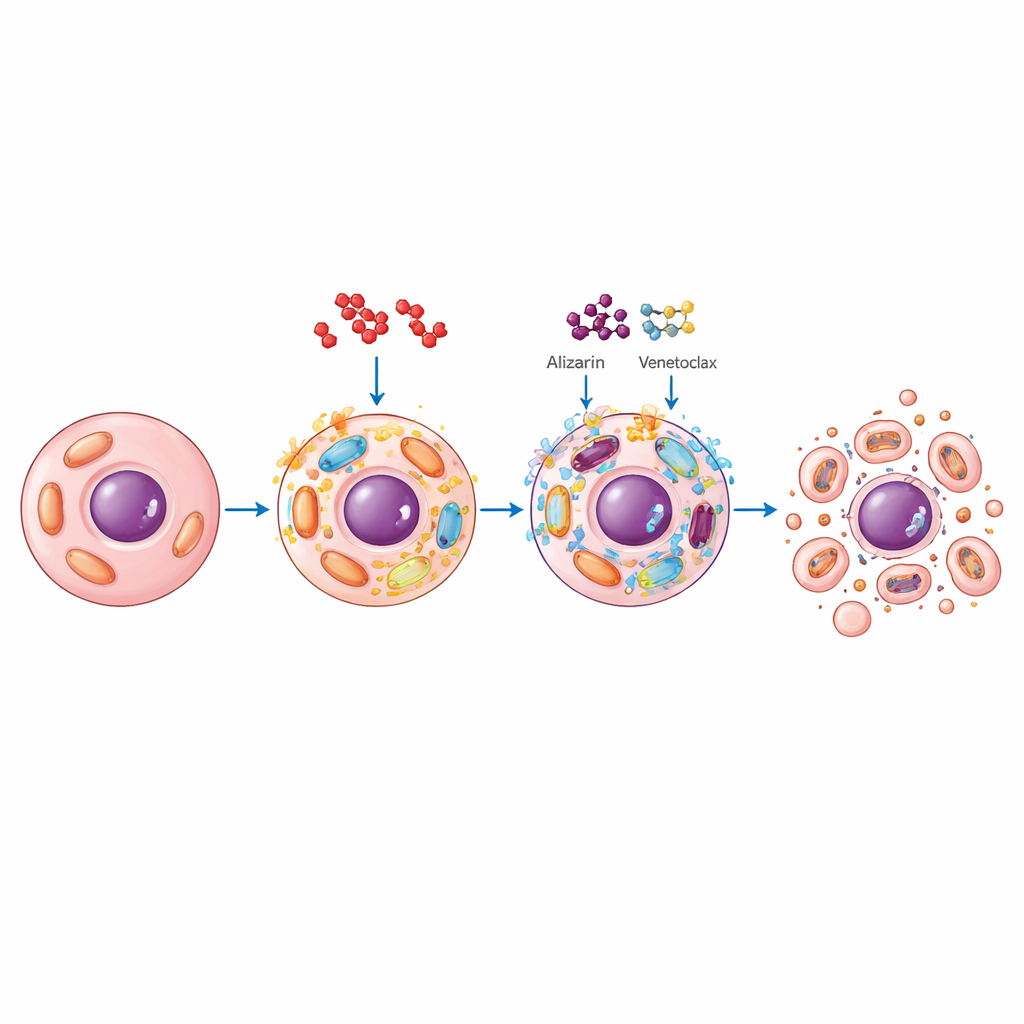
إيقاف الانقسام والحركة وإحداث فوضى انقسامية
بجانب قتل الخلايا السرطانية، تقوّض الأليزارين أيضاً عدة خصائص تجعل الأورام خطرة. أوقف الخلايا في مرحلة G2/M من دورة الخلية، أي قبل وخلال الانقسام، وخفّض بشكل جذري نسبة الخلايا التي كانت تنقسم بنشاط. في اختبارات "الخدش" التي تحاكي الجرح، تحركت الخلايا المعالجة بالأليزارين ببطء أكبر بكثير، ما يشير إلى قدرة مخفضة على الغزو إلى مناطق جديدة. وتحت المجهر، أظهرت العديد من الخلايا سمات "كارثة انقسامية" (mitotic catastrophe)، فشل درامي في الانقسام ينتج خلايا ضخمة مشوهة النواة متعددة أو مجزأة. معاً، تشير هذه التغيرات إلى أن الأليزارين يعطل كل من سلوك النمو والانتشار في الخلايا السرطانية.
أقوى معاً: مزج الأليزارين مع دواء مستهدف
استكشفت الدراسة أيضاً كيف يعمل الأليزارين عند اقترانه بفينيتوكلوكس (Venetoclax)، دواء مستهدف يثبط Bcl-2 ويستخدم حالياً في بعض سرطانات الدم. عندما تم الجمع بين المركبين، ماتت خلايا سرطان عنق الرحم وخصوصاً سرطان البروستاتا بأعداد أكبر مما يحدث مع أي من العاملين بمفردهما، وأظهرت نسبة أكبر من الخلايا تنشيط الكاسبازات وعلامات واضحة للاستماتة. ضعف المزيج أيضاً مسارات البقاء PI3K/Akt وMAPK/ERK بشكل أكبر ونتجت عنه تأثيرات قوية ليس فقط في الزرعات المسطحة ولكن أيضاً في الكريات الشبيهة بالأورام ثلاثية الأبعاد، حيث انهارت بنيتها مع موت مساحات واسعة من الخلايا.
ماذا قد يعني هذا للعلاجات المستقبلية
بعبارات بسيطة، توحي الدراسة أن الأليزارين يهاجم الخلايا السرطانية من جهات عدة في آن واحد: يجهد مصانع طاقتها، يتلف حمضها النووي، يعيق إشارات النمو الأساسية، يتداخل مع انقسام الخلايا، وفي النهاية يدفعها إلى الانتحار المبرمج. وعند تضافره مع فينيتوكلوكس، الذي يستهدف أحد بروتينات البقاء المفضلة لدى السرطان، يصبح التأثير أقوى. وعلى الرغم من أن هذه النتائج محصورة حالياً في نماذج خلوية مخبرية ولا تثبت بعد فائدة علاجية لدى المرضى، فإنها تبرز الأليزارين كشريك واعد في العلاجات التركيبية المستقبلية لسرطانات عنق الرحم والبروستاتا الصعبة العلاج.
الاستشهاد: Trybus, W., Trybus, E. & Król, T. Alizarin induces a multidirectional mechanism of anti-cancer action in cervical cancer and prostate cancer cells. Sci Rep 16, 12843 (2026). https://doi.org/10.1038/s41598-026-43011-y
الكلمات المفتاحية: الأليزارين, سرطان عنق الرحم, سرطان البروستاتا, الاستماتة, العلاج التركيبي