Clear Sky Science · ar
علامة حيوية إذاعية-جينية للعلاج الموجَّه المستند إلى طفرة مستقبل عامل نمو البشرة في سرطان الرئة غير صغير الخلايا
لماذا يهم هذا البحث مرضى سرطان الرئة
لا يزال سرطان الرئة واحداً من أكثر الأورام فتكاً، ولدى كثير من المرضى تكون أفضل آمالهم مرتبطة بعقاقير تستهدف بدقة العيوب الجينية التي تُحرّك أورامهم. ومع ذلك غالباً ما يستلزم اكتشاف هذه العيوب خزعات غازية واختبارات مخبرية معقدة ليست ممكنة أو موثوقة دائماً. تُظهر هذه الدراسة أن معلومات مخفية في فحوصات التصوير المقطعي الروتينية يمكن أن تساعد الأطباء على تحديد نمط جيني مهم في سرطان الرئة غير صغير الخلايا، مما قد يوجِّه المرضى بسرعة أكبر وبشكل أكثر أماناً نحو العلاجات الأكثر احتمالاً لأن تنفعهم.
استخدام الصور بدلاً من الإبر
اليوم، غالباً ما تعتمد خيارات علاج سرطان الرئة على ما إذا كان الورم يحمل تغييرات في جين يُدعى EGFR، والتي قد تجعله حساساً لفئة من الحبوب المعروفة بمثبطات كيناز التيروسين. لاكتشاف هذه التغييرات، يقوم الأطباء عادة بإدخال إبرة أو استخدام منظار لأخذ نسيج من الورم ثم تسلسل حمضه النووي. يمكن أن تكون هذه العملية مؤلمة ومحفوفة بالمخاطر وأحياناً مستحيلة إذا كان الورم صعب الوصول أو كان المريض ضعيفاً. أما الخزعات السائلة المعتمدة على الدم فهي أقل غزوياً لكنها قد تفوِّت طفرات أو تلتقط إشارات مضللة من خلايا طبيعية. هدف مؤلفو هذه الورقة إلى معرفة ما إذا كانت صور التصوير المقطعي، التي يتلقاها تقريباً كل مريض بسرطان الرئة، قادرة على التنبؤ غير الغازي بملف EGFR للورم بطريقة مفيدة إكلينيكياً.
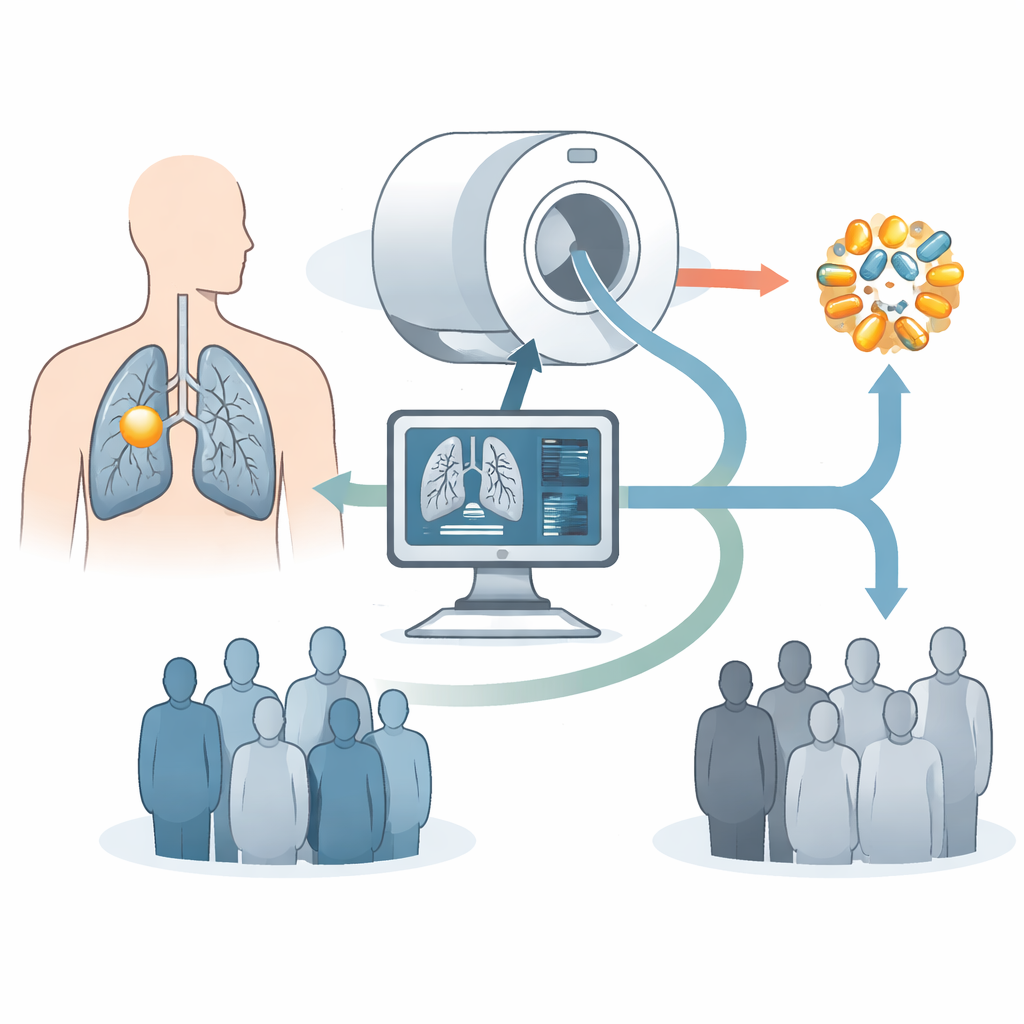
بصمة مخفية في صور التصوير المقطعي
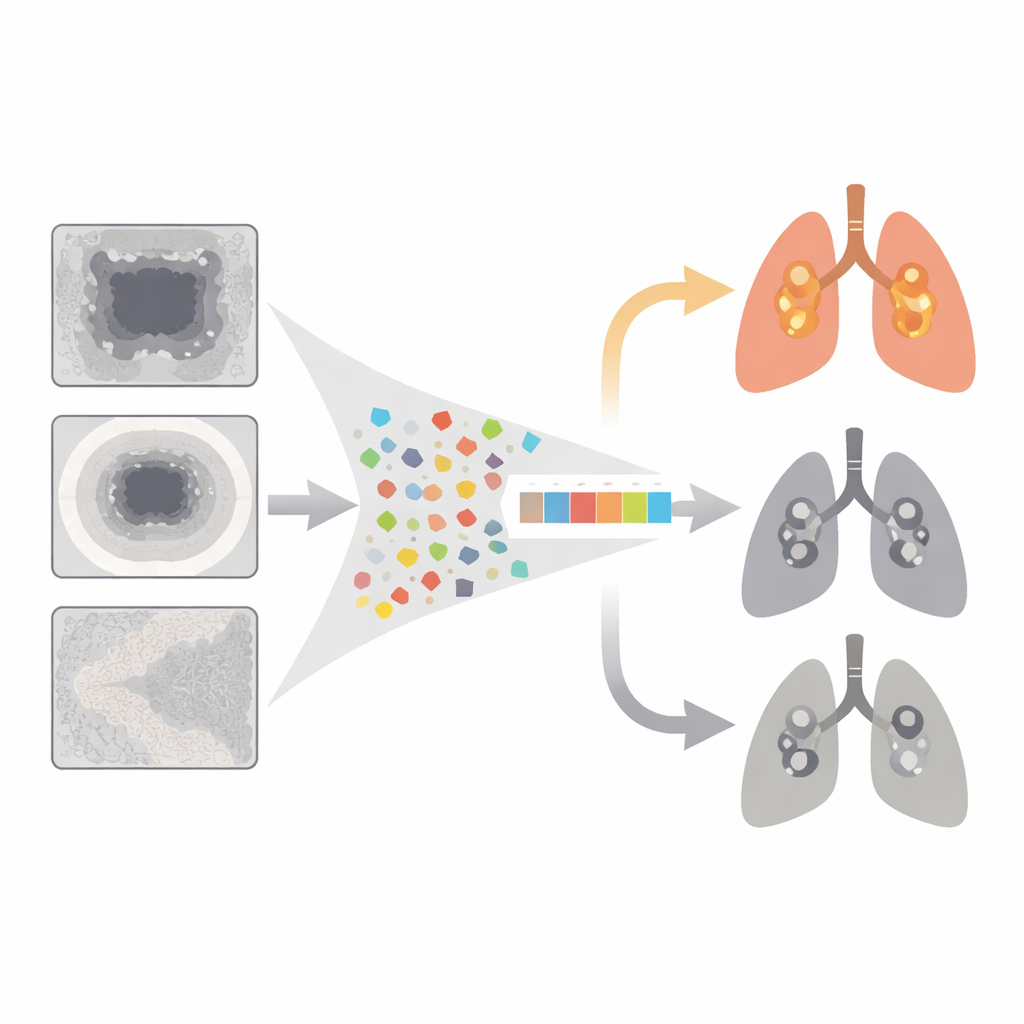
ركَّز الفريق على سيناريو يصفونه بأنه "طفرة EGFR الحصرية": الأورام التي تحمل تغيرات في EGFR لكنها تفتقر إلى طفرات مستهدفة رئيسية أخرى مثل ALK أو KRAS. تميل هذه الأورام إلى الاستجابة بشكل أفضل للعقاقير الموجَّهة إلى EGFR، مما يجعلها مرشحة جذابة للعلاج الخطي الأول. باستخدام صور التصوير المقطعي والبيانات الجينية من 304 مرضى في عدة مستشفيات، بالإضافة إلى مجموعة بيانات عامة مستقلة مكونة من 51 مريضاً، استخرج الباحثون مجموعة كبيرة من القياسات الكمّية الصورية — المسماة ميزات راديومية — من ثلاث مناطق: الورم نفسه، حلقة رقيقة من النسيج المحيط، والرئة القريبة. ثم طبقوا تقنيات إحصائية لتقليص هذه المكتبة إلى توقيع مكوَّن من 10 ميزات مُجمّعة سموه EGFR‑RPV (المتجه التنبُّؤي الراديومي)، مصمَّم لتمييز أورام EGFR الحصرية عن باقي الأورام.
مدى أداء العلامة الصورية
عند اختباره على مرضى لم تُستخدم بياناتهم في بنائه، تعرف EGFR‑RPV بشكل صحيح على الأورام الحاملة لطفرات EGFR الحصرية في نحو ثلاثة من كل أربعة حالات، في مجموعات التحقق الداخلية والخارجية على حد سواء. جاءت العديد من الميزات الصورية الأكثر إفادة من النسيج المحيط مباشرة بالورم بدلاً من نواة الورم، مما يدعم الفكرة القائلة إن الخلايا السرطانية تؤثر في محيطها بطرق دقيقة لكن قابلة للكشف. إحدى الميزات المأخوذة من منطقة الرئة الأوسع حملت إشارة سالبة، مما يتوافق مع الملاحظة السريرية أن أورام EGFR أكثر شيوعاً لدى الأشخاص الذين لا يعانون أضرار رئوية كبيرة ناجمة عن التدخين. بالإضافة إلى التنبؤ بحالة الطفرة، فرّق المقياس الراديومي أيضاً المرضى إلى مجموعات نجاة أعلى وأدنى خطراً، مما يشير إلى أنه يلتقط جوانب أوسع من سلوك الورم.
ربط الصور ببيولوجيا الورم
لدراسة ما قد يفسر أنماط الصور، لجأ الباحثون إلى بيانات نشاط الجينات من المجموعة العامة. وجدوا أن الأورام ذات طفرات EGFR الحصرية كانت تعبر في كثير من الأحيان عن جينين، FAM190A وBCMO1، المتورطين في ضبط انقسام الخلايا وأيضاً في أيض فيتامين أ. أشارت تحليلية مسارات أوسع إلى أن هذه الأورام قد تعتمد على مسار إشارة تطوري يُعرف باسم Hedgehog، مع تقليل بعض البرامج المعتادة للنمو الخلوي السريع والالتهاب. وعلى الرغم من أن هذه الروابط البيولوجية تحتاج إلى تأكيد إضافي، فإنها توحي بأن التوقيع القائم على التصوير المقطعي ليس مجرد خدعة إحصائية، بل يعكس اختلافات حقيقية في طريقة نمو هذه الأورام وتفاعلها مع بيئتها.
ماذا قد يعني هذا للمرضى
من منظور المريض، تكمن جاذبية EGFR‑RPV في عمليته: فهو يستخدم فحوصات التصوير المقطعي القياسية، يمكن حسابه بسرعة، ولا يتطلب إجراء إضافياً. يؤكد المؤلفون أن أداتهم تهدف إلى التكامل، لا الاستبدال، مع فحوصات النسيج والدم. في الحالات التي تكون فيها عينات الخزعة نادرة، أو تكون نتائج الاختبارات متأخرة أو غير واضحة، أو تكون الإجراءات الغازية المتكررة مرهقة، يمكن لتقدير قائم على الصور لحالة EGFR الحصرية أن يساعد في توجيه القرارات — مثل ما إذا كان ينبغي إعطاء أولوية للحبوب الموجَّهة إلى EGFR، توسيع فحوصات الطفرات، أو النظر في استراتيجيات أخرى. وبينما لا تزال هناك حاجة إلى دراسات أكبر ومقدّمة قبل اعتماد هذا النهج على نطاق واسع، يبرز العمل كيف يمكن لتحليل الصور الحديث أن يحوّل الفحوص الروتينية إلى أدلة قوية للعناية الدقيقة بسرطان الرئة.
الاستشهاد: Chen, M., Copley, S.J., Linton-Reid, K. et al. A radio-genomics biomarker for precision epidermal growth factor receptor mutation targeting therapy in non-small cell lung cancer. Sci Rep 16, 12416 (2026). https://doi.org/10.1038/s41598-026-42948-4
الكلمات المفتاحية: سرطان الرئة غير صغير الخلايا, العلاج الموجَّه لمستقبل عامل نمو البشرة (EGFR), الراديوميكس, علامة تصوير مقطعي محوسبة, الطب الدقيق