Clear Sky Science · ar
ريسفيراترول يخفف الألم العصبي المرتبط باستعادة توازن الانقسام والاندماج الميتوكوندري في فئران CCI
تخفيف الألم من مصدر غير متوقع
الألم العصبي—ذاك الألم المحترق أو الرامي أو الشبيه بالصدمة الكهربائية الذي يستمر طويلًا بعد إصابة العصب—يمكن أن يكون مقاومًا بشدة للأدوية الموجودة. تستقصي هذه الدراسة ما إذا كان الريسفيراترول، المركب الطبيعي الشائع في العنب الأحمر والفول السوداني، يمكن أن يخفف هذا النوع من الألم في الفئران عبر حماية محطات الطاقة الدقيقة داخل الخلايا العصبية المسماة الميتوكوندريا. يربط العمل بين جزيء غذائي مألوف والآليات الداخلية للأعصاب المصابة، مقدمًا إشارات قد تلهم يومًا علاجات أكثر لطفًا واستهدافًا للألم المزمن.
عندما يخطئ العصب
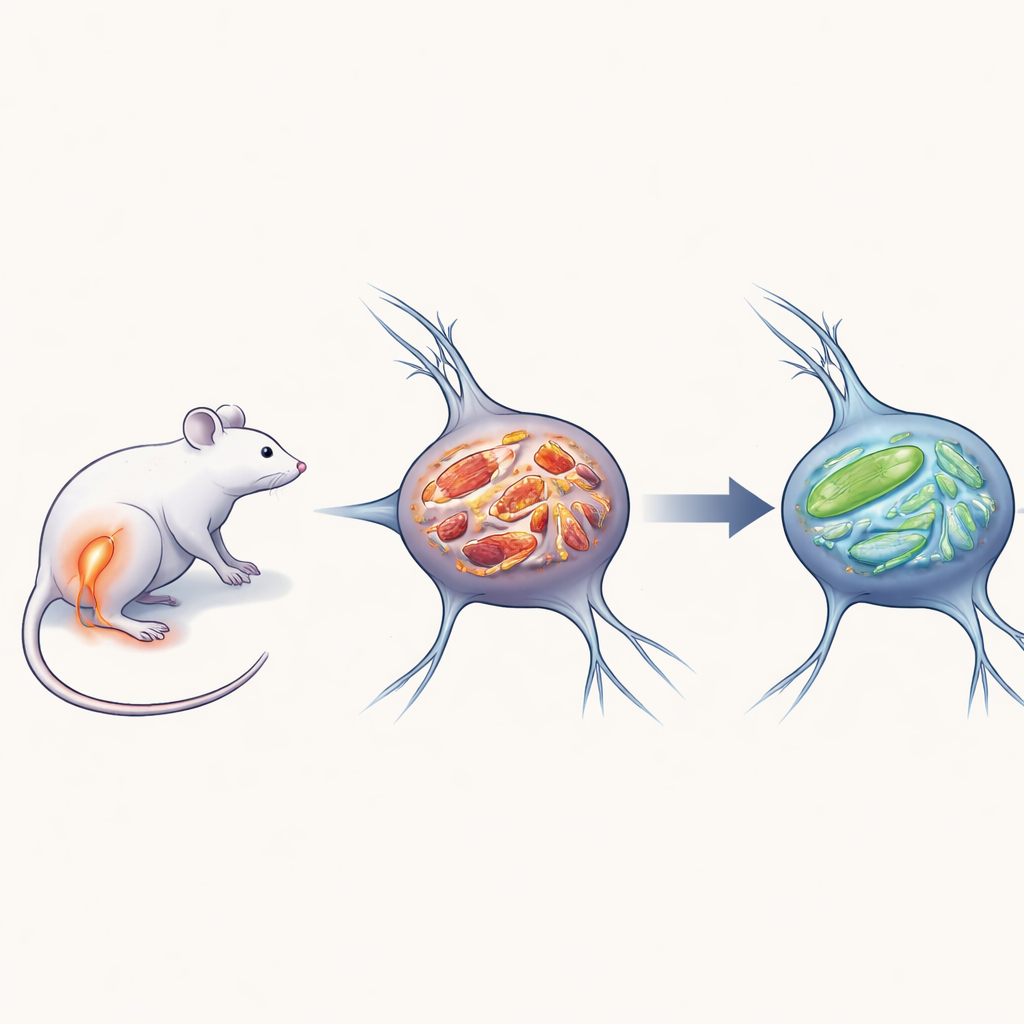
ينشأ الألم العصبي عندما يتعرض الجهاز العصبي نفسه للضرر—على سبيل المثال بعد جراحة أو داء السكري أو عدوى فيروسية. بدلًا من نقل إشارات اللمس أو الحرارة الطبيعية فحسب، تبدأ الأعصاب المصابة في إرسال رسائل خطر مبالغ فيها إلى الدماغ. في هذه الدراسة، استخدم الباحثون نموذجًا فأرِيًا معتمدًا يسمى إصابة الضغط المزمن (chronic constriction injury)، حيث يُربط العصب الوركي في الساق بشكل مرتخٍ لمحاكاة تلف عصبي طويل الأمد. كما كان متوقعًا، أصبحت هذه الفئران شديدة الحساسية للمس الخفيف والحرارة على الجورة المصابة، بما يشبه إلى حد كبير الألم العصبي لدى البشر.
محطات الطاقة تحت الضغط
ركز الفريق على عقدة الجذور الظهرية، مجموعات خلايا عصبية حسية تنقل الإشارات من الجسم إلى الحبل الشوكي. داخل هذه الخلايا، تولد الميتوكوندريا الطاقة وتساعد في السيطرة على تراكم أنواع الأكسجين التفاعلية الضارة—جزيئات كيميائية عدوانية يمكن أن تتلف البروتينات والدهون والحمض النووي. بعد إصابة العصب، وجد الباحثون علامات إجهاد تأكسدي شديد: ارتفعت مستويات أنواع الأكسجين التفاعلية وانخفض نشاط إنزيم وقائي رئيسي، سوبرأوكسيد ديسميوتاز. في الوقت نفسه، ضعفت أجزاء من آلية إنتاج الطاقة الميتوكوندرية، وتحديدًا المركبان I و II من سلسلة التنفّس، مما يوحي بأن محطات الطاقة في الخلايا كانت تتراجع حينما كانت الخلايا العصبية في أمس الحاجة إليها.
توازن دقيق بين الانقسام والالتحام
الميتوكوندريا ليست كتلًا ثابتة؛ فهي تنقسم وتندمج باستمرار في شبكة ديناميكية. تحافظ الخلايا السليمة بعناية على توازن هذه العمليات من «الانقسام» و«الالتحام» للحفاظ على أداء الميتوكوندريا وإزالة الأجزاء التالفة. في خلايا الأعصاب لدى الفئران المصابة، انحاز هذا التوازن نحو انقسام مفرط. ارتفعت مستويات بروتين يدعم الانقسام (DRP1)، في حين انخفض مستوى بروتين يدعم الالتحام (OPA1). تحت المجهر بدا أن الميتوكوندريا في هذه الخلايا أصغر وأكثر عددًا وأكثر تشققًا، مع مساحة أقل ومحيط أقصر وترابط أضعف—وهي سمات شبكة مكسورة تكافح في توفير الطاقة بالتساوي عبر الخلية.
تدخل الريسفيراترول
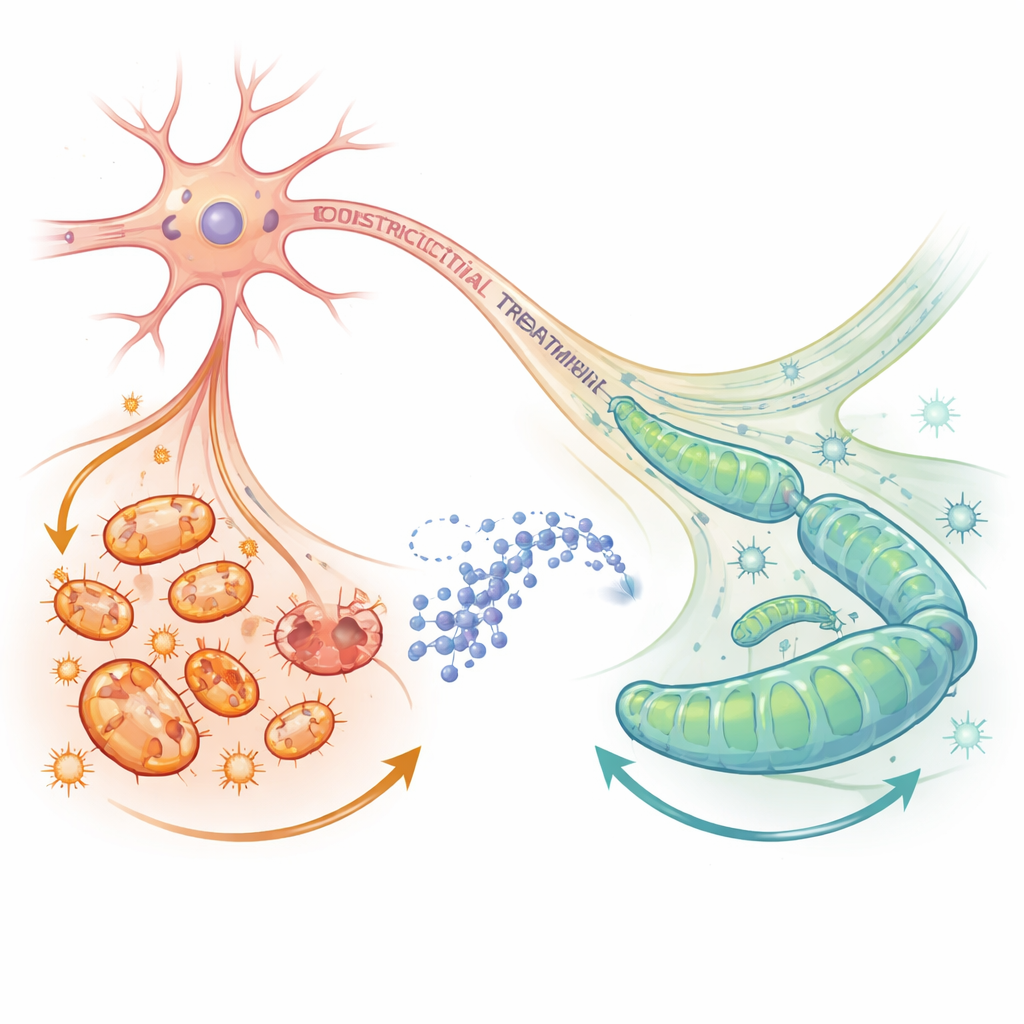
ابتداءً من أسبوع واحد بعد إصابة العصب، قدّم الباحثون جرعة منخفضة من الريسفيراترول مباشرة حول الحبل الشوكي لمدة ثلاثة أيام. خفّض هذا العلاج استجابات الفئران المبالغ فيها للمس والحرارة على الجانب المصاب، مما يدل على تراجع حقيقي في سلوكيات الألم. في عقد الجذور الظهرية، قلّل الريسفيراترول بشكل حاد تراكم الأنواع الأكسجينية التفاعلية وعزّز نشاط الإنزيم الوقائي. كما أعاد مستويات مركبات الميتوكوندريا I و II. والأبرز أن الريسفيراترول أعاد توازن الانقسام–الالتحام نحو الوضع الطبيعي: انخفضت مستويات DRP1، وارتفعت مستويات OPA1، وأصبحت الميتوكوندريا أكبر وأكثر ترابطًا مرة أخرى، مكونة شبكات تشبه إلى حد أكبر تلك الموجودة في الحيوانات غير المصابة.
ما قد يعنيه هذا لرعاية الألم المستقبلية
تشير النتائج مجتمعة إلى أن الريسفيراترول يخفف الألم العصبي في هذا النموذج الفأري جزئيًا عن طريق تهدئة الإجهاد التأكسدي وإعادة بناء شبكات ميتوكوندرية أكثر صحة في الخلايا العصبية الحسية. تتوقف الدراسة عند عدم إثبات أن هذه التغيرات الجزيئية هي السبب المباشر في تخفيف الألم، كما تفحص فقط تأثيرات قصيرة الأجل في نموذج حيواني واحد. مع ذلك، تدعم الفكرة القوية التالية: أن استهداف صحة وشكل الميتوكوندريا، بدلًا من حجب إشارات الألم فقط، قد يفتح مسارًا جديدًا لعلاج الألم العصبي المزمن. قد يساعد الريسفيراترول نفسه، أو أدوية تحاكي تأثيراته على توازن الميتوكوندريا، يومًا ما في تغيير كيفية تعاملنا مع هذه الحالة المُنهِكة.
الاستشهاد: Xie, L., Xu, Y., Yang, Q. et al. Resveratrol alleviates neuropathic pain associated with restoration of mitochondrial fission–fusion balance in CCI mice. Sci Rep 16, 11978 (2026). https://doi.org/10.1038/s41598-026-41965-7
الكلمات المفتاحية: الألم العصبي, ريسفيراترول, الميتوكوندريا, الإجهاد التأكسدي, إصابة العصب