Clear Sky Science · ar
حقن خلايا الميلانوما يحسّن الضعف الإدراكي في نموذج الفأر 5xFAD لمرض الزهايمر
عندما تبدو خلايا السرطان مساعدة للدماغ
مرض الزهايمر والسرطان هما من أكثر الأمراض المثيرة للخوف في الشيخوخة، ومع ذلك كشفت دراسات سكانية نمطًا غريبًا: الأشخاص المصابون بالسرطان يبدو أنهم أقل عرضة لتطوير الزهايمر، وقد يكون المصابون بالزهايمر محميين إلى حد ما من السرطان. تبحث هذه الورقة في هذا اللغز باستخدام فئران تطور لديها تغيّرات دماغية شبيهة بالزهايمر، مطروحة سؤالًا جريئًا: هل يمكن أن يؤدي التعرض لخلايا ورمية إلى تليين مشاكل الذاكرة بشكل غير متوقع عبر تعديل جهاز المناعة في الجسم؟
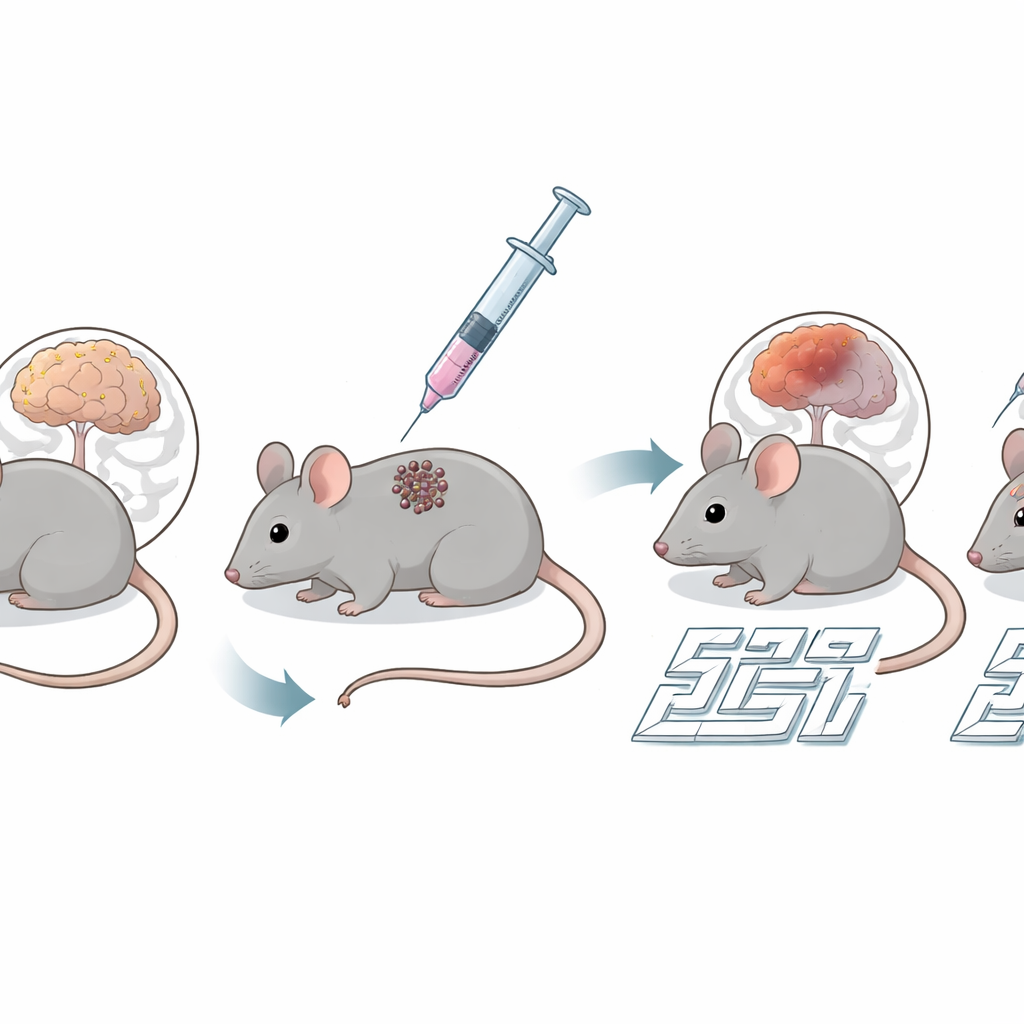
اختبار علاقة غير اعتيادية
عمل الباحثون مع فئران 5xFAD، وهو نموذج مستخدم على نطاق واسع يتطور بسرعة فيه لويحات أميلويد وفقدان للذاكرة يشبه السمات الرئيسية لمرض الزهايمر. في عمر خمسة أشهر، تلقّت هذه الفئران وأشقاؤها الأصحاء حقنًا صغيرة بخلايا ميلانوما تحت الجلد، أو محلولًا ملحيًا غير ضار. خلال الشهر التالي راقب الفريق نمو الأورام وخضع الحيوانات لاختبارين قياسيين للذاكرة المكانية: متاهة بسيطة على شكل حرف Y ومتاهة "واحة" أكثر طلبًا، حيث يجب على الفئران أن تتعلم وتتذكر موقع مكافأة مائية على منصة تحتوي على العديد من الحفر الممكنة.
تحسن الذاكرة دون إزالة اللويحات
تصرّف فئران نموذج الزهايمر التي تلقت المحلول الملحي وحده كما هو متوقع: فقد واجهت صعوبة في التعرف على الذراع الجديدة في متاهة Y وسلكت طرقًا طويلة ومتعرجة للعثور على الماء المخفي في متاهة الواحة. على النقيض الواضح، أدت فئران نموذج الزهايمر التي تم تلقيحها بخلايا الميلانوما أداءً أفضل بكثير. أظهرت تفضيلًا للذراع الجديدة في متاهة Y ومارَت متاهة الواحة بمسارات أكثر مباشرة وكفاءة، محققة معدلات نجاح مماثلة لرفاقها الأصحاء. بدت هذه المكاسب متعلقة بالدرجة الأولى بالذاكرة القصيرة الأمد والذاكرة العاملة. والمفاجئ أن التلوين المفصّل لنسيج المخ أظهر أن مؤشرات الزهايمر الكلاسيكية—عبء لويحات أميلويد-بيتا في القشرة والحُصين—لم تنخفض بعد تلقيح الميلانوما. كما بقي عدد الخلايا الداعمة النجمة الشكل (الخلايا النجمية) والخلايا المناعية المقيمة (الميكروجليا) في الدماغ دون تغيير يُذكر.
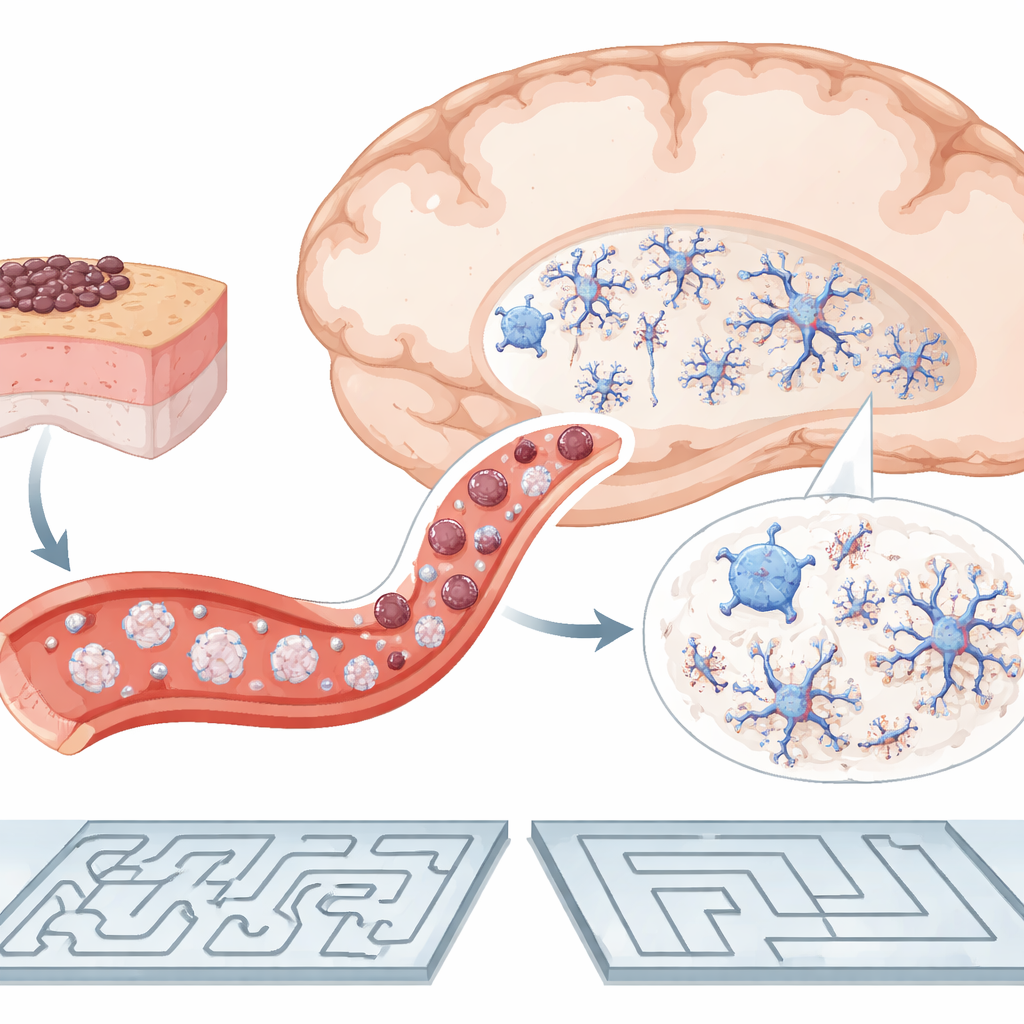
المناعة تتقدم إلى الواجهة
نظرًا لأن تحسين الذاكرة لم يرتبط بانخفاض اللويحات، اتجه العلماء إلى جهاز المناعة كوسيط محتمل. أولًا، لاحظوا أن عددًا أقل من فئران نموذج الزهايمر طورت أورامًا قابلة للقياس مقارنة بالفئران الصحية، وعندما نمت الأورام كانت تميل إلى أن تكون أصغر. يعكس هذا النمط بيانات بشرية تلمّح إلى أن بيولوجيا الزهايمر قد تقاوم السرطان. ومع ذلك ظهرت الفائدة الإدراكية بغض النظر عمّا إذا كان الفأر قد طور ورمًا فعليًا أم لا، مما يوحي أن الإشارة الحاسمة تأتي مبكرًا—ربما من الاستجابة المناعية لخلايا الميلانوما نفسها. في الطحال، العضو المناعي الرئيسي، أظهرت فئران نموذج الزهايمر الملقّحة بالميلانوما زيادة في تجمع الخلايا النخاعية، وهي عائلة تشمل العديد من المدافعين الأماميين وخلايا "التنظيف" النسيجية. على الرغم من أن مستويات الجزيئات الالتهابية الشائعة في الدم لم تتغير بشكل يمكن اكتشافه، فإن هذا التحول يوحي بأن المناعة المحيطية أعيد ضبطها بطريقة قد تؤثر على الدماغ.
خلايا مناعية دماغية أهدأ دون انخفاض أميلويد
لمعرفة كيف يمكن لنشاط المناعة الخارجي أن ينعكس داخل الجمجمة، فحص الفريق الميكروجليا في الحُصين، وهو مركز ذاكرة رئيسي. في فئران نموذج الزهايمر التي أُعطيت المحلول الملحي فقط، كانت الميكروجليا تميل إلى امتلاك أجسام خلوية أكبر وأكثر انتفاخًا—شكل مرتبط بحالة تفاعلية والتهابية. بعد تلقيح خلايا الميلانوما، انكمشت تلك الميكروجليا عائدة إلى شكل أنحف وأكثر تشعبًا في جميع مناطق الحُصين، بما يتفق مع موقف أقل عدوانية. حدث هذا رغم أن العدد الكلي للمايكروجليا بقي ثابتًا ولم تتحرك لويحات الأميلويد. كما قاس الباحثون CXCL10، وهو كيموكين يساعد على استدعاء الخلايا المناعية إلى الدماغ وقد ارتبط بتدهور الإدراك لدى المصابين بالزهايمر. كما هو متوقع، كانت نشاطات جين CXCL10 أعلى في فئران نموذج الزهايمر منها في الضوابط الصحية، لكن تحدي الميلانوما لم يخفض هذه المستويات بوضوح، مما يبرز أن التأثير المفيد قد يعتمد أكثر على إعادة تشكيل دقيقة لسلوك الخلايا المناعية من أن يعتمد على تغييرات واسعة في الإشارات الالتهابية المعروفة.
ما الذي قد يعنيه هذا للعلاجات المستقبلية
تجمَع النتائج لتشير إلى أن لقاءً محيطيًا مع خلايا الميلانوما يمكن أن ينقذ جزئيًا الذاكرة في نموذج فأر شبيه بالزهايمر، ليس بمحو لويحات الأميلويد بل بدفع جهاز المناعة وتهدئة ميكروجليا الدماغ. نفس التلاعب جعل الفئران أيضًا أقل ميلاً لنمو الأورام، ما يعكس الحماية الثنائية التي لوحظت في الدراسات البشرية. وبينما إعطاء خلايا سرطانية عن قصد للمرضى ليس استراتيجية علاجية، تشير الدراسة إلى فكرة واعدة: قد تكون التدخلات المناعية المضبوطة بعناية—ربما لقاحات، أو أدوية نقاط تفتيش مناعية، أو طرق أخرى لمحاكاة تحول المناعة الناتج عن الورم—قادرة يومًا ما على استغلال صلة السرطان–الزهايمر هذه لمنع أو إبطاء تدهور الذاكرة.
الاستشهاد: Bruna-Jara, B., More, J., Lobos, P. et al. Melanoma cell inoculation improves cognitive impairment in the 5xFAD mouse model of Alzheimer’s disease. Sci Rep 16, 11263 (2026). https://doi.org/10.1038/s41598-026-40699-w
الكلمات المفتاحية: مرض الزهايمر, صلة السرطان–الزهايمر, مناعة الدماغ, الميكروجليا, نموذج الميلانوما