Clear Sky Science · ar
أغشية خشبية مُكربوكسلة للالتقاط الانتقائي واسترداد أيونات المعادن الحيوية والتجارية
تحويل الأشجار إلى منظفات للمياه
مع سباق العالم لبناء المزيد من البطاريات، واستخراج المزيد من المعادن، وإعادة تدوير نفايات الصناعية، تتجمع ببطء في أنهارنا وبحيراتنا مخلفات: أيونات معادن مثل الليثيوم والحديد قد تضر بالأنظمة البيئية لكنها أيضًا ثمينة جدًا بحيث تُهدر. تستكشف هذه الدراسة مساعدًا غير متوقع في هذا التحدي — خشب التنوب العادي، مُعدَّل بلطف بمواد كيميائية بسيطة بحيث يستطيع سحب المعادن المفيدة من الماء، مما يحول مادة متجددة ومنخفضة التكلفة إلى مرشح ذكي للتنقية واسترداد الموارد. 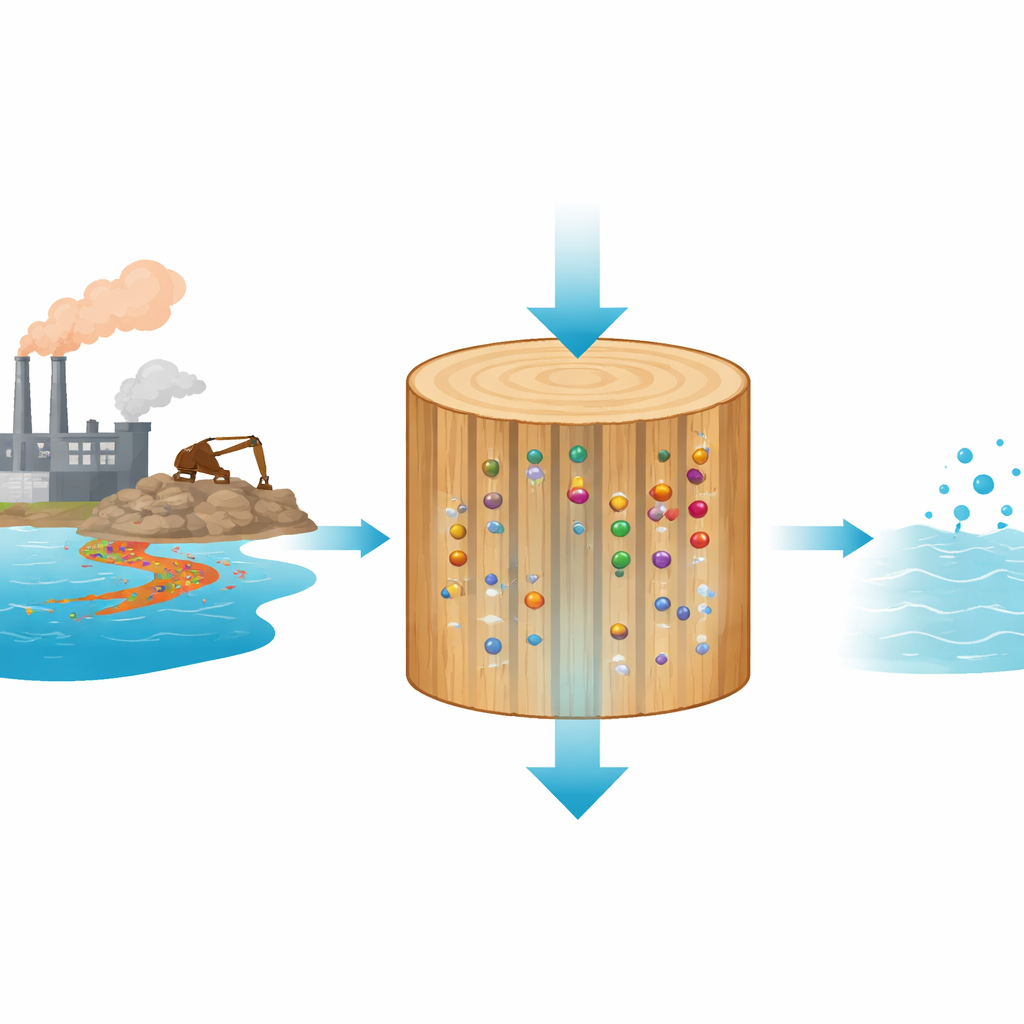
لماذا تشكل المعادن في الماء مشكلة خفية
تتسرّب معادن مثل النحاس والمنغنيز والرصاص والحديد والكوبالت والليثيوم إلى المياه من التعدين وإنتاج البطاريات والطلاء بالكهرباء وغيرها من الصناعات. حتى كميات ضئيلة يمكن أن تكون سامة وتستمر في البيئة لسنوات. الطرق الحالية للمعالجة — مثل التناضح العكسي، والراتنجات المبدلة للأيونات، والمواد الماصة المتقدمة — غالبًا ما تعمل جيدًا لكنها قد تكون مكلفة، مستهلكة للطاقة، عُرضة للانسداد، ومعتمدة على بلاستيك أو سيراميك مشتق من الوقود الأحفوري. لذلك يبحث الباحثون عن مواد حيوية أرخص، وأقل ضررًا للبيئة، وقادرة على التقاط المعادن بشكل انتقائي من المياه الجارية حتى يمكن استعادتها وإعادة استخدامها.
الخشب كأسفنجة طبيعية متدفقة
قد يبدو الخشب غير مرشح محتمل، لكنه يمتلك ميزة مدمجة: شبكة من القنوات الدقيقة الموازية التي كانت تستخدمها الأشجار لنقل الماء. تسمح هذه القنوات الدقيقة بمرور الماء تحت تأثير الجاذبية بينما توفر مسارات طويلة يمكن أن تُحتجز فيها الملوثات. أظهرت أعمال سابقة أن الخشب يمكنه ترشيح الجسيمات والبكتيريا وبعض الملوثات العضوية في المقام الأول عن طريق الاستبعاد الحجمي والامتزاز على السطح. يأخذ مؤلفو هذه الورقة هذه الفكرة أبعد من ذلك: بدلًا من إزالة بنية الشجرة الطبيعية، يحتفظون بالخشب سليمًا ويضيفون مجموعات كيميائية يمكنها استبدال أيونات غير ضارة موجودة في الخشب بأيونات المعادن في الماء.
تعديلات كيميائية ذكية لسطح الخشب
عالج الفريق أقراصًا رقيقة من التنوب بمادتين صغيرتين — أنهيدريد السكسينيك وأنهيدريد الماليك — اللتين تتفاعلان مع مجموعات «القبضات» الطبيعية في الخشب لإدخال مجموعات كربوكسيل قادرة على حمل أيون الصوديوم. بعد خطوة «شحن» منفصلة بمحلول الصوديوم، تعمل هذه المواقع الحاملة للصوديوم كنقاط تبادل: عندما يمر ماء يحتوي على الليثيوم أو الحديد، تُطلق أيونات الصوديوم ويحتل أيون المعدن مكانها. أكدت اختبارات الطيف تحت الحمراء والمجهر الإلكتروني وتشتت الأشعة السينية وتحليل الحرارة وامتصاص الرطوبة أن هذه المواقع الجديدة رُكبت بنجاح دون تدمير بنية قنوات الخشب. أضافت معالجة السكسينيك مزيدًا من هذه المجموعات لكنها سببت تراكمًا وتشوّهًا وهشاشة في الخشب، بينما أضافت معالجة المالِيك عددًا أقل قليلاً من المجموعات لكنها حافظت على الصلابة والهيكل العام بشكل أفضل بكثير.
مدى فعالية مرشحات الخشب عمليًا
تحت ترشيح مدفوع بالجاذبية — دون مضخات، مجرد صب ماء فوقها — خضعت أقراص الخشب المعدلة لتحدي محاليل مخففة من الليثيوم والحديد عبر ثلاث دورات إعادة استخدام. أزالت الأغشية المعالجة بالمالِيك تقريبًا كل الليثيوم (حوالي 99.9٪) وحافظت على هذا الأداء عبر الاستخدام المتكرر، بينما كانت الأغشية المعالجة بالسكسينيك أكثر تباينًا وعادة ما التقطت نحو 90٪. بالنسبة للحديد، كان الفرق أوضح: أزال الخشب المعالج بالمالِيك تقريبًا 72٪ من الحديد المذاب بثبات، أفضل بكثير من نسخة السكسينيك، وبفارق كبير عن الخشب غير المعدل الذي لم يحفظ أي معدن تقريبًا. أظهرت اختبارات التوازن المنفصلة أن المعدنين يرتبطان بطبقة موحدة من المواقع التي تتصرف مثل طلاء أحادي الطبقة، مع ارتباط أقوى للحديد مقارنة بالليثيوم — وهو ما يتسق مع شحنته الأعلى وقدرته على الالتصاق بعدة مجموعات كربوكسيل في وقت واحد. 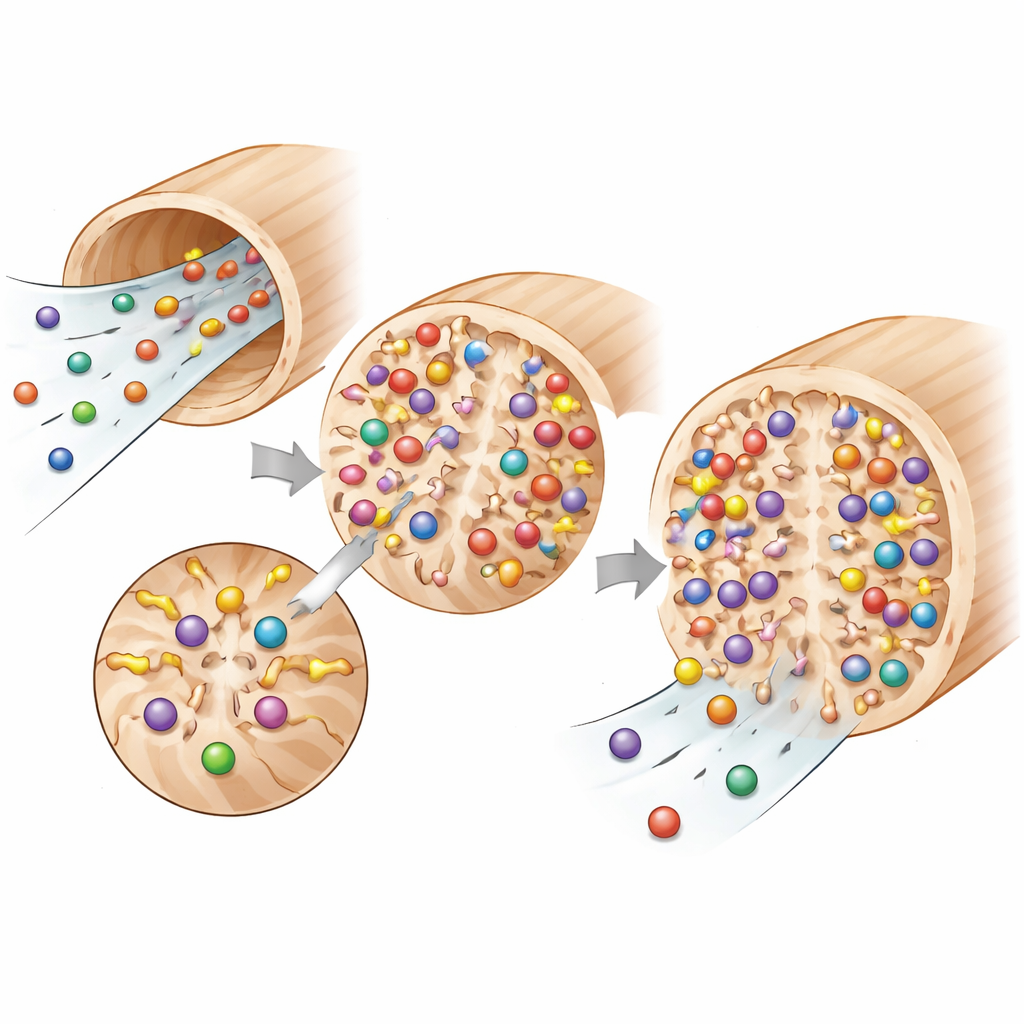
ما الذي يجعل الخشب المعالج بالمالِيك مميزًا
ينبسط التفوق في أداء الخشب المعالج بالمالِيك إلى كيفية ترتيب المجموعات المضافة ومدى سهولة احتفاظها بالشحنة في الماء. يميل أنهيدريد المالِيك إلى وضع مجموعتي كربوكسيل متقاربتين، مما يسمح بالربط متعدد الأسنان حيث يمكن لأيون الحديد الواحد أن يُمسك بعدة «أذرع» في وقت واحد. كما يجعل السطح أكثر حمضية، لذا تظل هذه المواقع فعالة عبر نطاق واسع من قيم الأس الهيدروجيني النموذجية للمجاري المائية الحقيقية. في المقابل، يباعد أنهيدريد السكسينيك مجموعات الكربوكسيل أكثر ويكون أكثر حساسية لتغيرات صغيرة في الأس الهيدروجيني، لذا ليست كل المواقع متاحة في جميع الأوقات. وحتى وإن حمّلت معالجة السكسينيك عددًا أكبر من المجموعات إجمالًا في الخشب، فإن العديد منها أقل فعالية عمليًا، والتعديل الأثقل يضعف الاستقرار الميكانيكي.
من مفهوم مخبري إلى استرداد معادن أكثر خضرة
بعبارات بسيطة، تُظهر هذه الدراسة أن ترقية كيميائية بسيطة يمكن أن تحول شريحة من التنوب إلى مرشح قابل لإعادة الاستخدام ينظف الماء ويلتقط المعادن التي تستحق الاسترداد. يحقق الخشب المعالج بالمالِيك، بشكل خاص، توازنًا واعدًا بين القوة وتدفق الماء والتقاط المعدن، حيث يزيل تقريبًا كل الليثيوم وحصة كبيرة من الحديد بينما يسمح بمعدلات عملية عملية تحت الجاذبية وحدها. على الرغم من أن العمل المستقبلي يجب أن يختبر هذه الأغشية في خليط أكثر تعقيدًا — حيث ستتنافس الأيونات الشائعة مثل الصوديوم والكالسيوم والمغنيسيوم على المواقع — يشير المفهوم إلى مرشحات قائمة على المواد الحيوية ومنخفضة التكلفة تساعد على إغلاق حلقات استخدام المعادن، وتقليل النفايات من صناعات ناشئة مثل تصنيع البطاريات، والاستفادة من قدرة ترشيح مادة مألوفة ومتجددة مثل الخشب.
الاستشهاد: Sánchez-Ferrer, A., Upadhye, D., Ahmed, M.J. et al. Carboxylated wood membranes for selective capture and recovery of critical and commodity metal cations. npj Clean Water 9, 36 (2026). https://doi.org/10.1038/s41545-026-00577-4
الكلمات المفتاحية: أغشية خشبية, إزالة أيونات المعادن, استرداد الليثيوم, معالجة مياه مستدامة, ترشيح قائم على مواد حيوية