Clear Sky Science · ar
الترانسأمينة البيومحاكاة غير المتناظرة للفوسفونات α-كيتو ممكنة بفضل البيريدوكسامينات الكيرالية والمذيب التآزري
لماذا هذا مهم للأدوية المستقبلية
تعتمد العديد من الأدوية الحديثة على تفاصيل ثلاثية الأبعاد دقيقة تجعل شكل المرآة الواحد من الجزيء أكثر نفعًا بكثير من الآخر. تتناول هذه الدراسة كيفية بناء مثل هذه الجزيئات المشكَّلة بدقة بطريقة أنظف وأكثر كفاءة. يقلّد الباحثون الطريقة التي تنقل بها الإنزيمات في الخلايا الحية ذرات النيتروجين لصنع مركبات أساسية تسمى أمينوفوسفونات، والتي تظهر في المضادات الحيوية، علاجات السرطان، وإمكانات لعلاجات الزهايمر. من خلال تقليد استراتيجية الطبيعة باستخدام جزيئات صغيرة قابلة للتعديل، يفتحون مسارًا لطرق أسرع وأكثر استدامة لصنع أدوية مستقبلية.
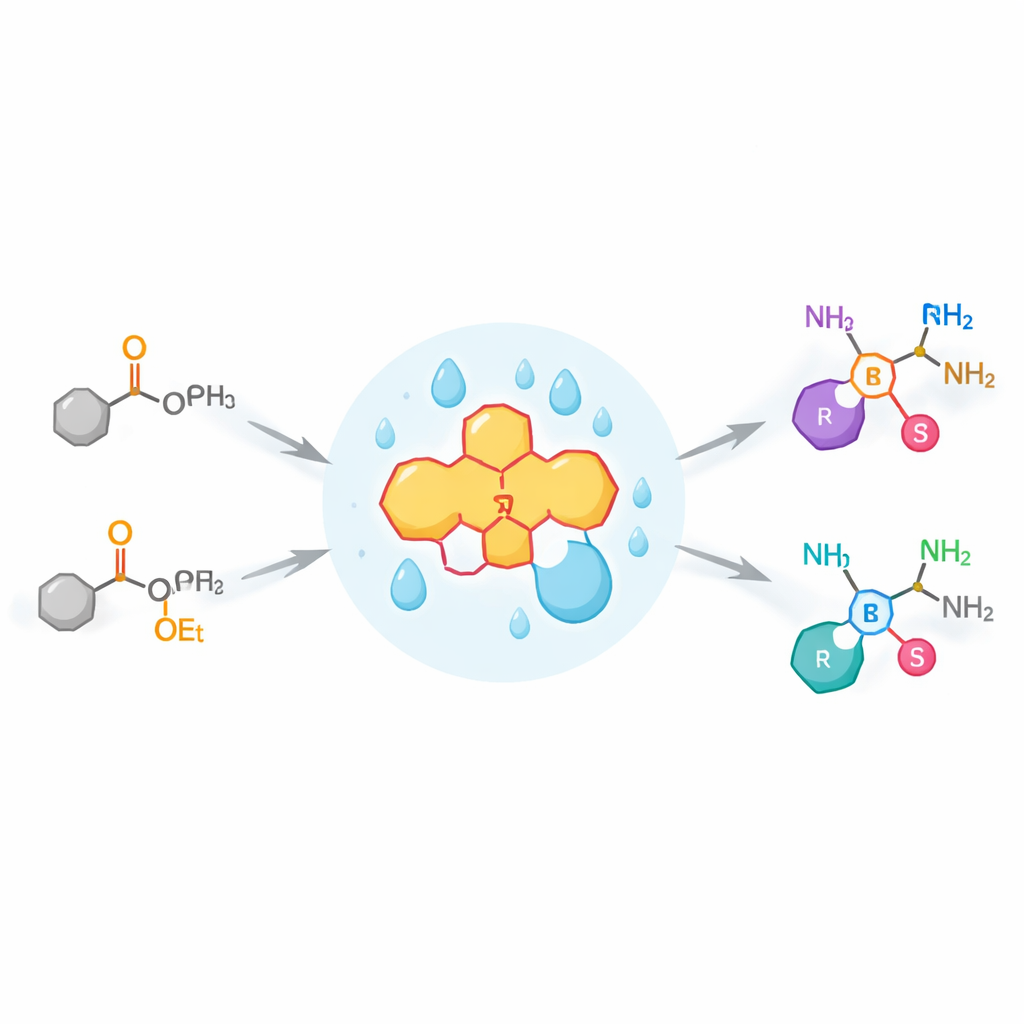
خدعة الطبيعة لبناء الأمينات
في الأحياء، تحوّل الإنزيمات بانتظام وحدات الكربون–الأكسجين البسيطة في الجزيئات إلى وحدات كربون–نيتروجين، مكوِّنة أمينات مركزية في كيمياء الحياة. يتم ذلك عبر عملية تسمى الترانسأمينة، حيث تُنقَل ذرة نيتروجين من جزيء إلى آخر عبر سلسلة من تحولات البروتون المنسقة بدقة. تعلم الكيميائيون الصناعيون بالفعل استخدام الإنزيمات الطبيعية المعروفة بالترانسأمينازات على نطاق واسع لصنع الأمينات الكيرالية. لكن هذه الإنزيمات انتقائية: تعمل بأفضل شكل على الركائز الطبيعية وغالبًا ما تواجه صعوبة مع الأهداف «غير الطبيعية» التي يهتم بها مصممو الأدوية، مثل الكيتونات المحتوية على الفوسفور الخاصة المعروفة باسم α-كيتو فوسفونات.
الاستهداف لجزيئات خاصة تحتوي على الفوسفور
تشبه المركبات المعروفة باسم α-أمينوفوسفونات الكيرالية الأحماض الأمينية لكنها تحوي ذرة فوسفور في موضع عادة ما يكون كربونًا في الطبيعة. يمنح هذا الاستبدال الصغير خواصًا إلكترونية غير معتادة ويجعلها قادرة على حجب أو ضبط المسارات البيولوجية، على سبيل المثال في بناء جدار الخلية البكتيرية، إنزيمات متعلقة بالعظام، أو مستقبلات الدماغ. تتطلب الطرق الكيميائية التقليدية لصنعها عادة مجموعات حماية على النيتروجين وعدة خطوات منفصلة لإضافة هذه المجموعات، تعديلها ثم إزالتها. سعى المؤلفون إلى إيجاد طريقة مبسطة وعامة تُنتج هذه الجزيئات القيمة مباشرة في شكلها الحر غير المحمي، وبيد واحدة مفضّلة من المرآة.
اقتراض استراتيجية فيتامين ب6
لتحقيق ذلك، صمّم الفريق محفزًا جزيئيًا صغيرًا مستوحى من فيتامين ب6، الذي تستخدمه الطبيعة في العديد من تفاعلات الإنزيمات المتعلقة بالأحماض الأمينية. يشكل محفزهم البيريدوكسامين الكيرالي شراكة مؤقتة مع α-كيتو الفوسفونات، مكونًا وسطًا يمكنه إعادة ترتيب ذرات الهيدروجين داخليًا. وفي الوقت نفسه، يخدم مشتق حمض أميني بسيط كمانح للنيتروجين، مكملاً دورة «تبادل النيتروجين» الكاملة التي تُحاكي عن كثب كيفية عمل الإنزيمات الحقيقية. كان الاكتشاف الرئيسي أن المذيب ثلاثي فلوروإيثانول ليس وسطًا خاملًا فحسب: بل ينظم بدقة شبكة روابط هيدروجينية حول الشركاء المتفاعلين، موجهًا التفاعل بحيث يُفضَّل بقوة أحد نواتج المرآة.
مدى واسع واستخدامات عملية
تحت شروط لطيفة وفي درجة حرارة الغرفة، يحوّل هذا النظام المستوحى من فيتامين ب6 العديد من α-كيتو الفوسفونات المختلفة إلى α-أمينوفوسفونات كيرالية بعائد عالٍ ومع تفضيل يصل إلى 98% ليد واحدة. تتحمّل الطريقة الحلقات العطرية، سلاسل الكربون الطويلة، الروابط الثنائية والثلاثية، والقطع الضخمة الشبيهة بالأدوية. في عدة حالات، تكون المنتجات نظائر مباشرة لأحماض أمينية طبيعية، مما يُظهر كيف يمكن للطريقة أن تُنتج نسخًا معدلة بالفوسفور من اللبنات البيولوجية المألوفة. كما نجح المؤلفون في توسيع التفاعل على نطاق أكبر وأظهروا أن بضع خطوات متابعة بسيطة تحول هذه المنتجات إلى جزيئات متقدمة، بما في ذلك مثبط معروف لإنزيمات إعادة تشكيل الأنسجة ونظير لدواء معتمد لعلاج السرطان.
نظرة تحت الغطاء
لفهم سبب انتقائية التفاعل، أجرى الفريق محاكاة حاسوبية مفصلة لمنظومة الطاقة على طول مسار التفاعل. تُبرز هذه الحسابات خطوة معينة يُنقل فيها ذرة هيدروجين لتكوين المنتج الكيرالي النهائي. في المسار المفضل، يقفل المحفز ومركز الكربون المتفاعل وجزيئات المذيب معًا في نمط روابط هيدروجينية مدمج يكون أقل طاقة من الترتيب المنافس المؤدي إلى المرآة المقابلة. يشرح التحليل أيضًا سبب تفوق المذيبات الكحولية الأكثر مسخنةًا إلكترونيًا، مثل ثلاثي فلوروإيثانول، على الكحوليات العادية مثل الإيثانول: فهي تُثبّت حالة العبور الأساسية بشكل أفضل وتُحسّن قدرة النظام على التمييز بين المنتجات اليمنى واليسرى.
الخلاصة العامة
تُظهر هذه الدراسة أن الجزيئات الصغيرة المصممة بعناية يمكن أن تُحاكي الرقص الدقيق للإنزيمات، ليس فقط في نقل الذرات ولكن أيضًا في استخدام المذيب المحيط كشريك في التحكم. من خلال تحويل كيتونات بسيطة محتوية على الفوسفور مباشرة إلى أمينوفوسفونات كيرالية نقية وعارية من الحماية، تُقصّر الطريقة طرق التخليق إلى أهداف بيولوجية معقدة ونشطة. للمختصين غير المتخصصين، الخلاصة أن الكيميائيين يقتربون من بناء جزيئات شبيهة بالأدوية بنفس أناقة وكفاءة الخلايا الحية، وهو ما قد يعني في النهاية وصولًا أسرع وأنظف إلى علاجات جديدة.
الاستشهاد: Cai, D., Huang, L., Wang, Z. et al. Asymmetric biomimetic transamination of α-keto phosphonates enabled by chiral pyridoxamines and synergistic solvent. Nat Commun 17, 2750 (2026). https://doi.org/10.1038/s41467-026-69567-x
الكلمات المفتاحية: التحفيز البيومحاكى, أمينوفوسفونات كيرالية, كيمياء مستوحاة من فيتامين ب6, التحضير غير المتماثل, تفاعلات الترانسأمينة