Clear Sky Science · ar
الـRNA N6-ميثيلأدينوزين (m6A) ينظم تقدم دورة الخلية في الورم الدبقي المنتشر في منتصف الدماغ (DMG) ويمنح حساسية تجاه تثبيط FTO
لماذا تهم العلامات الصغيرة على الـRNA في أورام دماغ الأطفال
تعد الأورام الدبقية المنتشرة في منتصف الدماغ من أخطر سرطانات الدماغ عند الأطفال، حيث يعيش معظم الأطفال أقل من سنة بعد التشخيص وتتوافر خيارات علاجية قليلة ذات فاعلية. تدرس هذه الدراسة زاوية غير متوقعة: علامات كيميائية صغيرة على جزيئات الـRNA، التي تساعد على تحويل الجينات إلى بروتينات. من خلال رسم خرائط لهذه العلامات في خلايا الورم وتجربة دواء يغيرها، يكشف الباحثون عن نقطة ضعف جديدة في هذه السرطانات ويقترحون استراتيجية علاجية جديدة.
كيف يشكل رمز مخفي على الـRNA سلوك الورم
داخل كل خلية، تحمل جزيئات الـRNA رسائل من الـDNA إلى آلية تصنيع البروتينات. العديد من هذه الرسائل مزينة بعلامة كيميائية صغيرة تسمى m6A، والتي يمكن أن تغيّر مدة بقاء الـRNA أو مدى استخدامه. ركز الفريق على الورم الدبقي المنتشر في منتصف الدماغ، وهو ورم دماغي طفولي يُعتقد أنه ينشأ من خلايا داعمة غير ناضجة في الدماغ ويحركه تغييرات قوية في كيفية تغليف الـDNA. وبما أن m6A تساعد في التحكم بتطور هذه الخلايا غير الناضجة، افترض المؤلفون أن هذا "الشفرة بعد النسخ" قد تكون أيضاً حاسمة لنمو الورم.
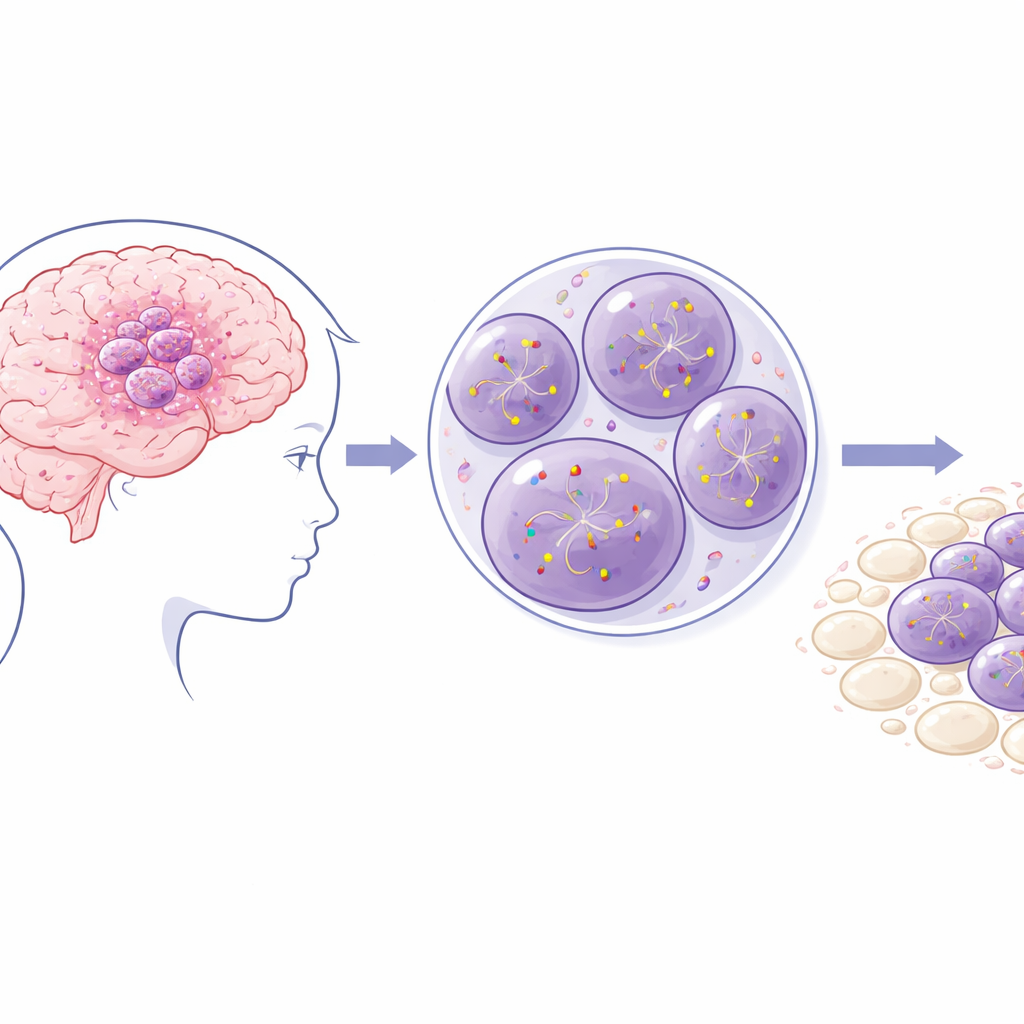
رسم خرائط لعلامات الـRNA في أورام دماغ قاتلة
باستخدام تسلسل الـRNA المباشر، القادر على قراءة جزيئات الـRNA الفردية وكشف علاماتِها الكيميائية، أنشأ الباحثون أول خرائط عالية الدقة لـm6A في خلايا مأخوذة من أورام دبقية منتشرة في منتصف الدماغ لدى الأطفال ومن نسيج دماغي غير سرطاني. حملت خلايا الورم مستويات أعلى بكثير من m6A بشكل عام، خصوصاً على الـRNAs المرتبطة بحركة الخلية والغزو — الصفات التي تساعد السرطان على الانتشار في الدماغ. على النقيض من ذلك، كانت مجموعة أصغر من الـRNAs التي انخفضت فيها مستويات m6A في الأورام منخرطة بشدة في دورة الخلية وفصل الكروموسومات، العملية المنسقة بدقة التي تسمح بانقسام الخلايا. أقترح النمط أن مثيلة الـRNA تساعد الأورام على الحفاظ على هويتها العدوانية الشبيهة بالخلايا الجذعية بينما تضبط آلية الانقسام السريع للخلية.
إيقاف ممحاة الـRNA يبطئ انقسام خلايا الورم
علامة m6A ليست دائمة؛ فهناك إنزيمات تضيفها وأخرى تزيلها. اختبر المؤلفون أدوية تحجب جانبي هذا النظام في خلايا الورم: METTL3 الذي يضيف العلامة، وFTO الذي يمحوها. لم يُظهر تثبيط METTL3 تأثيراً يذكر حتى بجرعات عالية. بالمقابل، أدت حجب FTO بمركب صغير يسمى FB23‑2 إلى انخفاض حاد في بقاء خلايا الورم مع حفاظٍ على الخلايا الدماغية غير السرطانية عند جرعات مماثلة، مما يوحي بوجود نافذة علاجية. كشفت تجارب المجهر وقياس التدفق الخلوي أن الخلايا المعالجة تراكمت في طور نسخ الـDNA من دورة الخلية ثم دخلت في موت مبرمج، ما يدل على أن عملية انقسامها تعرضت للإجهاد والتوقف.
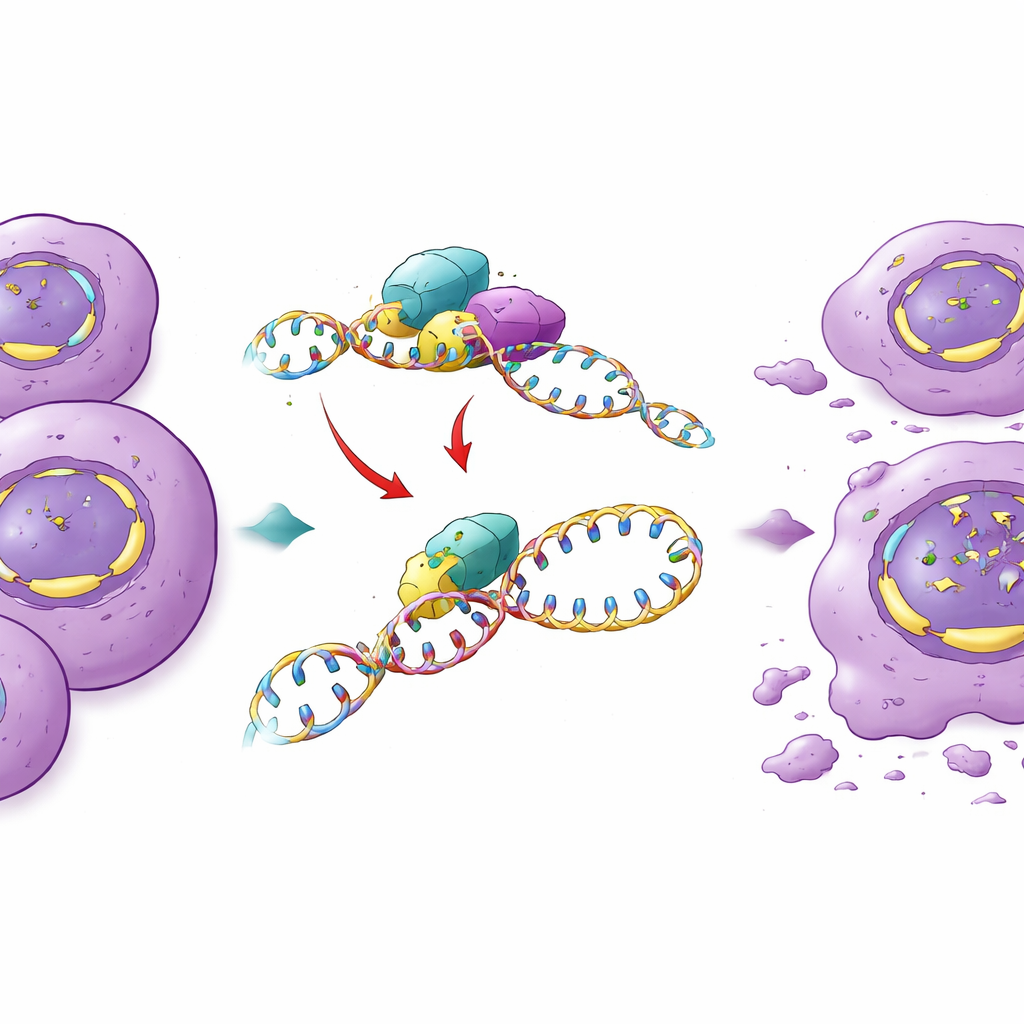
ما الذي يتغير داخل الخلية عند حجب FTO
لفهم سبب تأثير تثبيط FTO بشدة على خلايا الورم، قاس الفريق التغيرات الشاملة في مستويات الـRNA والبروتين بعد المعالجة. عبر ثلاث مزروعات ورمية مختلفة، خفّض FB23‑2 بصورة متسقة السائقين الرئيسيين لدورة الخلية، بما في ذلك العديد من مكونات الآلية التي تفصل الكروموسومات، بينما شغّل جينات تستجيب لتلف الـDNA والضغط الخلوي. حملت العديد من هذه الـRNAs علامات m6A وكان معروفاً تفاعلها مع YTHDF2، البروتين الذي يتعرف على m6A ويعزز تحلل الـRNA — وهو عامل أيضاً وُجد بمستويات مرتفعة في هذه الأورام. أكدت تسلسلات الـRNA المباشرة بعد المعالجة أن بعض المواقع التي كانت منخفضة m6A بشكل غير اعتيادي في الأورام استعادت جزئياً هذه العلامات عند تثبيط FTO، لا سيما في الجينات التي تتحكم بدورة الخلية. أظهرت قياسات البروتين المطابقة انخفاضات موازية في منظمات دورية مركزية للخلية وزيادات في مؤشرات الاستماتة، مما يعزز الصورة القائلة بأن FTO يساعد الأورام في الحفاظ على انقسام سريع ومنظم.
فرص وتحديات جديدة للعلاج
تُظهر هذه النتائج معاً أن الأورام الدبقية المنتشرة في منتصف الدماغ تعتمد على توازن دقيق من مثيلة الـRNA للحفاظ على نموها، وأن قلب هذا التوازن بتثبيط FTO يمكن أن يختنق قدرتها على التكاثر والبقاء. بالنسبة للقارئ غير المتخصص، الرسالة الأساسية هي أن خلايا السرطان في هذه الأورام الدماغية الطفولية تعتمد بشكل غير عادي على علامة كيميائية قابلة للعكس على الـRNA الخاص بها، وأن الأدوية المستهدفة للإنزيم الذي يزيل هذه العلامة يمكن أن تُضعفها بشكل انتقائي. وبينما لا تعبر مثبطات FTO الحالية الحاجز الدماغي بعد، تبرز هذه الدراسة مساراً ملحاً وواعداً: تطوير أدوية قادرة على اختراق الدماغ، أو طرق توصيل جديدة، تستغل بأمان هذه النقطة الضعيفة لتقديم خيارات علاجية أكثر فاعلية للأطفال.
الاستشهاد: Ross, S.E., Holliday, H., Wang, E. et al. RNA N6-methyladenosine (m6A) regulates cell cycle progression in diffuse midline glioma (DMG) and confers sensitivity to FTO inhibition. Cell Death Dis 17, 371 (2026). https://doi.org/10.1038/s41419-026-08647-8
الكلمات المفتاحية: الورم الدبقي المنتشر في منتصف الدماغ, مثيلة الـRNA, m6A, تثبيط FTO, سرطان دماغي طفولي