Clear Sky Science · ar
تحديد الاستجابات تحت الخلوية للغشاء الزليلي في بداية التهاب مفصل الفك الصدغي عبر نماذج الإجهاد الميكانيكي وتشوه قرص المفصل
لماذا يهم تآكل مفصل الفك
مفصل الفك، أو المفصل الصدغي الفكي (TMJ)، هو ما يتيح لك المضغ والتحدث والتثاؤب. عندما يبدأ في الانهيار — حالة تُعرف بالتهاب مفصل الفك التنكسي — قد يعاني الأشخاص من ألم مزمن وصعوبة في الأكل وتراجع نوعية الحياة. ومع ذلك، مقارنة بالركبتين أو الوركين، فقد حُدِث دراسة أقل على هذا المفصل الصغير والمعقد. تستخدم هذه الورقة أدوات رسم خرائط جينية متطورة في نماذج فأرية لكشف ما يحدث داخل البطانة الرقيقة للمفصل عند بداية التهاب مفصل الفك التنكسي، بتفصيل غير مسبوق.
طريقتان لتحميل مفصل الفك زيادة على الحد
لمحاكاة المشكلات الشائعة لدى المرضى، أنشأ الباحثون نوعين من تلف المفصل في الفئران. في أحدهما، عدلوا كيفية التقاء الأسنان بحيث أغلق الفك بطريقة مائلة، مما حمّل المفصل مرارًا وتكرارًا — وهذا يمثل الإجهاد الميكانيكي الناتج عن سوء إطباق الأسنان. في النموذج الآخر، سحبوا قرص التوسيد داخل المفصل جراحيًا إلى الأمام وربطوه في موضع خاطئ، مقلدين قرصًا منزاحًا غالبًا ما يرتبط بألم المفصل. تمت مقارنة كلا النموذجين مع حيوانات ضابطة سليمة على مدى ثلاثة أسابيع، بينما قيس تغير البنية العظمية والنسجية باستخدام تصوير ثلاثي الأبعاد بالأشعة والمجهر. 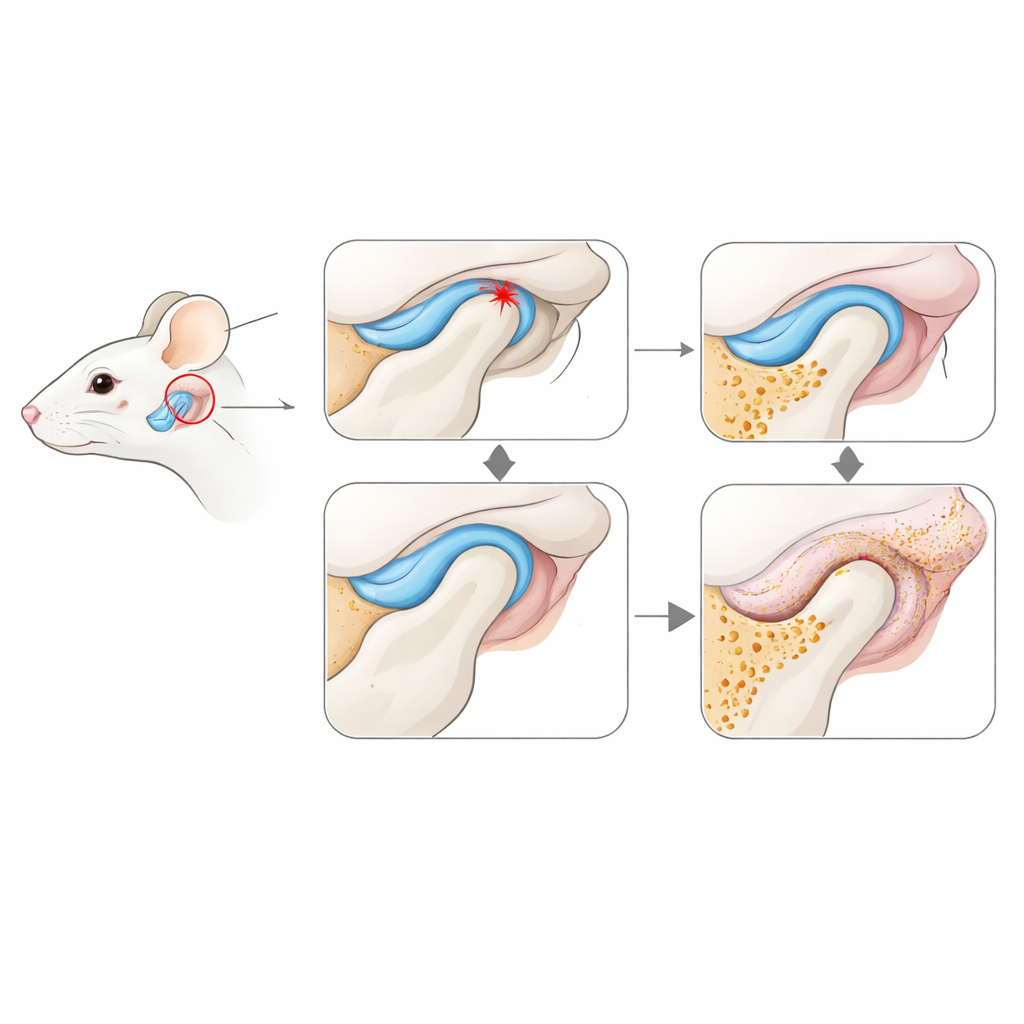
أضرار مبكرة في العظم والغضروف وبطانة المفصل
أظهرت المفاصل المضغوطة والمزاحة للقرص سريعًا علامات مميزة لبداية التهاب المفاصل التنكسي. فقد رأس العظم في الفك كثافته المعدنية وظهرت به حفر ونموات عظمية إضافية وزيادة في الخلايا الناهة للعظم، مما يشير إلى أن الإطار الداخلي للمفصل يخضع لإعادة تشكيل سريع جدًا. بدأ الغضروف الذي يوفر عادة سطحًا أملسًا بالترقق والتشقق وفقدان الجزيئات الحامية، لا سيما في نموذج انزياح القرص. في الوقت نفسه، ازداد سمك الغشاء الزليلي — النسيج الرقيق والناعم الذي يغذي المفصل — وتمتلئ بالخلايا وأصبحت في بعض المناطق دهنية أو ليفية. تشير هذه التغيرات البنيوية إلى أن بطانة المفصل ليست مجرد متفرج سلبي بل لاعب أساسي في بدء تنكس المفصل.
قراءة إشارات المفصل الجزيئية خلية خلية
للتجاوز عن التشريح ورؤية ما تفعله الخلايا الفردية، فحص الفريق أي الجينات كانت مفعلة عبر آلاف الخلايا باستخدام تسلسل الحمض النووي الريبوزي الكلي، وتسلسل الحمض النووي الريبوزي للخلايا المفردة، والنَّسخانية المكانية عالية الدقة. أَتَاحَت هذه الطرق تحديد متى وأين غيرت الأنواع الخلوية المختلفة سلوكها. في نهاية العظم بالمفصل، انخفض تعبير الجينات التي عادةً تحافظ على صحة الغضروف، بينما ارتفع تعبير الجينات المرتبطة بتفكك الأنسجة ونشاط الخلايا الناهِمة للعظم، لا سيما في نموذج انزياح القرص. في الغشاء الزليلي، زادت الخلايا إنتاجها للرسل الالتهابية وإنزيمات هاضمة للنسج وجزيئات مرتبطة بالتندب والتليف. كانت بقعة مهمة بشكل خاص هي الجزء الخلفي (الذيلي) من بطانة القرص، حيث تلاقت مبكرًا الالتهاب وتراكم الدهون والسماكة الليفية.
التواصل الخلوي وخريطة جديدة لمفصل الفك
من خلال تحليل نشاط الجينات خلية خلية وإعادة ربط تلك الخلايا بمواقعها الدقيقة في النسيج، حدد المؤلفون أحياء مميزة من الأرومات الليفية (خلايا داعمة)، والخلايا المناعية، والخلايا المكوِّنة للأوعية الدموية داخل الغشاء الزليلي. بدا أن هذه الأنواع الخلوية تتواصل مع بعضها عبر مسارات إشارية تستجيب للشد الميكانيكي والالتهاب. على سبيل المثال، كانت إشارات مسار Notch — المعروفة بتنظيم الأوعية الدموية وإعادة تشكيل النسيج — نشطة بشكل خاص في الخلايا البطانية (بانية بطانة الأوعية) في المفاصل المتضررة، على الأرجح بتأثير من الأرومات الليفية المجاورة. أظهرت المناطق نفسها أيضًا مستويات عالية من الإنزيمات التي تهضم الغضروف وعلامات التليف، مما يعزز فكرة أن الخلايا الزليلية المتضررة يمكن أن تدفع فقدان الغضروف والألم. 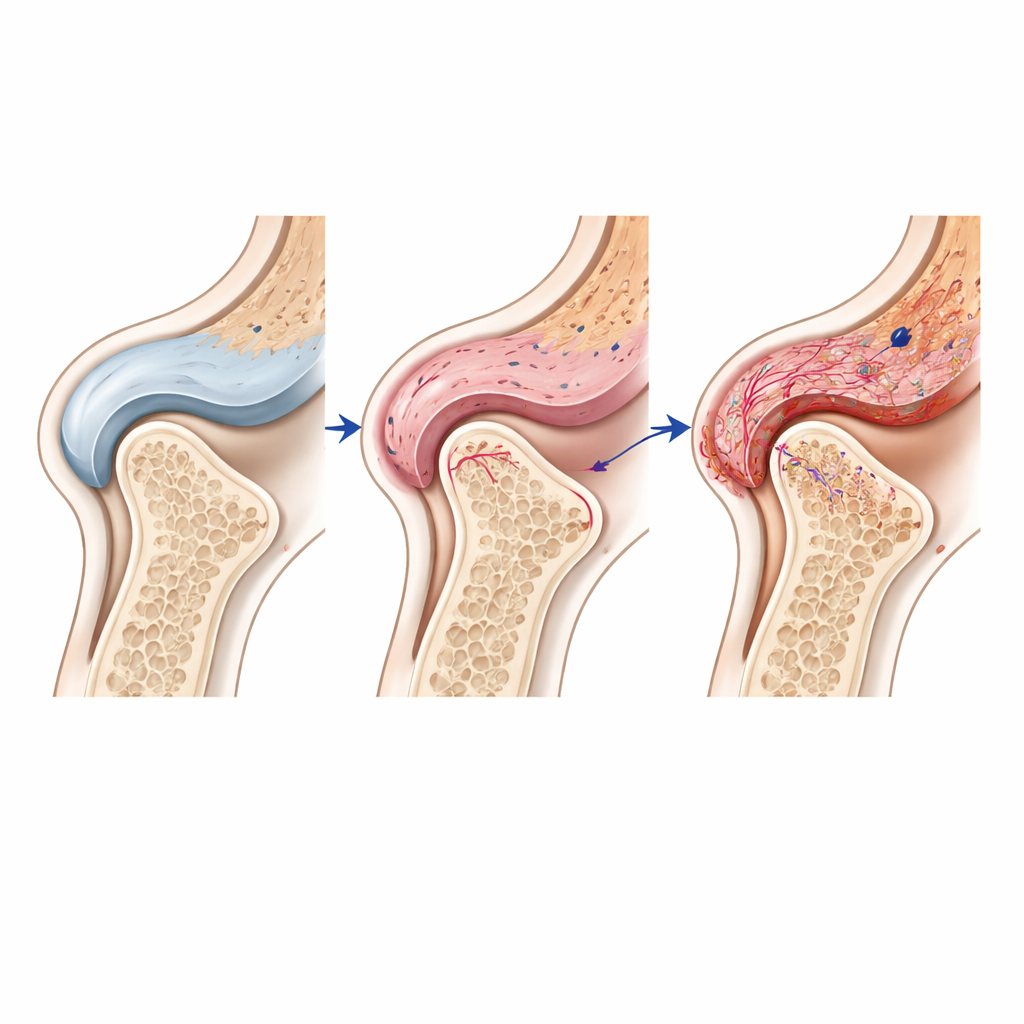
كيف قد تؤثر هذه الدراسة على العلاجات المستقبلية
بدلًا من اختبار دواء محدد، تقدم هذه الدراسة أطلسًا مفصلًا لكيفية استجابة بطانة المفصل والغضروف في TMJ للقوى الضارة في بداية المرض. تُظهر أن التهاب مفصل الفك التنكسي المبكر يتميز بتغيرات منسقة في العظم والغضروف وخلايا الغشاء الزليلي على وجه الخصوص، التي تصبح التهابية وليفية بينما ترسل إشارات ضارة إلى داخل المفصل. من خلال ربط هذه التغيرات بأنواع خلوية ومواقع دقيقة، يبرز العمل أهداف علاجية محتملة جديدة — مثل المسارات المشاركة في إشارة Notch، وإشارة الكيموكينات، والإنزيمات المحللة للمصفوفة — التي قد تُمنع قبل أن يصبح تلف المفصل لا عودة فيه. باختصار، توفر الورقة مخططًا قويًا لفهم وقطع سلسلة الأحداث التي تحول حركات الفك اليومية إلى ألم TMJ المزمن.
الاستشهاد: Shibusaka, K., Negishi, S., Terashima, A. et al. Defining subcellular synovial responses in TMJ osteoarthritis onset via mechanical stress and articular disk derangement models. Int J Oral Sci 18, 28 (2026). https://doi.org/10.1038/s41368-025-00411-6
الكلمات المفتاحية: المفصل الصدغي الفكي, التهاب المفاصل التنكسي, الغشاء الزليلي, الإجهاد الميكانيكي, التعبير الجيني للخلايا المفردة