Clear Sky Science · ar
رؤى مرضية من فسيفساء الخلايا الجسدية في الدماغ
بقع خفية في الدماغ
يحمل كل دماغ لوحة فسيفسائية سرية. على الرغم من أننا نميل إلى الاعتقاد بأن خلايانا تشترك في نفس المادة الوراثية، فإن تغييرات جينية طفيفة تتراكم بهدوء في خلايا الدماغ الفردية على مدى الحياة. تشرح هذه المراجعة كيف يمكن لتلك اللوحة الجينية — المسماة الفسيفساء الخلوية في الدماغ — أن تساعد العلماء على تتبع كيفية بناء الدماغ، وكيف يشيخ، ولماذا يُصاب بعض الأشخاص بحالات مثل الصرع أو التوحد أو الفصام أو مرض ألزهايمر. قد تشير فهم هذه الفسيفساء الخفية إلى طرق للتشخيص المبكر وعلاجات جديدة أكثر استهدافاً.
كيف يصبح الدماغ فسيفساء جينية
تعني الفسيفساء الجسدية أن ليست كل خلايا الجسم تحمل نفس الجينوم تمامًا. مع انقسام الخلايا، تنشأ طفرات عشوائية وتنتقل إلى السلالات اللاحقة منها، مكوِّنة جيوبًا من الخلايا ذات التغييرات المشتركة. في الدماغ، من المحتمل أن معظم هذه الطفرات ليس لها تأثير واضح على سلوك الخلايا، لكنها تعمل كـ "رموز شريطية" طبيعية تسجل متى وأين وُلدت الخلايا. وبما أن خلايا الدماغ ثابتة إلى حد كبير ونادراً ما تُستبدل، فإن نمط الطفرات الناتج يحفظ سجلاً أحفورياً للتطور والشيخوخة. من خلال مقارنة الأماكن التي تظهر فيها هذه المتغيرات، يستطيع الباحثون إعادة بناء المسارات التي اتخذتها الخلايا الدماغية المبكرة، كاشفين كيف تتفرع المناطق والخلايا المختلفة من مجموعة صغيرة من الخلايا المؤسِّسة.
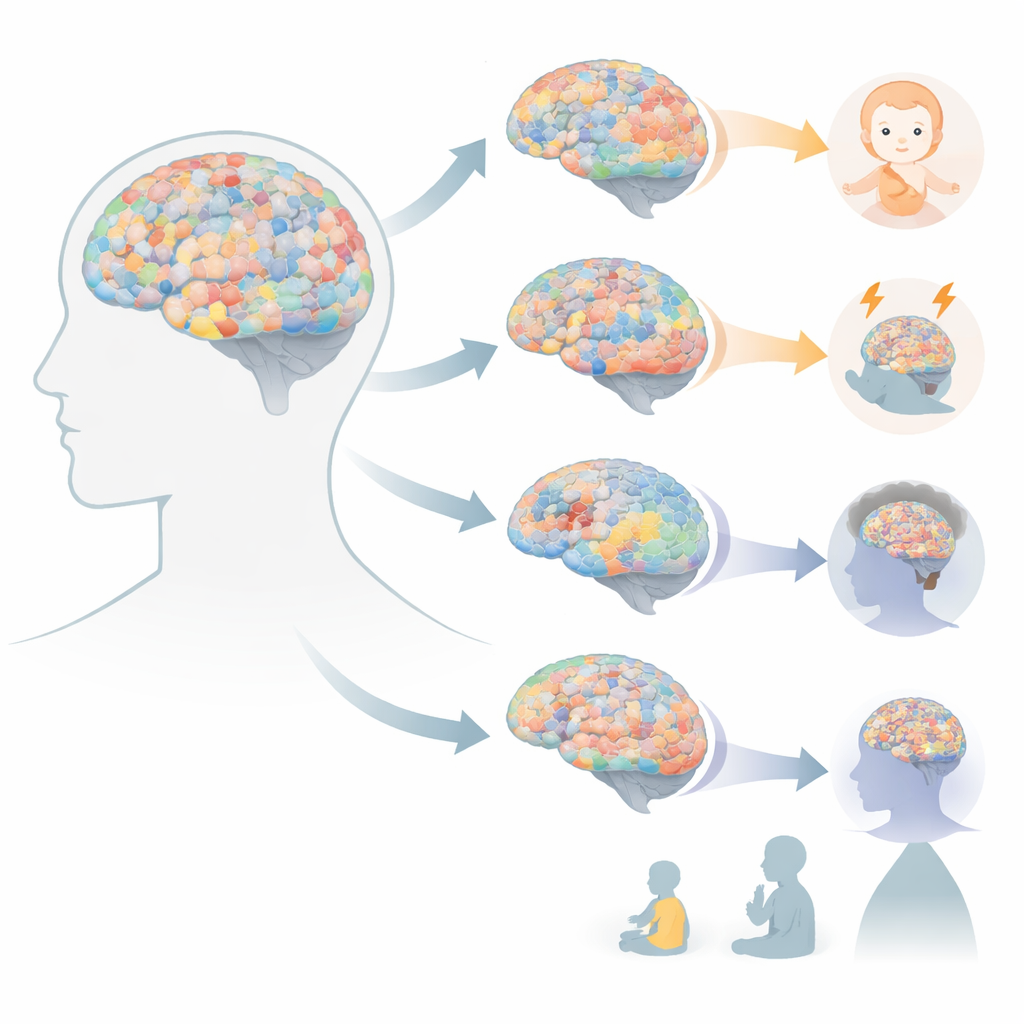
التغيرات عبر العمر في الخلايا العصبية وخلايا الدعم
تُظهر المراجعة أن خلايا الدماغ تكتسب طفرات في مراحل ومعدلات مختلفة. خلال التطور المبكر، تحصل الخلايا السلف العصبية المنقسمة على مئات التغيرات الصغيرة في الحمض النووي، متبعة أنماطًا كيميائية مميزة مقارنةً بالانقسامات الأولى بعد الإخصاب. بعد أن تترك الخلايا العصبية دورة الخلية وتصبح ثابتة، تواصل تراكم عدد متواضع من الطفرات الجديدة سنويًا، بحيث قد يحمل خلية عصبية لشخص مسن أكثر من ألف تغير من هذا النوع. ترتبط أنماط الشيخوخة هذه بعمليات روتينية مثل إصلاح الحمض النووي والنسخ، لكن يمكن أن تتكثف بفعل الإجهاد التأكسدي، لا سيما في الأمراض التنكسية العصبية. تظهر خلايا الدبق، ولا سيما الخلايا قليلة التغصن التي تعزل الألياف العصبية، توقيعات طفرة مميزة لها وغالبًا تكتسب طفرات بسرعة أكبر من الخلايا العصبية، مما يوحي بأن دورة حياتها وبيئتها تشكّلان كيفية تراكم تلف الحمض النووي.
ماذا تكشف الفسيفساء عن اضطرابات الدماغ
لأن الطفرات الفسيفسائية يمكن أن تغير فقط مجموعة فرعية من الخلايا في منطقة دماغية محددة، فإنها تتناسب طبيعيًا مع الاضطرابات البؤرية. في الصرعات البؤرية، تحوي العديد من الآفات المستأصلة جراحيًا طفرات ممرضة لا تُرى في دم المريض. غالبًا ما تؤثر هذه الطفرات على مسارات النمو والإشارة، مثل نظام mTOR، وتكون مركزة في أنواع خلايا غير طبيعية داخل الآفة. من المدهش أن بعض أنماط الفسيفساء تنشأ عندما يتم تصحيح خلل كروموسومي ضار كان موجودًا قبل الإخصاب جزئيًا في بعض الخلايا الدماغية المبكرة، مما يترك مزيجًا من خلايا مُصحَّحة وغير مُصحَّحة. رُبطت المتغيرات الفسيفسائية أيضًا بالتوحد، حيث تظهر التغيرات المدمرة في جينات نشطة قبل الولادة، أو في مفاتيح تنظيمية رئيسية، بتواتر أكبر لدى الأفراد المتأثرين. بالنسبة للفصام وحالات نفسية أخرى، تظهر أدلة تشير إلى أن بعض الكسب أو الفقدان الكبير للحمض النووي المرتبط بالدماغ قد يحدث جسديًا ويزيد المخاطر، رغم أن الكثير لا يزال غير مؤكد.
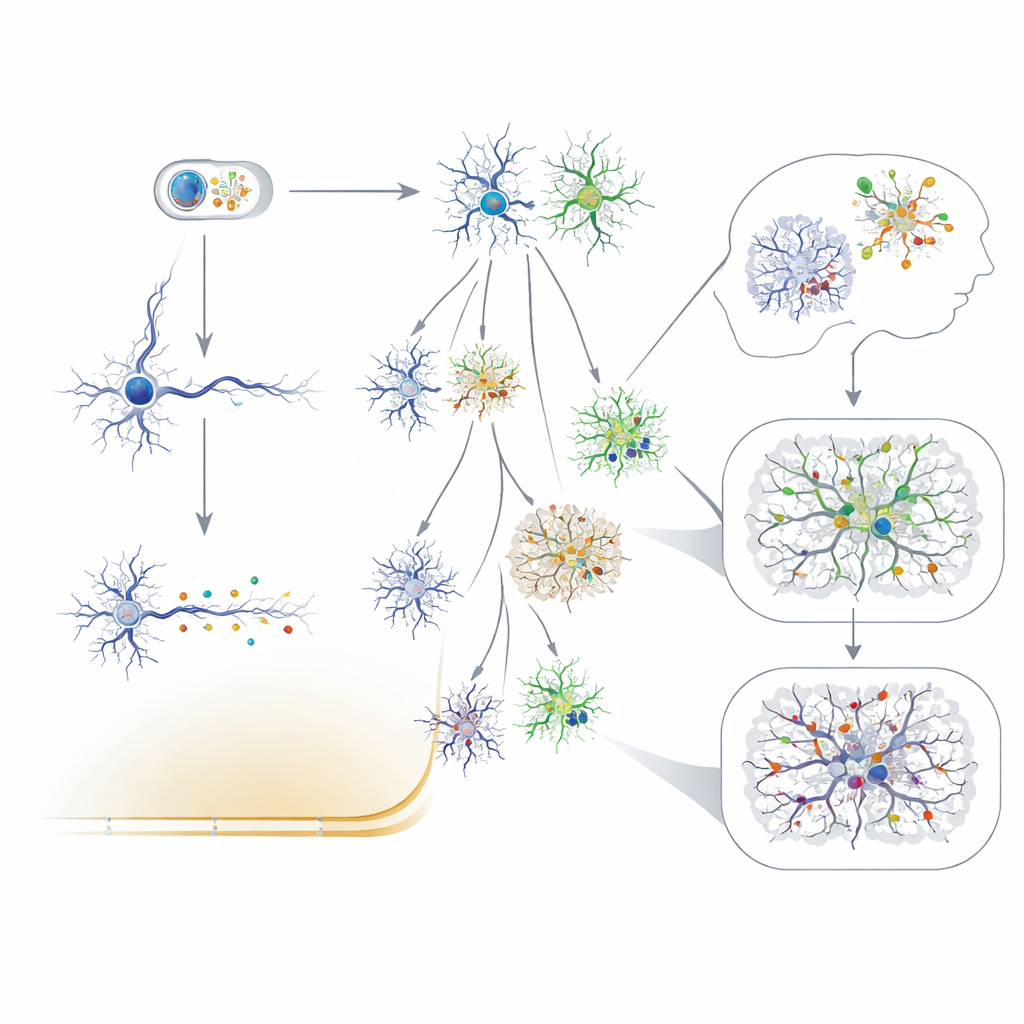
قراءة النسب وكشف التغيرات الطفيفة
تتيح التقنيات الجديدة الآن للعلماء قراءة هذه الفسيفساءات الدقيقة بتفصيل غير مسبوق. يمكن للتسلسل العميق لكامل الجينوم، وتسلسل الجينوم والـRNA لخلايا مفردة، والأساليب التي تعزل أنواع خلايا محددة اكتشاف متغيرات نادرة جدًا وقياس عدد الخلايا الحاملة لها. من خلال معاملة الطفرات المحايدة كرموز شريطية، استخدم الباحثون هذه الطفرات لتأريخ توقيت انفصال المناطق الدماغية الرئيسية، ولإظهار أن القشرة البشرية مقسمة بشكل أكثر وضوحًا من اليسار إلى اليمين مقارنةً من الأمام إلى الخلف، ولإثبات أن بعض الخلايا العصبية المثيرة والمثبطة تنشأ من سلفيات محلية مشتركة. سريريًا، بدأ التسلسل فائق الحساسية من عينات جراحية أو من السائل الشوكي أو حتى من مادة جمعت على أقطاب عمق أن يكشف عن طفرات منخفضة المستوى قد تفسر حالات صرع غامضة بخلاف ذلك.
لماذا تهم هذه الفسيفساء لصحة الدماغ
تجمعًا، تجادل الأعمال التي استعرضت هنا بأن الفسيفساء الجسدية في الدماغ ليست شذوذاً نادراً بل سمة طبيعية لبيولوجيا الدماغ يمكن أن، في بعض الظروف، تدفع الخلايا نحو المرض. قد تُعطّل نفس الطفرات العشوائية التي تسجل بهدوء تاريخ تطورنا أحيانًا جينات أو مسارات حرجة عندما تنشأ في المكان أو الوقت الخطأ. ومع تحسن طرق الكشف عن اختلافات الحمض النووي الدقيقة ودمجها مع خرائط مفصلة لأنواع الخلايا والتنظيم المكاني، يأمل الباحثون في الانتقال من وصف هذه الفسيفساء إلى فهم أيها فعلاً ذي أهمية. قد يساعد هذا الفهم على تفسير لماذا قد يكون لدى شخصين يحملان حمضًا وراثيًا موروثًا مشابهًا نتائج دماغية مختلفة تمامًا، وفي نهاية المطاف توجيه علاجات دقيقة تستهدف مجموعات الخلايا المحددة التي تقيم فيها الطفرات الضارة.
الاستشهاد: Chung, C., Nedunuri, R. & Gleeson, J.G. Disease insights from brain somatic mosaicism. Exp Mol Med 58, 953–960 (2026). https://doi.org/10.1038/s12276-024-01331-x
الكلمات المفتاحية: فسيفساء الدماغ, الطفرات الجسدية, التطور العصبي, الصرع, التنكس العصبي