Clear Sky Science · zh
基于卷积神经网络的光学相干断层成像内镜用于经皮肾造瘘引导
为何更安全的肾脏通路至关重要
肾结石疾病日益常见,许多患者需要在肾脏内直接放置一根小管以引流尿液或取出结石。这个过程称为经皮肾造瘘,通过从患者背部引导针头进入肾脏的空腔中心完成。尽管穿刺很小,但选错路径可能撕裂脆弱的肾组织或损伤血管,导致出血和其他并发症。本研究介绍了一种新的高分辨率成像探头,结合人工智能,安装在针尖内部,帮助医生精确看到前方位置并避免伤害。
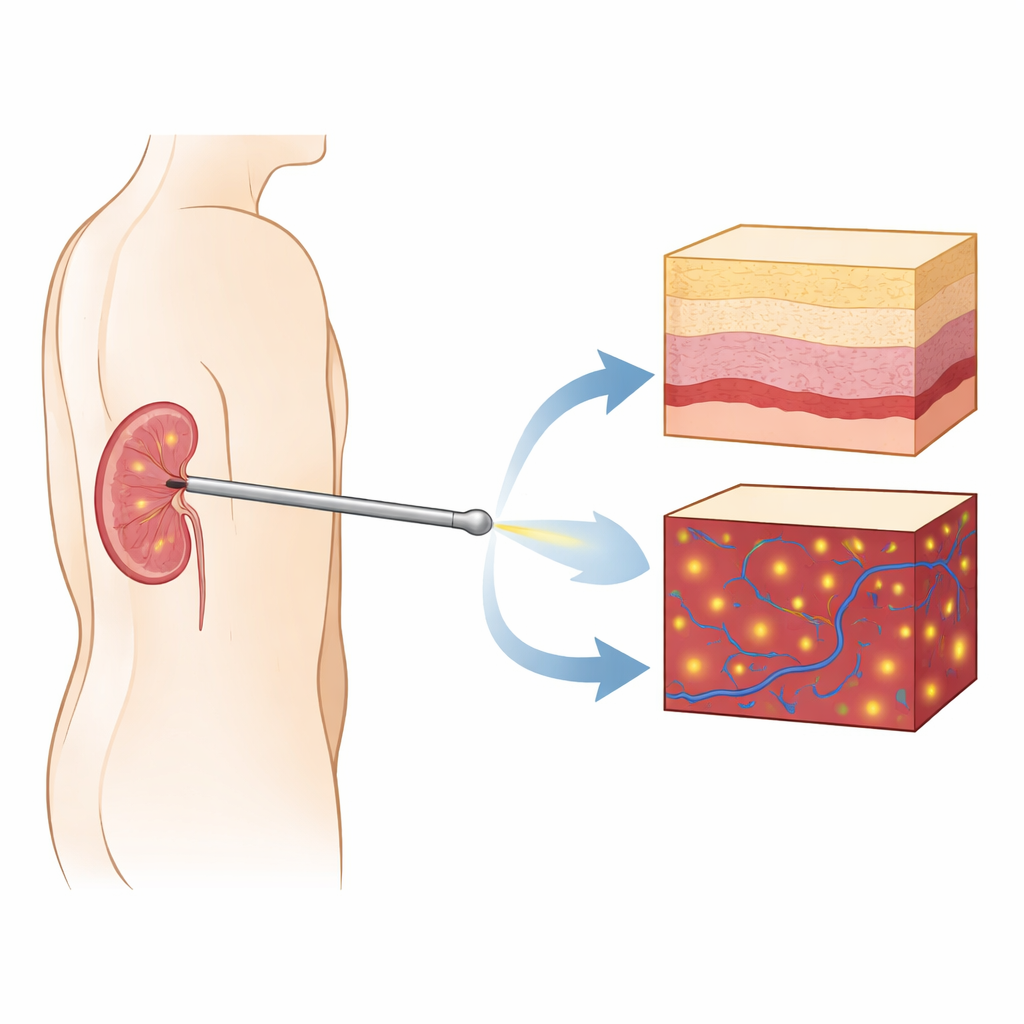
针内的微型相机
研究人员构建了一个前视成像探头,基于光学相干断层成像(OCT)——一种基于光的成像方法,可在微米级分辨率下捕获组织的横截面“切片”,约为常规医学超声的十倍精细。他们在标准的肾造瘘针内嵌入了一枚薄的梯度折射率透镜,使探头在插入时能直接向前观察肾脏。不同于主要显示表面视图的常规内镜,该系统提供了具有深度分辨的图像,显示针尖下方组织结构如何变化。同一探头还可切换到多普勒模式,突出显示流动的红细胞,从而在针刺入之前揭示前方的血管。
实时识别肾脏层次
为测试系统是否能区分不同的肾脏组织,研究团队在31例保持近似正常条件的人体捐献肾脏上进行了实验。在真实手术中,针头应穿过外层皮质和内层髓质,然后进入称为肾盏的杯状结构,最终到达中央的集尿池。偏离路径可能穿过结构间的脂肪间隙并撕裂薄壁。研究者系统性地让探头接触五种组织类型——皮质、髓质、肾盏、窦周脂肪和肾盂,并捕获了数百万张显示其独特模式的OCT图像。例如,皮质与髓质看起来都较为平滑但在深度上有差异,肾盏显示条纹状过渡,窦周脂肪产生明亮的斑点网络,而肾盂则在探头下方呈现为空腔空间。
教会智能系统识别危险
由于人类专家在手术过程中需要时间和训练来解读这些新图像,团队转向深度学习。他们训练了若干卷积神经网络来将每帧OCT图像分类为五种组织类型之一,并最终选定名为Inception的架构作为表现最佳者。在内部测试中,该模型对组织的识别准确率约为99.6%,并在其从未见过的其他肾脏样本上保持高性能。在另一项任务中,他们采用了另一种神经网络设计nnU‑Net,对多普勒OCT图像中的血管进行轮廓分割。该模型学会将流动血液与背景组织区分开,与专家手工标注具有很高的一致性,甚至可以识别宽度小于0.2毫米的微小血管,这些血管用常规工具难以看到。
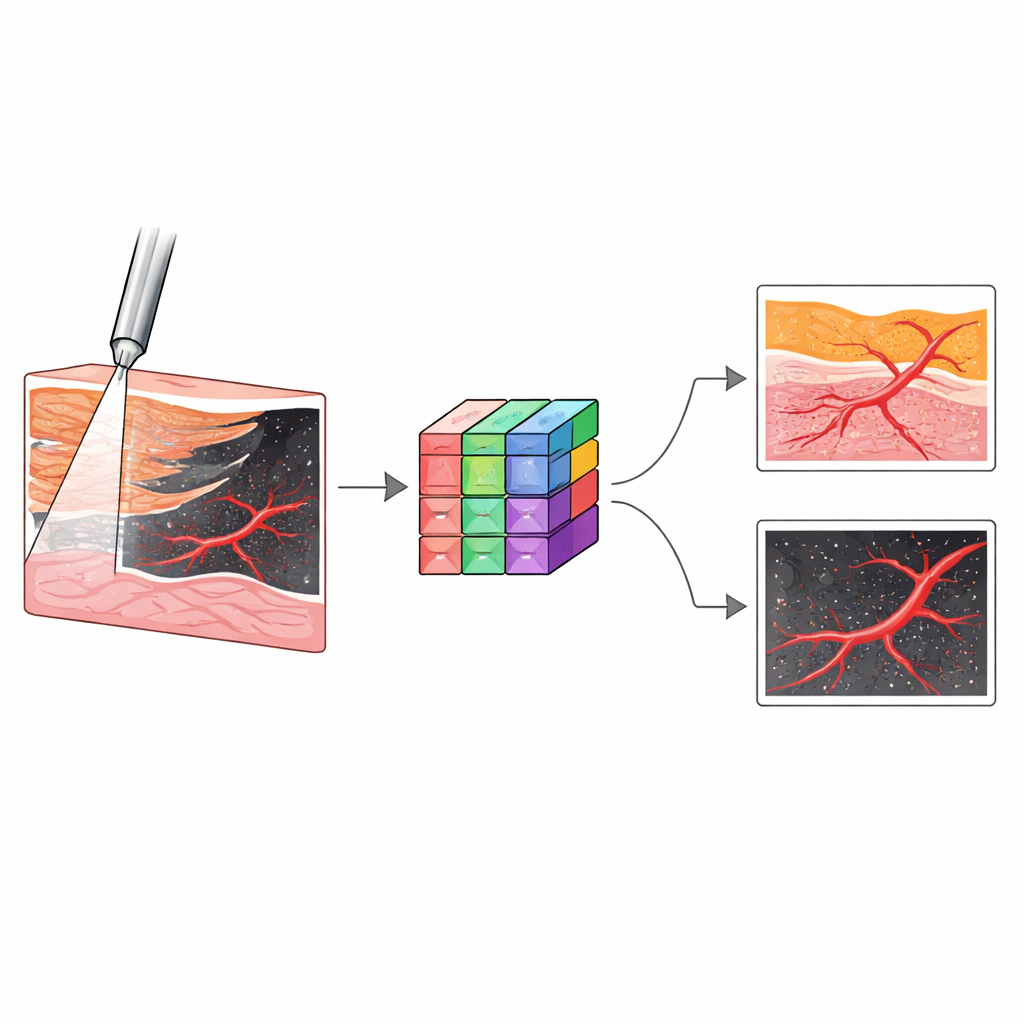
与现有工具的比较
目前,医生通常依赖超声或基于X射线的透视成像来引导肾造瘘针。这些技术能显示肾脏的大致位置和针的总体路径,但其相对粗糙的分辨率使得很难确切判断针尖处是哪种组织或血管距离有多近。在对照实验中,经验丰富的放射科医师即使用结构和多普勒超声也难以识别针尖处的精确组织,且无法可靠地可视化极小的血管。相比之下,OCT系统提供了详细的局部视图,并配有可在现代图形处理器上在几分之一秒内运行的自动分析,足够快以在针推进时提供反馈。
这对患者意味着什么
研究表明,将针内安装的OCT探头与深度学习结合,可能使肾脏通路操作更安全、更高效。未来,医生可在常规针内置入该探头,实时观看细尺度图像,并依靠软件在针尖进入正确腔室或接近血管时发出信号。减少穿刺尝试次数将意味着更少的组织创伤、更低的出血风险,以及可能更短的手术时间和住院时间。尽管该工作是在捐献的肾脏上完成而非在活体患者身上,但它为临床系统奠定了基础,这些系统也可能用于指导其他针式介入操作,从活检和麻醉阻滞到靶向药物输送。
引用: Wang, C., Calle, P., Yan, F. et al. Percutaneous nephrostomy guidance by a convolutional-neural-network-based optical coherence tomography endoscope. Commun Eng 5, 47 (2026). https://doi.org/10.1038/s44172-026-00613-8
关键词: 肾结石手术, 针头引导, 光学相干断层成像, 医学影像人工智能, 血管检测