Clear Sky Science · zh
使用人工智能从整片血液学切片图像定量微核,作为可转化的DNA损伤反应抑制剂药效学生物标志物
为什么血液中的微小斑点能讲述重要信息
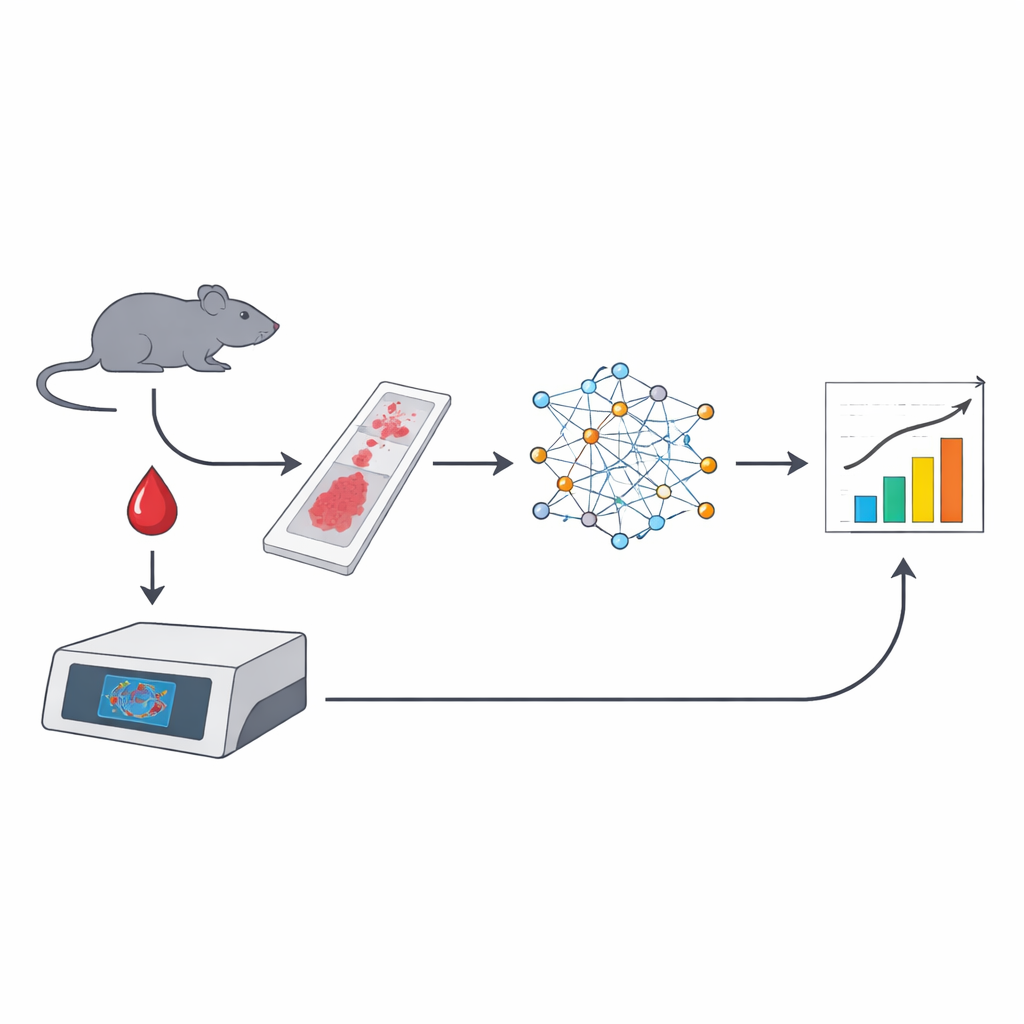
医生和科学家始终在寻找简单的方法来判断一种抗癌药物在体内是否发挥了预期作用。这项研究表明,存在于红细胞内的小斑点,称为微核,可以充当某些抗癌治疗所致DNA损伤的天然指示物。通过将显微镜式的整片扫描图像与人工智能(AI)相结合,研究人员把几滴血变成了关于DNA靶向药物作用强度的丰富、自动化读数。
红细胞中的小片DNA岛
微核是与细胞主核分离的微小DNA囊泡。它们在染色体断裂或细胞分裂时染色体分离错误时形成,这类事件在癌症以及暴露于DNA损伤剂后很常见。在大多数组织中,显微镜下识别真实的微核很有挑战性,因为薄切片容易产生假象。红细胞提供了一种解决办法:在成熟过程中,红细胞通常会排出其主核,但此前形成的任何微核可以作为微小且轮廓清晰的斑点遗留在细胞内。这些历史上称为Howell–Jolly小体的已知结构,因而成为便利且真实的微核,循环于血流中,能揭示近期发生的DNA损伤程度。
用AI将血涂片转化为数据
团队构建了一个自动化管线,起始于小鼠的标准血涂片,染色方式包括荧光DNA染料或医院实验室常用的May–Grünwald Giemsa染色。整片切片以高分辨率扫描,并训练有监督的深度学习模型来识别红细胞、挑出微核,以及根据细微的尺寸和颜色差异将未成熟的网织红细胞与成熟红细胞区分开来。单幅图像中,该系统可分析超过10万个细胞,标记携带微核的细胞,甚至计数包含多个微核的细胞——这是传统流式细胞术难以做到的。
将血中微小变化与药物强度联系起来
研究人员接着探问,红细胞中微核阳性细胞的频率是否随对DNA造成损伤的化疗以及阻断DNA损伤反应的药物(如PARP抑制剂)的暴露而变化。在接受顺铂或紫杉醇处理的小鼠中,基于AI的计数捕捉到了微核细胞预期的增加。在携带肿瘤的小鼠接受奥拉帕利或saruparib等PARP抑制剂治疗时,较高剂量导致携带微核细胞的增加更多,并伴随更强的肿瘤缩小。在数周的每日给药过程中,小量的连续血样(每次仅约5微升)使团队得以追踪微核如何逐渐累积并在停止治疗后下降。将其基于切片的方法与标准流式细胞术比较时,二者高度一致,表明这一新流程既准确又稳健。
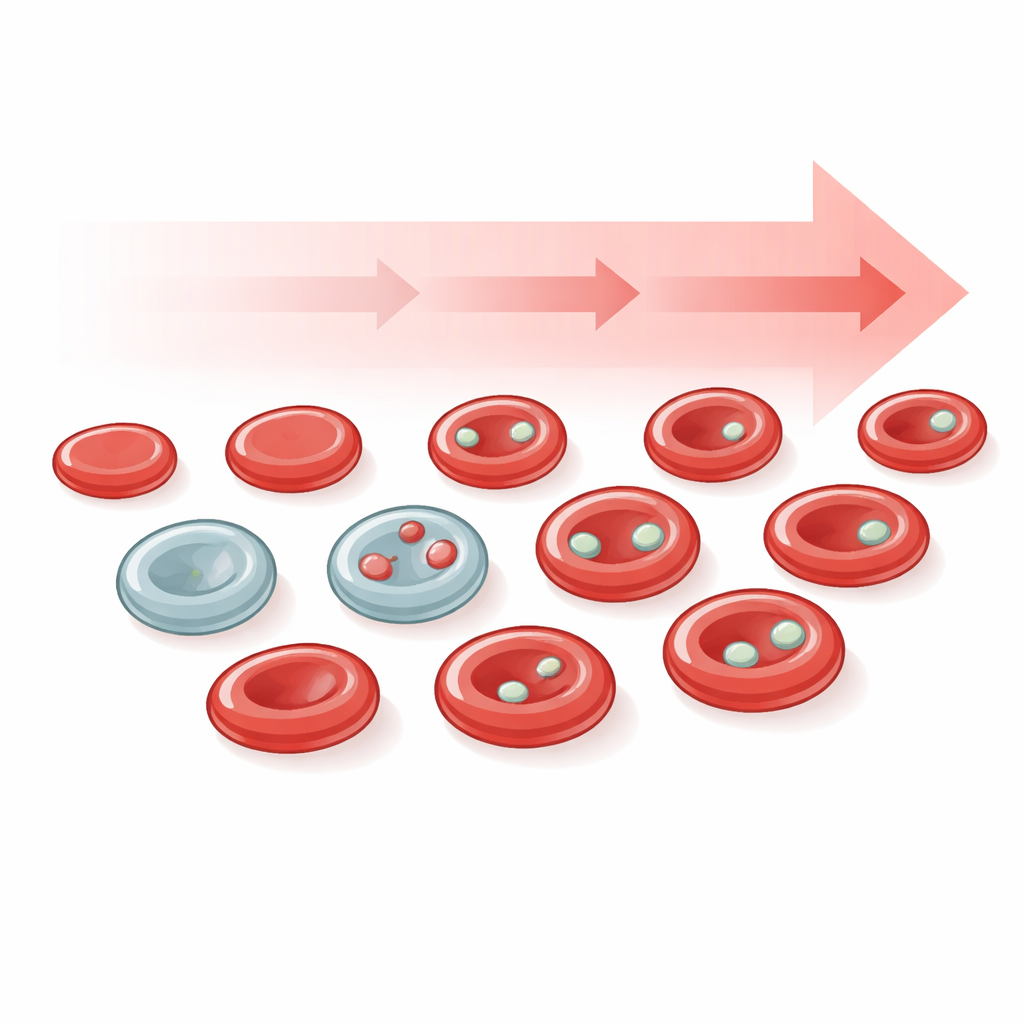
聚焦年轻红细胞以获得更清晰的信号
由于年轻红细胞(网织红细胞)尤其容易含有新近形成的微核,研究者训练其算法在常规染色切片上将红细胞群体分为未成熟和成熟细胞。该细化分析显示,微核在网织红细胞中远为富集且动态性更强,相较于年老细胞提供了更敏感且变化更快的药物作用信号。整片图像还使得可对样本质量本身进行监控——例如检测因保存不当而变形的红细胞——以便在分析前标记不合格切片,这对未来临床应用是重要的一步。
这对未来癌症护理可能意味着什么
该研究表明,一小份血样、一次标准染片和一个AI驱动的成像管线可以共同提供一种可扩展、创伤性小的指标,用以衡量DNA靶向药物在体内的作用强度。尽管这项工作是在小鼠中完成,且红细胞只能作为肿瘤内部情况的替代指标,微核信号与肿瘤反应之间的强关联表明,这一方法有望成为药物开发中乃至最终临床试验中的实用工具。简单来说,计数血液中这些微小的DNA“点”可能帮助研究者和临床医师调整剂量、比较新药并随时间跟踪治疗效果——而无需反复进行侵入性活检。
引用: Yong, K.H.R., Robak, W.S., Mulderrig, L. et al. Micronucleus quantification from whole-slide haematology images using AI serves as a translatable pharmacodynamic biomarker for DNA damage response inhibitors. Sci Rep 16, 11437 (2026). https://doi.org/10.1038/s41598-026-41458-7
关键词: 微核, 红细胞, PARP 抑制剂, 数字病理学, DNA 损伤反应