Clear Sky Science · zh
富含7SK的外泌体抑制人肺癌细胞的癌性表型:来自2D与微流控3D体外模型的见解
体内微小信使为何重要
肺癌仍然是全球致死率最高的癌症之一,部分原因在于肿瘤常对现有药物产生耐药并向新组织转移。本研究探讨了一种出人意料的盟友:细胞天然释放的微观囊泡——外泌体,内含一种名为7SK的特殊RNA分子。通过利用这些天然信使将7SK递送到体外培养的肺癌细胞,研究者提出了一个简单但强有力的问题:我们能否重新编程癌细胞,使其增速放缓、停止扩散并走向凋亡,同时尽量不严重损伤健康细胞?
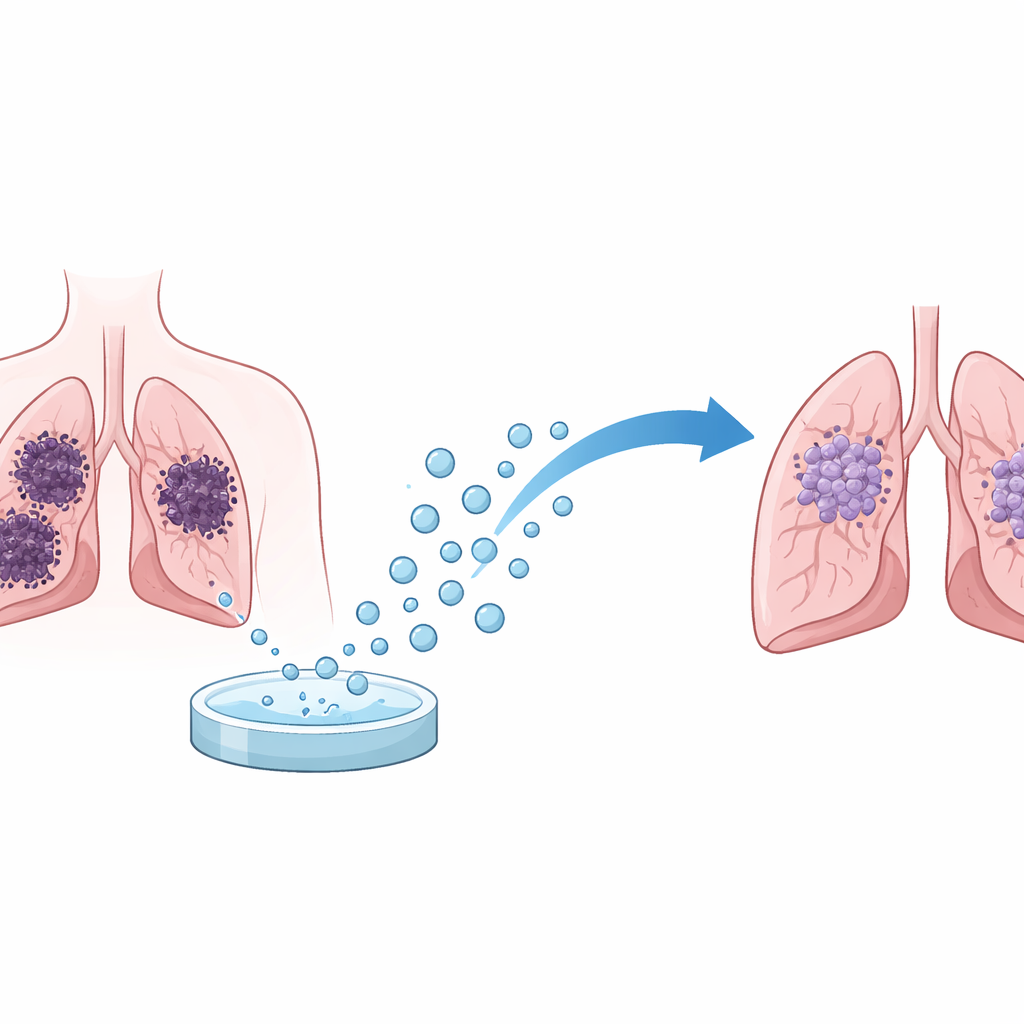
一种具有沉默作用的天然信息
每个细胞通过读取基因来决定何时生长、分裂或保持静止。7SK是一种不编码蛋白的长链RNA,它通过调控其他基因的开关来发挥作用。早期研究提示,7SK水平下降时,某些肿瘤会变得更具侵袭性。本研究聚焦于非小细胞肺癌——最常见的肺癌类型,检验提升7SK是否能将肿瘤细胞朝相反方向推移。研究团队并未通过病毒或DNA构建体强制细胞持续过表达7SK,而是选择了一条更类似体内通讯方式的路径:将实验室合成的7SK装入来自脐带衍生干细胞的外泌体,然后将这些“富含7SK”的外泌体喂给肺癌细胞。
携带强效货物的微小囊泡
研究者首先确认了干细胞来源的外泌体在形态和行为上符合预期:它们是具有完整膜结构且尺寸分布窄的小而圆的颗粒。通过荧光染料示踪,他们在平面(2D)培养皿和更真实的嵌入胶原凝胶并置于微流控装置中的三维(3D)微型肿瘤中,都观察到肺癌细胞能够有效吞噬这些标记的外泌体。当外泌体被装载7SK后,癌细胞内的7SK含量明显上升,证明这种天然运输系统成功递送了货物。
在平面培养中减缓生长与迁移
一旦癌细胞摄取富含7SK的外泌体,其行为在几个重要方面发生变化。细胞的生存与增殖能力在数小时到数日内下降,这一点通过常规活力测定和直接计数得到证实。程序性细胞死亡的标志增加,包括关键酶的激活以及促死与促存活基因之间平衡的转变。与此同时,细胞的迁移与侵袭能力降低。在伤口愈合和经膜小室(transwell)实验中,处理过的细胞在爬入空隙或穿越障碍物时更为迟缓,基因活性也从与松散、易迁移和侵袭相关的状态,转向更为粘附、迁移性较低的状态。
在3D中检验肿瘤行为
鉴于真实肿瘤以三维簇状生长而非平面片状,团队使用球状体(spheroids)——由肺癌细胞组成的紧凑球体,并将其置于模拟体内环境的微流控芯片中。当暴露于装载7SK的外泌体时,这些球状体体积保持较小,向周围凝胶的扩散减少,且死细胞比例高于未处理或接受空载外泌体的球体。换言之,在更接近嵌入肺组织的早期肿瘤环境中,7SK货物仍能抑制生长并减弱转移的前奏行为。
这对未来肺癌治疗可能意味着什么
总体而言,实验表明通过外泌体将额外的7SK送入肺癌细胞,可以降低一些关键的癌症特性——失控的生长、生存能力和侵袭性扩散——同时在所测的早期时间点对正常肺细胞影响较小。该工作仍处于早期、仅限于实验室的阶段,作者强调需要在更多细胞类型和动物模型中进行更详尽的研究,以阐明7SK在肺肿瘤中的具体作用机制及此类疗法的安全性。不过,这些发现指向一种有趣的未来策略:利用体内自身的纳米级信使来递送调控性RNA,以温和地推动癌细胞远离恶性表型,而不是用广谱高毒性的药物去猛攻肿瘤。
引用: Aghamiri, S., Ajoudanian, M., Farhadi, S. et al. 7SK-enriched exosomes suppress the cancer phenotypes in human lung cancer cells: insights from 2D and microfluidic 3D in vitro models. Sci Rep 16, 10789 (2026). https://doi.org/10.1038/s41598-026-40761-7
关键词: 肺癌, 外泌体, 长链非编码RNA, RNA疗法, 微流控肿瘤模型