Clear Sky Science · zh
中性粒细胞稳态紊乱与危重新冠患者线粒体功能改变相关
这对新冠患者为何重要
大多数人现在知道新冠不只是肺部感染,但病毒如何将机体自身防御变为伤害因素仍在被揭示中。本研究聚焦重症监护室中危重的新冠患者的中性粒细胞——一种常见的白细胞类型。通过检查这些细胞的生存、死亡以及它们内部“小发电站”(线粒体)的使用方式,研究者揭示出一种持久且过度活跃的中性粒细胞模式,这或能解释重症病例中持续的炎症、血液损伤和器官损害。
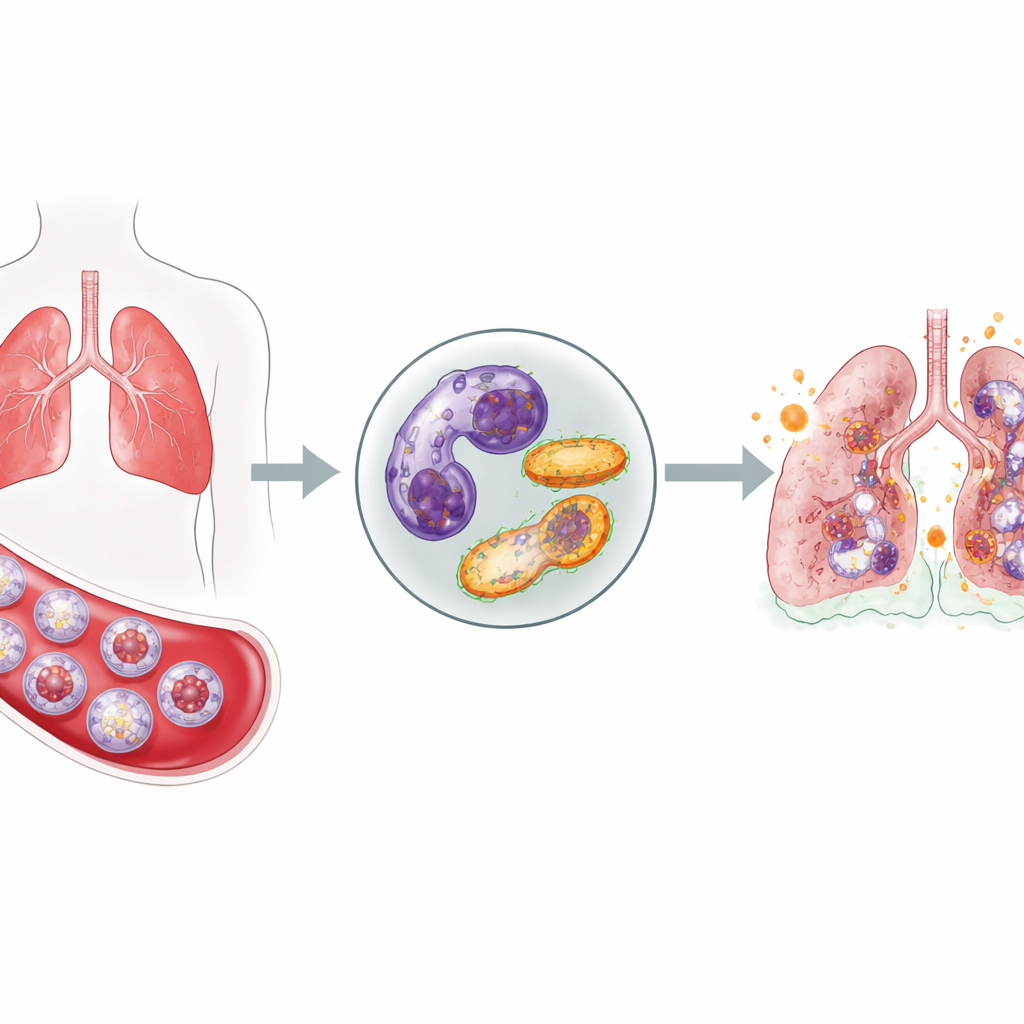
不肯收兵的一线细胞
中性粒细胞是机体对感染的首批应答者:它们迅速进入血流,迁移到组织,并释放有毒分子以杀死入侵微生物。通常在完成任务后,它们会安静地自我毁灭并被清除,以防伤害健康组织。在危重的新冠患者中,研究团队观察到了截然不同的情形。与健康志愿者相比,这些患者血中中性粒细胞激增,且重要的是,其中许多是被骨髓仓促释放的未成熟细胞。与此同时,多项检测显示,进入正常程序性死亡的中性粒细胞减少,表明这些攻击性细胞比应有的时间更久地滞留体内。
微妙的遗传信号但明确的存活模式
研究者还在重症监护生存者与死亡者的中性粒细胞中检测了微小调控分子microRNA。这些分子中有些在纸面上指向了控制细胞死亡和钙稳态的通路受扰。然而,当他们测量直接的细胞死亡标志时,未见生存者与非生存者之间存在显著差异——两组与健康人相比都表现出类似的中性粒细胞自我毁灭减少。这意味着microRNA的模式更像是未来研究的线索,而非能预测生死的确定性指标,并强调中性粒细胞总体上未能关闭是重症新冠的一个共同特征。
钙位移与过度充能的“发电站”
为了解中性粒细胞为何未按时死亡,团队聚焦于细胞内两个密切相关的系统:钙信号和线粒体。钙离子作为许多细胞决策的微小开关,包括何时自毁。研究者发现,来自重症新冠患者的中性粒细胞胞内可游离钙较少,同时负责将钙输送入线粒体并打开可触发细胞死亡的安全阀的关键蛋白水平均降低。与此同时,线粒体本身异常“带电”,膜电位更高,且氧耗增加,尤其通过一个主要呼吸通路。线粒体并未关闭,反而更加活跃,产生更多活性氧分子,这些分子可损伤周围组织并助长炎症。
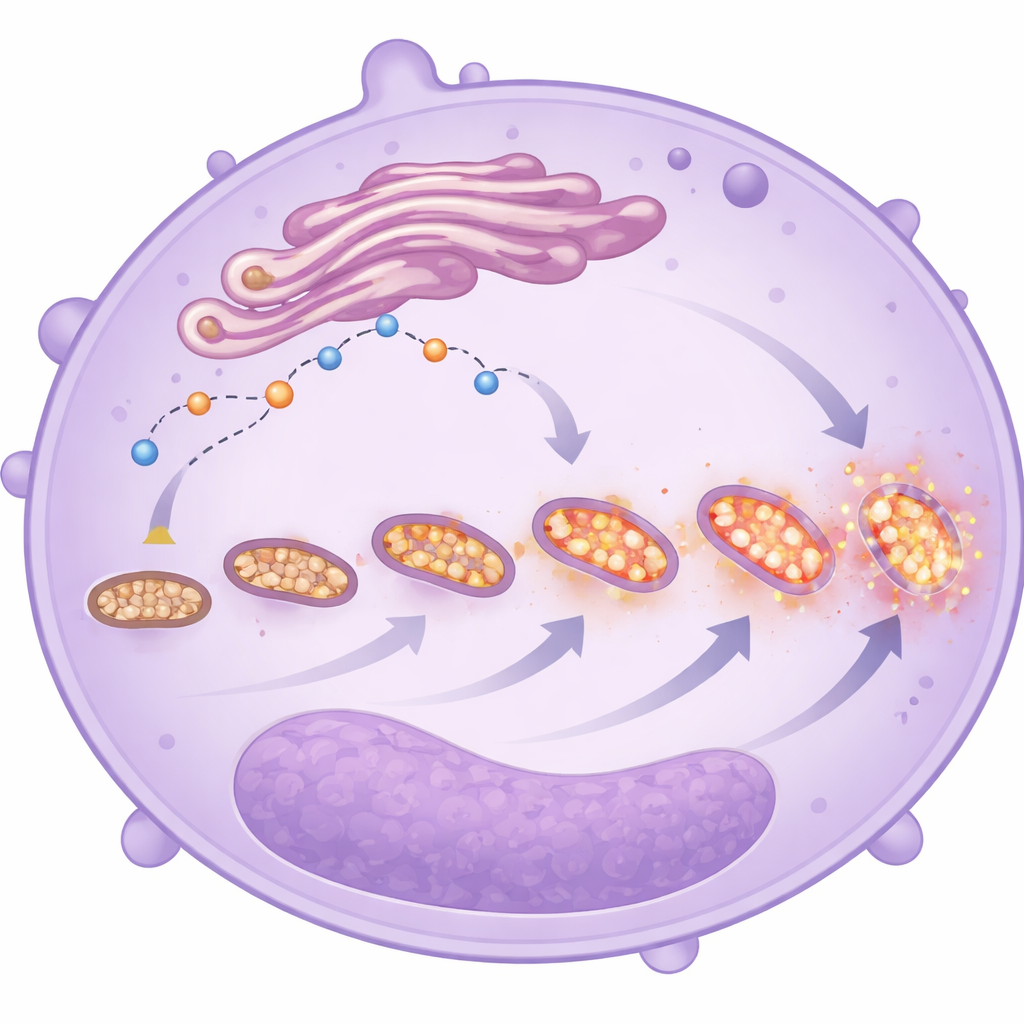
受压与碎裂的线粒体
电子显微镜图像与荧光染料提供了对这些线粒体形态与行为的更近观察。在最危重患者的中性粒细胞中,线粒体数量更多但更小且更碎裂——这些特征常提示应激。这些细胞还显示出更高水平的线粒体来源活性氧,无论患者最终是否存活。结合改变的钙处理和延迟的细胞死亡,这些变化勾勒出中性粒细胞已改变其能量策略的图景:它们不再主要依赖简单的糖酵解,而更多依赖线粒体代谢,尤其是在未成熟细胞中。这种转换可能增强它们的迁移、持久性以及在肺和其他器官释放有害分子的能力,尽管该研究不能证明这些改变是导致更差结局的直接原因。
这对未来治疗可能意味着什么
通俗地说,研究表明在危重的新冠中,中性粒细胞数量过多、偏年轻且难以关闭。它们的细胞内钙信号和线粒体被重新接线,使其保持存活并高度活跃,产生有害的氧基化学物质。虽然该研究为观察性,未能证明因果关系,但它指出了这些细胞中若干潜在的“调节旋钮”——例如钙调节因子和线粒体检点——未来可能通过温和调整来促使中性粒细胞恢复正常行为。如果后续研究证实这些想法,修复中性粒细胞关闭机制或平抑其过度充能的线粒体的治疗,有望减少这些关键细胞在重症新冠乃至其他危重疾病中造成的附带损伤。
引用: Elkhodiry, A.A., Yasseen, B.A., El-sayed, H. et al. Disruption of neutrophil homeostasis is associated with functional alterations in mitochondria of critically ill COVID−19 patients. Sci Rep 16, 7838 (2026). https://doi.org/10.1038/s41598-026-38741-y
关键词: COVID-19, 中性粒细胞, 线粒体, 炎症, 危重病