Clear Sky Science · zh
通过 SLCO2A1 介导前列腺素与药物运输的结构基础
分子守门员如何塑造药物与激素效应
许多常用药物和类激素分子在发挥作用前必须穿过细胞上的微小通道。本文探讨了其中一种通道——名为 SLCO2A1 的蛋白质,它帮助将强效的信号脂类前列腺素和若干常见药物转运入细胞。通过揭示该蛋白的三维结构及其与货物结合的方式,研究者阐明了为何某些药物能够被携带通过,而另一些则仅仅堵住了通道。这些见解可为更安全的药物设计和治疗炎症、疼痛、肠道疾病以及伤口愈合不良等相关病症提供指导。
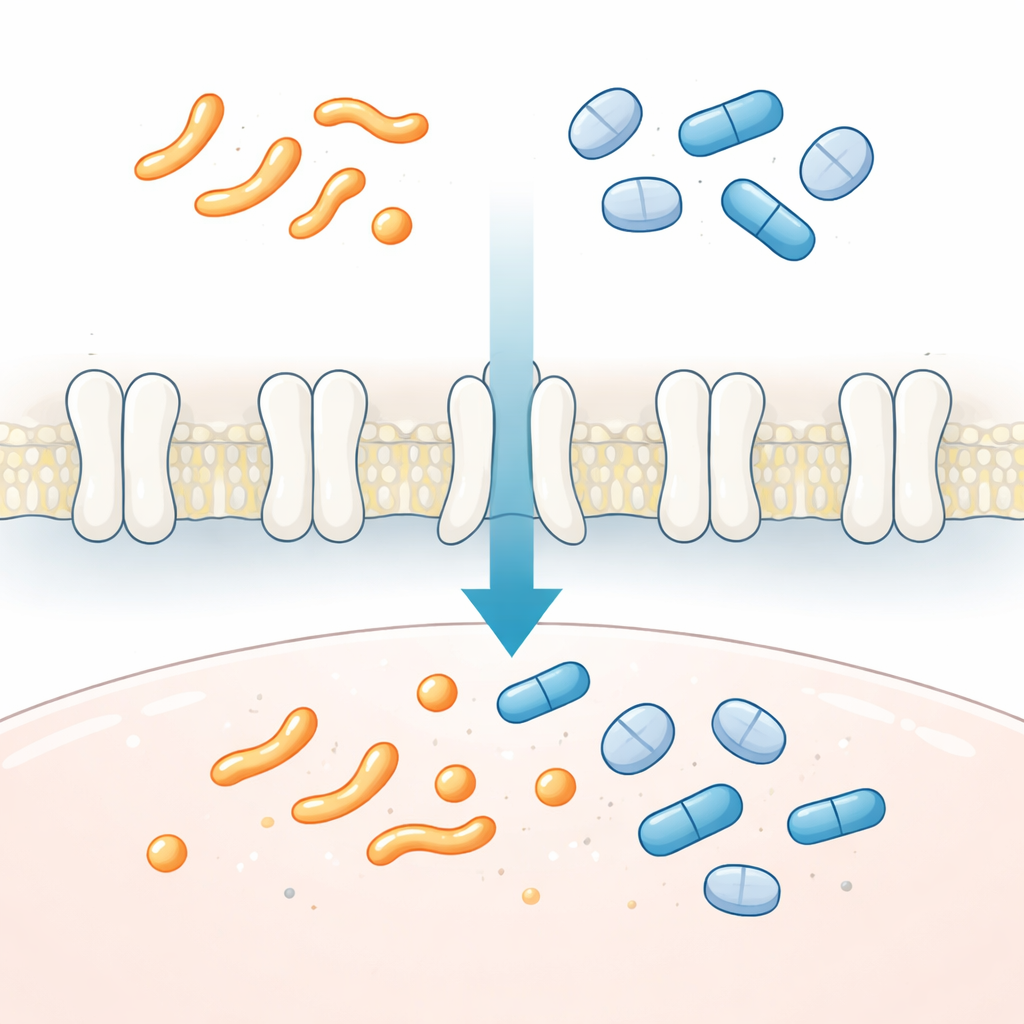
体内控制疼痛与炎症信号的交通指挥
前列腺素是寿命短暂、类激素的脂类分子,参与调节炎症、疼痛、发热、血流和器官发育。它们在生成处附近发挥作用,完成任务后必须迅速清除。SLCO2A1 位于细胞膜上,帮助将前列腺素及类似分子(如血栓素)从周围液相拉入细胞,在细胞内被分解。若该转运失常,前列腺素水平可能异常升高。SLCO2A1 的遗传缺陷已与罕见的骨骼和皮肤增生性疾病、慢性肠病以及溃疡愈合不良相关。由于前列腺素和许多广泛使用的药物共用这一进入细胞的通道,理解 SLCO2A1 的工作方式对于预测药物在全身的疗效与副作用至关重要。
以原子细节观察这个“门”
为弄清 SLCO2A1 如何识别并转运其货物,研究团队使用了冷冻电子显微镜,这是一种在近原子分辨率下成像速冻蛋白的方法。他们研究了与人类非常相似的近缘大鼠转运蛋白。研究者获得了该蛋白与两种天然前列腺素以及四种用于治疗哮喘、高血压、炎症和帕金森病的药物结合时的结构。在所有这些图像中,SLCO2A1 都呈现为十二条穿膜螺旋构成的束,形成一个向细胞外开放的中央空腔。前列腺素位于该空腔深处,其环状核心靠近一簇关键氨基酸,脂尾则穿入一个主要为疏油性的沟槽,与其疏脂性的性质相匹配。
选择通过的关键“握点”
通过比较结构并运行长时间的计算模拟,研究者识别出让 SLCO2A1 能区分真正货物与外观相似分子的特征。一个带正电的氨基酸——精氨酸 561(arginine 561),以及附近的色氨酸和苯丙氨酸,共同形成了对前列腺素带负电端的关键“握点”。当研究者突变这些残基时,转运基本失效,表明这一接触至关重要。周围的空腔主要为疏水性,偏好油性的、亲膜的分子,并包含一条在蛋白构象变化中起枢轴作用的“带”。两种药物扎非鲁卡斯特(zafirlukast)和氯沙坦(losartan)实际上会被转运,因为它们模仿了前列腺素向该精氨酸呈递负基团的方式,同时接触相同的疏水面。相比之下,抗炎药芬替阿扎克(fentiazac)和帕金森药物托卡朋(tolcapone)结合得不够紧密,无法稳定合适的构象,因此它们不是被携带通过,而是堵塞了结合位点。
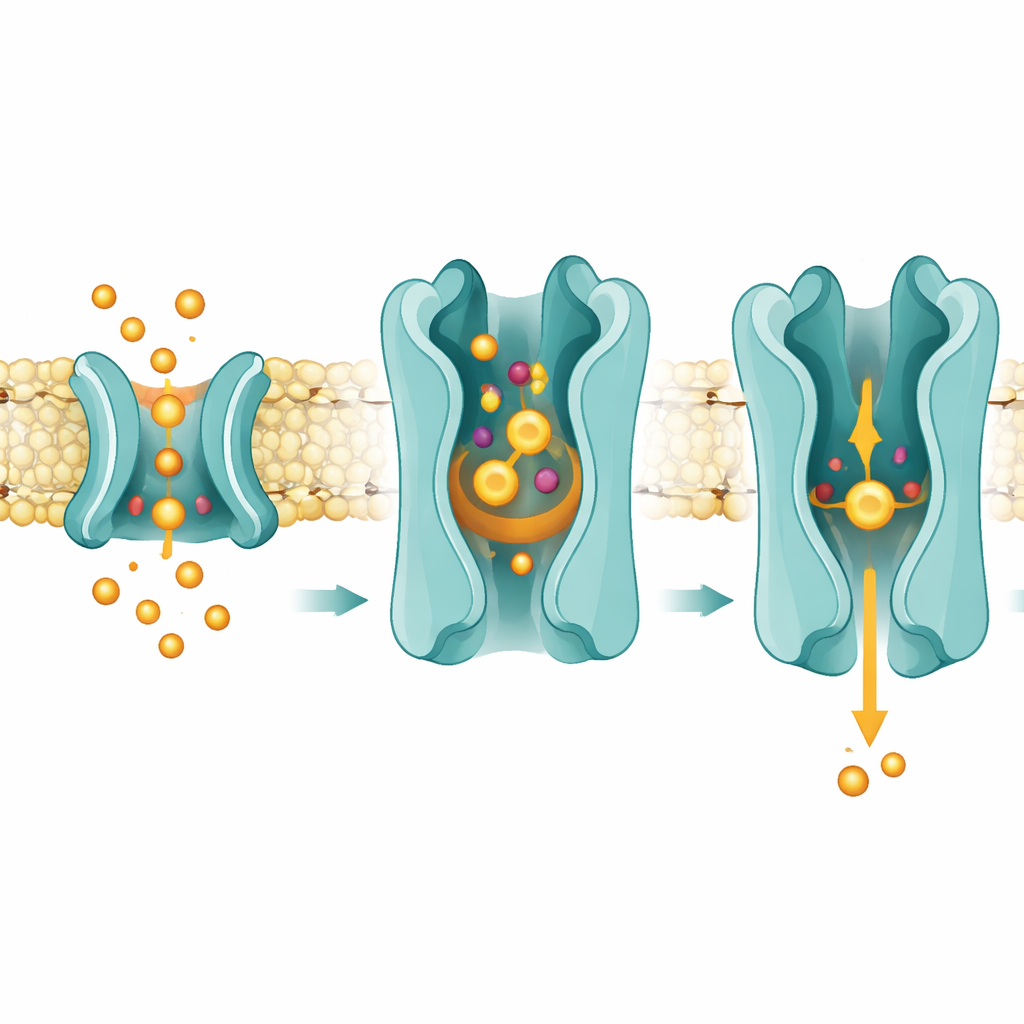
穿膜的侧门
这些结构还暗示前列腺素到达 SLCO2A1 并非来自开放水相,而是通过膜的脂质核心侧向滑入。研究者在两条螺旋之间的侧向开口处观察到与类脂分子相符的密度,正好位于前列腺素结合位点之上。致病突变和功能性测试将该区域定位为对转运至关重要。提出的机制是:前列腺素首先溶解在膜的外层,然后通过这个开口滑入转运蛋白。一旦结合到中央口袋,它们会破坏保守的盐桥(精氨酸 561 与一个谷氨酸残基之间),这反过来有助于触发转运蛋白由向外开放构象摆动到向内开放构象,将前列腺素释放到内层膜与细胞内部。
这对药物与疾病意味着什么
对外行来说,主要信息是 SLCO2A1 扮演着一个精细调控的门的角色,决定疼痛、发热和炎症等化学信号被关闭的速度,以及某些药物如何进入细胞。本研究以分子细节展示了该门如何识别前列腺素以及为何只有部分药物能搭乘该通道而另一些则堵塞通道。通过绘制关键接触点和穿膜侧入口路线,这项工作为设计新药提供了蓝图,使其要么能高效利用该转运系统,要么能在可控的情况下有意识地阻断它。最终,这类知识可能改善针对炎症性疾病、与前列腺素失衡相关的肠道疾病的疗法,以及在转运蛋白相互作用导致药物反应难以预测的治疗方案中的用药设计。
引用: Joshi, C., Deme, J.C., Nakamura, Y. et al. Structural basis for prostaglandin and drug transport via SLCO2A1. Nat Commun 17, 2285 (2026). https://doi.org/10.1038/s41467-026-70227-3
关键词: 前列腺素 运输, 药物 转运蛋白, SLCO2A1, 膜蛋白, 冷冻电镜 结构