Clear Sky Science · zh
通过1,2‑氧迁移实现的双环[1.1.0]丁烷硼酸酯的催化不对称官能化
为何微小的方形环很重要
化学家喜欢像搭积木一样把小分子片段拼接起来,以构建新的药物和材料。四元碳环(称为环丁烷)尤其受青睐,因为它们在狭小的体积内储存了大量能量和独特形状,这会改变药物在体内的行为。本文介绍了一种通过巧妙反应以高度可控的“单手式”(手性)形式构建这些环的新方法,该方法促使含氧基团从一个原子迁移到另一个原子。该工作为设计更复杂、更精确的药物分子和先进材料打开了新途径。
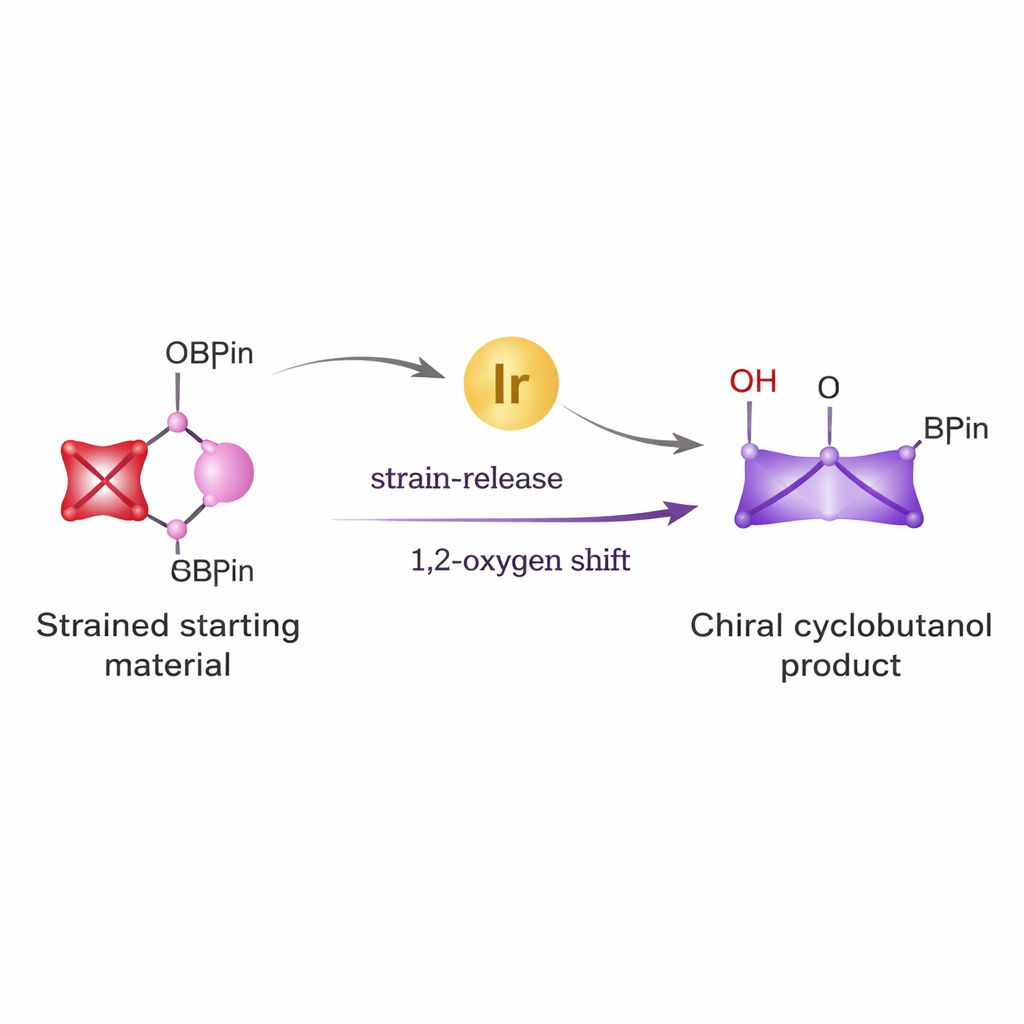
从简单构件到强效环系
环丁烷出现在多种抗病毒剂、抗癌候选分子和其他具有生物活性的化合物中。然而,要以药物所需的精确三维构型构建它们一直很困难。传统路线常常需要苛刻试剂,并产生难以分离的镜像产物混合物。作者试图通过结合两种强有力的思路来解决这一问题:利用一种极具应变的微小环——双环[1.1.0]丁烷的不寻常反应性,以及硼酸酯的多功能性,硼酸酯是形成碳‑碳键的交叉偶联化学中广泛使用的一类试剂。
将缺点变成新的反应通道
在常规金属催化的偶联反应中,硼酸酯会与烷氧基(基于氧的碱)形成中间配合物。该配合物几乎总是遵循一种常见路径——转金属化(transmetallation),随后直接形成新的碳‑碳或碳‑卤键。这一路径的“默认”优势使得探寻其他可能性(如氧基本身的迁移)变得困难。团队意识到,如果从应变的双环[1.1.0]丁烷硼酸酯出发,小环的内在张力可以用来覆盖通常的路径。通过将该应变体系与铱催化剂及精心选择的手性配体配对,他们希望在控制下促使氧发生迁移,同时环打开并重新闭合为环丁烷。
受应变引导的逐步舞蹈
实验证实了该策略的可行性。使用由各种醇——包括糖类、萜烯、甾体及简单脂肪族醇——制备的锂烷氧化物,作者将双环[1.1.0]丁烷硼酸酯转化为产率高且手性控制优良的顺式环丁醇产物。铱催化剂首先由烯丙基碳酸酯形成一个活泼的烯丙铱络合物。该络合物随后攻击受应变的双环[1.1.0]丁烷体系,在微小环打开的同时形成新的碳‑碳键。关键在于,所得的含硼中间体并未立即沿通常的转金属化路线进行,而是发生了碳‑硼键的微妙旋转,使得连接的氧基定位于可向邻碳原子清晰迁移的位置。该1,2‑氧迁移将新形成的环丁烷上的期望顺式构型锁定下来。
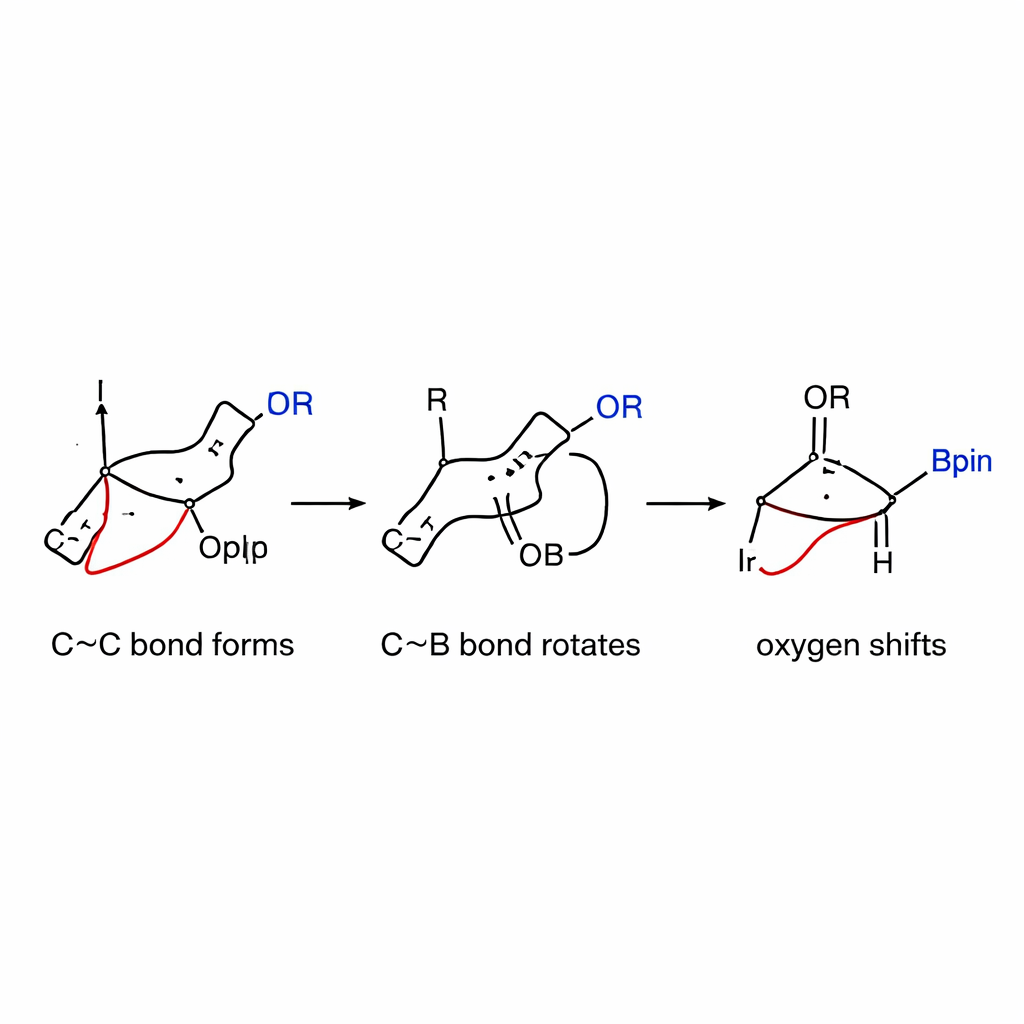
窥视机理内部
为理解为何该反应如此具有选择性,作者结合了动力学测定与详尽的计算机模拟。他们发现,决定速率的缓慢步骤是铱‑烯丙物种与应变硼酸盐络合物之间的初始碳‑碳键形成,而非前期烯丙基碳酸酯的活化。电子学测试显示,能稳定正电荷的烯丙配体反应更快,这支持一种在反应中形成部分带电中间体的机理。计算进一步揭示,在该体系中围绕碳‑硼键的旋转——此前被认为是困难的——具有出人意料的低能垒,这要归功于储存的环应变。一旦旋转将氧基对齐,1,2‑迁移顺利进行,并优先生成顺式产物而非更常见的反式构型。
为塑造未来药物提供新工具
除了解释机理外,该反应还提供了多用途的产物。环丁醇保留了硼酸酯单元,可利用已建立的化学方法转化为多种其他官能团。作者展示了多种“晚期”改造,如加氢、氧化、烯烃复分解和进一步偶联反应,同时保持了环的精确三维构型。简而言之,这项工作将曾经是问题的副路径——硼酸盐配合物中的氧迁移——转变为一个强大的合成工具。通过利用环应变与精细调控的铱催化剂,研究者为化学家提供了一种可靠方法来构建复杂、手性的环丁烷,这些分子可能在下一代药物和先进分子材料中发挥关键作用。
引用: Zhu, XY., Ji, CL., Dong, TG. et al. Catalytic asymmetric functionalization of bicyclo[1.1.0]butane boronic esters enabled by 1,2-oxygen migration. Nat Commun 17, 1941 (2026). https://doi.org/10.1038/s41467-026-69860-9
关键词: 环丁烷, 有机硼化学, 不对称催化, 双环丁烷, 氧迁移