Clear Sky Science · zh
与肿瘤相关的CD19+巨噬细胞在肝细胞癌中诱导免疫抑制微环境
为何机体的“守护者”有时会帮助肝癌
肝癌是全球最致命的癌症之一,部分原因在于肿瘤能够将机体自身的免疫系统变为助力。本研究揭示了肝肿瘤中一类令人意外的免疫细胞亚群,它们非但不抗癌,反而帮助肿瘤隐匿与生长。识别这些“叛变”细胞是谁以及它们如何运作,为提高肝细胞癌患者免疫治疗的疗效开辟了新途径。
肿瘤内的一类特殊免疫细胞
作者将注意力集中在与肿瘤相关的巨噬细胞上——这些免疫细胞通常负责吞噬病原与碎片,但在肿瘤内常被“腐化”。通过分析大量患者的肝肿瘤样本,他们发现一类携带表面分子CD19的独特巨噬细胞亚群,CD19通常出现在B细胞而非巨噬细胞上。与邻近的健康肝组织或血液相比,这些CD19阳性巨噬细胞在肝肿瘤中显著富集,且在其他若干实体瘤中也有增加。单细胞分析证实这些细胞确为巨噬细胞,具有独特的基因与蛋白表达谱,并非被误判的B细胞。
这些细胞如何营造有利于肿瘤的微环境
肿瘤中含有大量CD19阳性巨噬细胞的患者,往往肿瘤更大、更具侵袭性且存活期更短。富含这些细胞的肿瘤样本显示杀伤性CD8 T细胞减少而调节性T细胞增多,这是一种高度免疫抑制微环境的典型模式。在小鼠模型中,将CD19阳性巨噬细胞与肝癌细胞共同接种会加速肿瘤生长并减少有益的T细胞,同时增加其他抑制性髓系细胞。重要的是,当研究者使用识别CD19的工程化T细胞选择性清除这些巨噬细胞时,肝肿瘤即便在缺乏正常B细胞的小鼠中也出现缩小,进一步表明治疗靶点正是这些巨噬细胞本身。
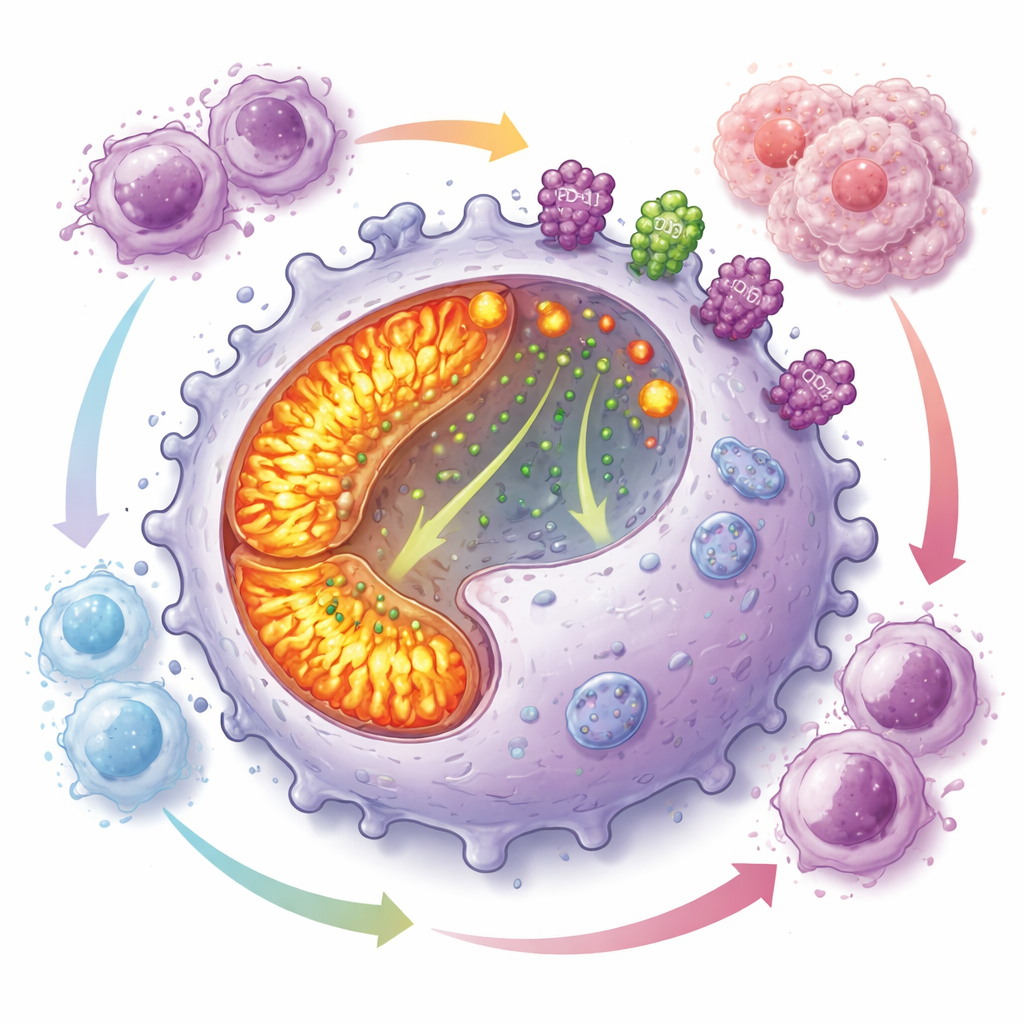
抑制免疫攻击的高能耗程序
深入研究显示,CD19阳性巨噬细胞以高强度运转其内部“发电厂”。其线粒体数量与活性均高于其他巨噬细胞,呈现增强的氧化磷酸化和活性氧。尽管处于这种高能状态,这些细胞吞噬靶标的能力较差,但增殖迅速,从而在肿瘤中积累。同时,它们在表面高度表达PD-L1和CD73——两种已知能抑制T细胞反应并产生腺苷(强效抑制免疫的小分子)的分子。共培养实验表明,这些巨噬细胞强烈抑制多种T细胞类型的增殖。
驱动“叛变”巨噬细胞的主开关
研究者鉴定出转录因子PAX5为该有害巨噬细胞程序的核心驱动因子。PAX5以指导B细胞发育闻名,但在这里它在CD19阳性巨噬细胞中高度活跃。强制使类巨噬细胞表达PAX5会促进线粒体生物生成、提高能量产出,并提高PD-L1、CD73和CD19的蛋白水平(而非mRNA水平)。机制性实验显示,PAX5将钙离子拽入线粒体,降低胞质钙,从而阻止关键调控因子TFEB进入细胞核。TFEB受抑后,溶酶体的生成与功能下降,导致像PD-L1和CD73这样的蛋白不再被有效降解,反而在细胞表面积累,加剧免疫抑制。
将发现转化为更好的治疗策略
鉴于这些巨噬细胞高度依赖CD73活性与线粒体代谢,作者测试了阻断这些通路是否能增强免疫治疗的效果。在小鼠肝癌模型中,将PD-L1阻断与CD73抗体或CD73抑制剂联合使用,能够使肿瘤变小、更多T细胞浸润并降低癌细胞增殖。同样地,将PD-L1抗体与线粒体氧化磷酸化抑制剂联用,也改善了肿瘤控制并促进免疫细胞进入肿瘤。显著的是,这些益处在巨噬细胞缺失PAX5的小鼠中消失,证实药物效应与破坏CD19阳性、由PAX5驱动的巨噬细胞程序相关。总体而言,这项工作表明选择性靶向这一巨噬细胞亚群——通过CD19导向的细胞疗法、CD73抑制或代谢药物——可能有助于将免疫学上“冷”的肝肿瘤转变为对现有免疫检查点阻断疗法更为敏感的肿瘤。
引用: Wang, J., Cao, W., Huang, J. et al. Tumor-associated CD19+ macrophages induce immunosuppressive microenvironment in hepatocellular carcinoma. Nat Commun 17, 3250 (2026). https://doi.org/10.1038/s41467-026-69638-z
关键词: 肝细胞癌, 与肿瘤相关的巨噬细胞, 免疫治疗, PD-L1 与 CD73, 线粒体代谢