Clear Sky Science · zh
肿瘤特异性 HORMAD1 表达扰乱有丝停滞并增加对有丝分裂激酶抑制剂的敏感性
这对癌症治疗的重要性
在细胞分裂时,细胞依赖复杂的安全检查来确保将正确的染色体组传递下去。癌症经常劫持或削弱这些防线,导致基因组混乱,这既推动疾病进展,也影响肿瘤对药物的反应。本研究揭示了一种异常蛋白 HORMAD1 的作用——该蛋白通常仅在生殖细胞中活跃,但在许多侵袭性乳腺癌和其他肿瘤中被重新激活。通过微妙破坏关键的细胞分裂检验点,HORMAD1 增强了癌细胞的不稳定性,同时也使它们对一类新型实验性药物特别敏感。
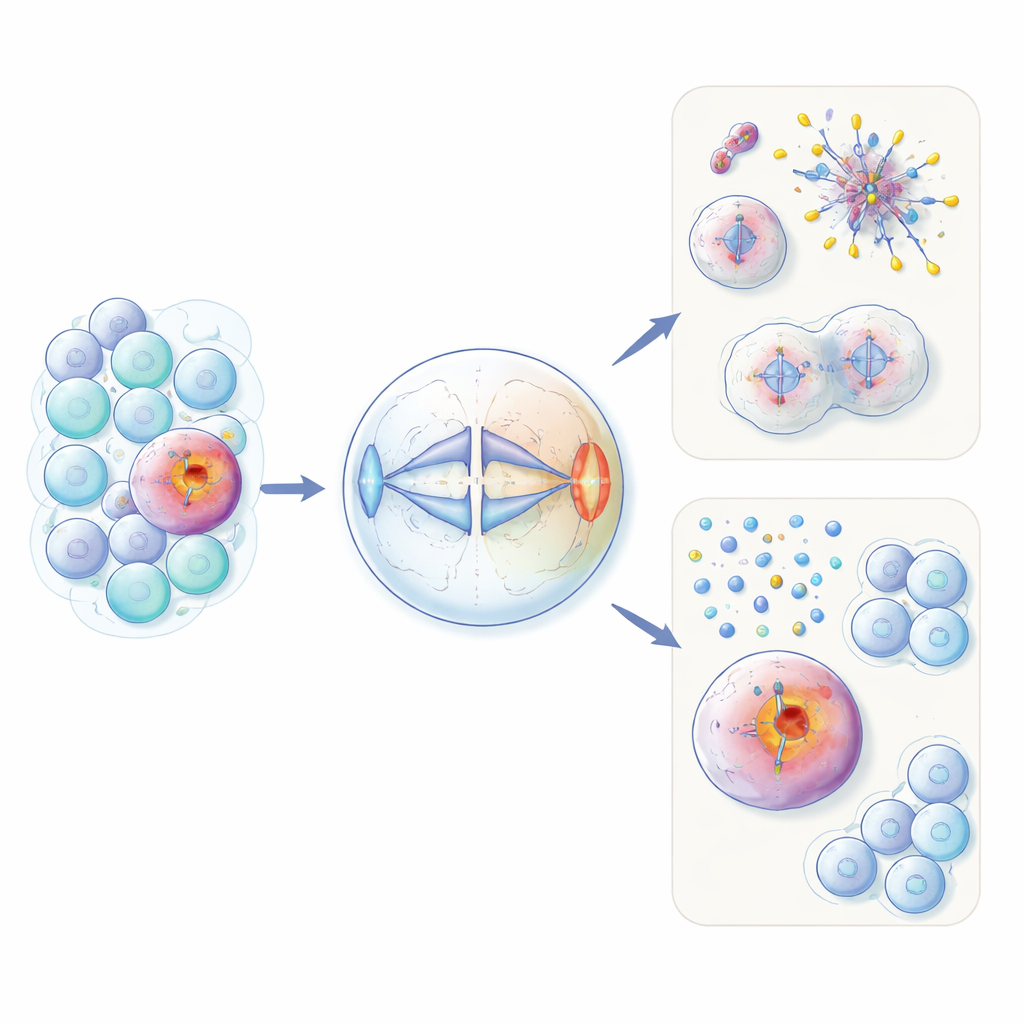
出现在肿瘤细胞中的错误生育蛋白
HORMAD1 通常只在生殖细胞中表达,在那里它参与减数分裂期间的 DNA 重组与质量控制。作者发现,在大约 60% 的三阴性乳腺癌以及若干其他肿瘤类型的亚群中,该蛋白被不恰当地重新激活。通过在工程化的非癌细胞和癌细胞系中研究,他们发现过量的 HORMAD1 干扰了常规有丝分裂过程中染色体的均匀分离。表达 HORMAD1 的细胞出现更多滞后染色体、染色体增减(非整倍性)以及小的含 DNA “微核”,这些都是侵袭性癌症中基因组混乱的典型标志。
细胞分裂安全检查的正常工作方式
为正确分裂,细胞构建由微管纤维组成的纺锤体并将其附着到每条染色体上。被称为纺锤体装配检验点的监控系统像一个对张力敏感的刹车:如果任何染色体未正确附着,刹车就会阻止分裂进程,直到错误被修复。若干称为有丝分裂激酶的酶(包括 MPS1、Aurora B 和 BUB1)帮助感知不良附着并促进“错误校正”,以确保每个子代细胞获得正确的染色体组。该系统的破坏既可以推动癌症发生,也可以产生某些药物可利用的特殊脆弱性。
HORMAD1 在无声中削弱了刹车
研究人员发现 HORMAD1 以一种微妙但重要的方式削弱了这一安全刹车。与直接干扰经典检验点组分(如 HORMA 蛋白 MAD2L1)不同,HORMAD1 直接与激酶 Aurora B 结合。Aurora B 通常与另一种蛋白 INCENP 配对以充分活化,并磷酸化着丝粒和着丝点处的靶蛋白——这些是纺锤体纤维附着的关键位点。当 HORMAD1 在分裂的肿瘤细胞中出现时,它与 INCENP 争夺与 Aurora B 的结合,减弱了二者的相互作用并抑制了 Aurora B 的活性。结果,Aurora B 对若干靶点的磷酸化信号减弱,错误校正效果下降,检验点变得“泄漏”:即使附着存在缺陷,细胞也过早退出有丝分裂,导致染色体错分离和基因组不稳定。
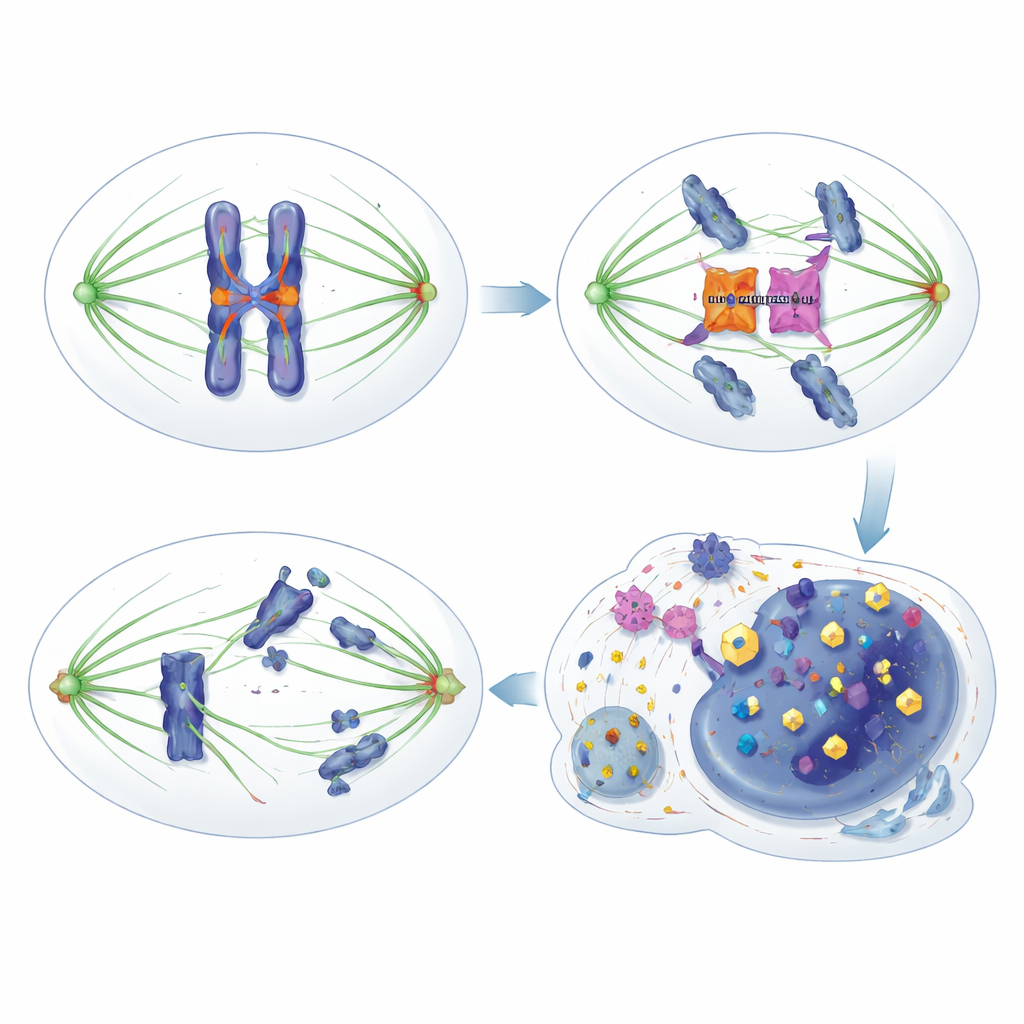
从脆弱性到治疗机会
由于 HORMAD1 只是部分削弱了 Aurora B 及相关防线,癌细胞仍然处于足以增殖的勉强存活状态,但它们高度依赖剩余的有丝分裂激酶功能以在反复出错的分裂中存活。研究组对此进行了测试:将 HORMAD1 阳性和阴性细胞暴露于 MPS1、Aurora B 和 BUB1 的实验性抑制剂。在多个模型中,HORMAD1 的表达使细胞对这些药物敏感性大幅增加,显著降低了增殖和克隆形成能力。遗传性去除 BUB1 在只有存在 HORMAD1 时特别致命,显示出强烈的选择性依赖性。在使用患者来源三阴性乳腺肿瘤的小鼠模型中,HORMAD1 水平高的肿瘤在使用纳米颗粒制剂的 Aurora B 抑制剂治疗后缩小或生长更慢,而 HORMAD1 阴性的肿瘤对相同治疗大多耐受。
这对患者的意义
对外行而言,HORMAD1 在癌症中像一把双刃剑:它推动肿瘤细胞向更大的染色体紊乱发展,从而促进疾病,但同时也使它们对少数残存的细胞分裂防线格外依赖。研究表明,这种被错位表达的生育蛋白通过误导 Aurora B 削弱了关键检验点,使 HORMAD1 阳性肿瘤对靶向 Aurora B、MPS1 或 BUB1 的药物特别敏感。因为 HORMAD1 在正常组织中几乎不存在但在一部分癌症中明显存在,它可能作为一种生物标志物,用于识别最有可能从这些新兴有丝分裂激酶抑制剂中获益的患者,进而为难治性癌症(如三阴性乳腺癌)开启新的靶向治疗途径。
引用: Walker, C., Kollarovic, G., Weekes, D. et al. Tumour specific HORMAD1 expression perturbs mitotic arrest and drives sensitivity to mitotic kinase inhibitors. Nat Commun 17, 2157 (2026). https://doi.org/10.1038/s41467-026-69561-3
关键词: HORMAD1, 三阴性乳腺癌, 染色体不稳定性, Aurora B 激酶, 有丝分裂检验点抑制剂