Clear Sky Science · zh
不同遗传谱系影响从婴儿期到青春期的体重指数
孩子的生长模式为何重要
当孩子看起来太胖或太瘦时,父母常常会担心,尤其是在儿童肥胖日益增多的今天。本研究提出了一个更深层的问题:影响儿童体重指数(BMI)的基因,是否在整个儿童期都相同,还是不同年龄阶段由不同基因决定?通过追踪数千名年龄从一岁到18岁的儿童,研究人员表明我们的基因组成在婴儿期、儿童期和青春期以不同方式影响生长——这些模式又与日后心脏病和糖尿病的风险相关联。
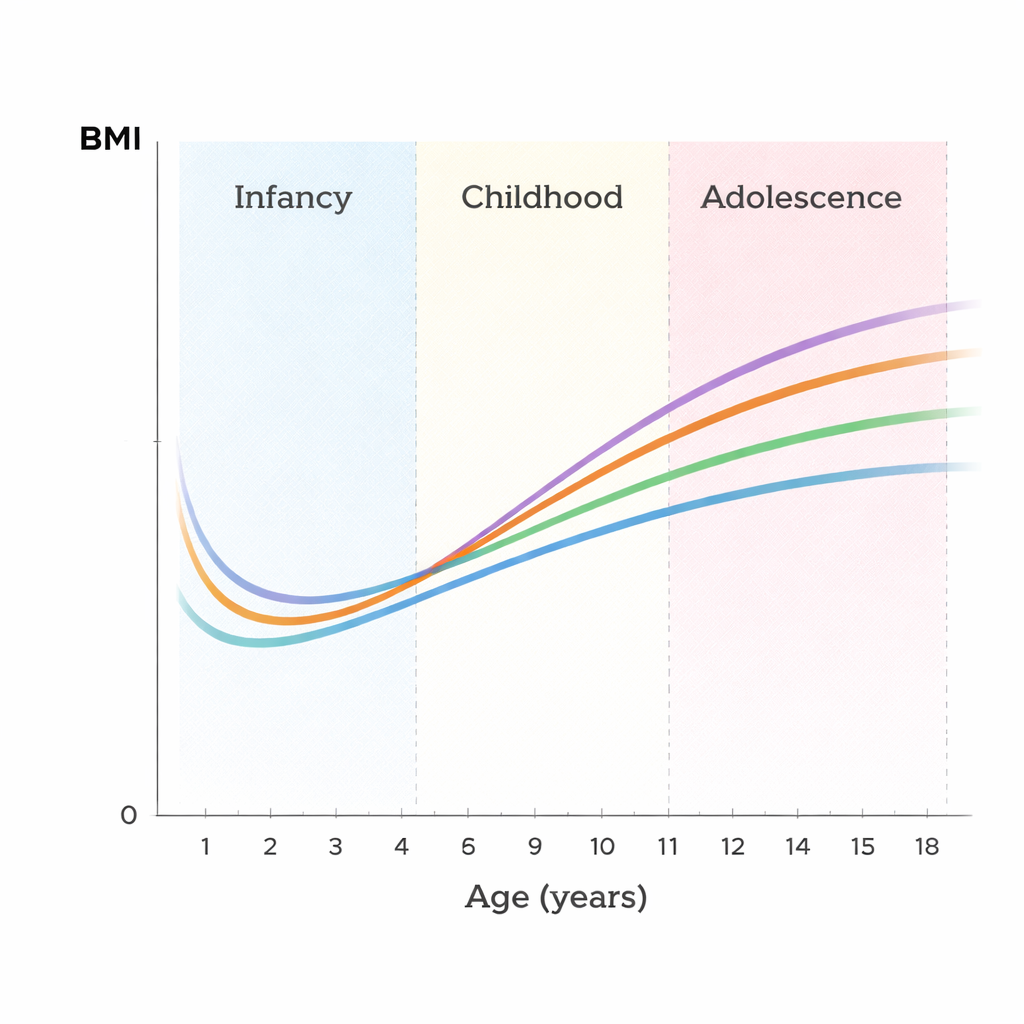
追踪数千名儿童的生长
研究团队分析了来自英国长期随访项目“阿冯父母与儿童纵向研究”(Avon Longitudinal Study of Parents and Children)中超过6200名儿童的数据。每个孩子平均在一岁到18岁之间接受了十次BMI测量。研究者没有只看单次测量值,而是采用一种称为随机回归模型的统计方法,将每个孩子的BMI视为随时间变化的平滑生长曲线。这使他们能够将遗传影响与其他个体因素区分开来,并估计在每个年龄段共有基因差异能够解释多少BMI差异。
持续起作用的基因与逐渐消退的基因
研究发现,常见的基因变异在任何给定年龄大约可以解释四分之一到三分之一的儿童BMI差异,这一比例从幼儿期到青春期相对稳定。然而,实际起作用的基因随年龄发生变化。影响一岁时BMI的基因几乎不与青春期重要的基因重叠。例如,统计上看,影响一岁与十岁BMI的基因几乎不相关,而相邻年龄(如一岁与二岁)之间的基因相关性则很高。这意味着婴儿期具有“高BMI基因”并不必然意味着在青春期或成年时存在相同类型的遗传风险。
两种主要的遗传生长模式
为了解这些与年龄相关的效应,研究者在遗传数据中寻找广泛的模式。他们发现了两条主要的遗传“轴线”,共同解释了几乎所有遗传性BMI生长差异。第一种模式在幼儿期时作用较弱,随后逐步增强,并在大约十岁时趋于平台。高分儿童往往在整个童年期间BMI较高、体重增长更快,并且在大约六岁时通常出现的脂肪“低谷”较不明显。第二种模式则呈近乎相反的作用:在婴儿期效果较强,随后减弱,甚至出现反向——一些在婴儿期提高BMI的变异在晚期青春期可能与较低BMI相关。
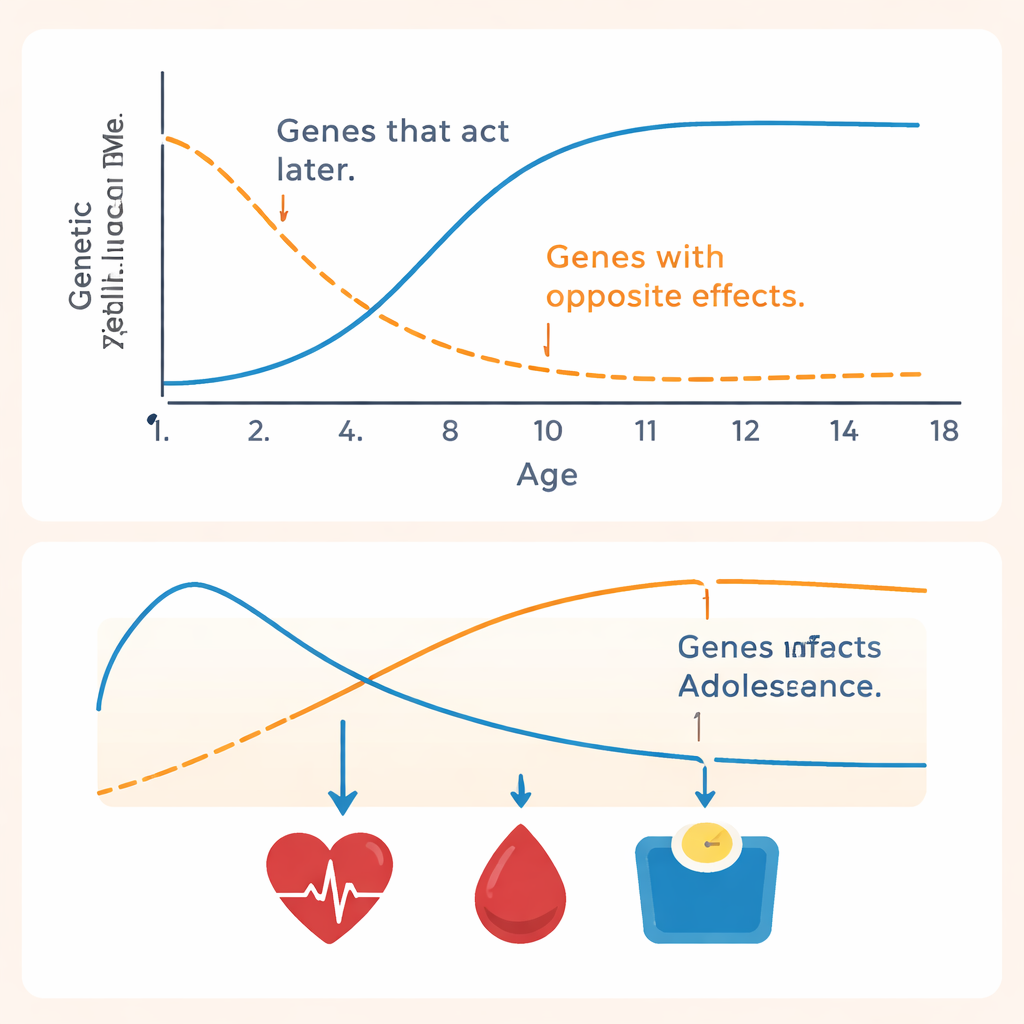
与成年体重和疾病的联系
研究团队还探讨了这些儿童期模式与已知成年肥胖基因及成年健康状况的关联。在将模型调整为基于成人BMI研究构建的多基因评分后,18岁时BMI的许多遗传变异可以被解释,但早期儿童期的遗传影响变化很小。这支持了婴儿期具有独特遗传驱动因素的观点。研究人员随后在基因组中检索影响儿童总体BMI水平和增长速度的变异,证实了多个知名肥胖相关基因的重要性,如FTO、ADCY3和OLFM4。他们还发现,儿童期较快的BMI增长在遗传上与成年体重较高、血脂和血糖水平更差以及2型糖尿病和高血压风险增加存在共同根源。
对家庭与预防的意义
简而言之,这项工作表明并不存在一种从摇篮到成年的单一“终生肥胖基因谱”。相反,不同的基因集在不同年龄阶段更为重要,从儿童后期开始出现一种强烈且持续的遗传推动力。与此同时,童年期间BMI增加的速度具有其自身的遗传成分,并与日后的心血管代谢风险相关。这些发现支持在整个儿童期关注健康的生长模式,而不仅仅集中在某一个关键年龄,并暗示未来基于基因的肥胖及相关疾病预测工具可能需要针对特定发育阶段进行定制。
引用: Wang, G., McEwan, S., Zeng, J. et al. Distinct genetic profiles influence body mass index between infancy and adolescence. Nat Commun 17, 1594 (2026). https://doi.org/10.1038/s41467-026-69310-6
关键词: 儿童肥胖, 体重指数, 遗传学, 生长轨迹, 心血管代谢风险