Clear Sky Science · zh
用于靶向降解 MYC 和 KRAS 的异功能蛋白拟体聚合物
用于击倒癌症最顽固蛋白的新工具
许多最危险的致癌蛋白,例如 MYC 和 KRAS,长期以来被标为“不可成药”,因为药物难以牢固结合它们。该研究揭示了一种新型柔性合成材料——称为 HYDRAC 聚合物——能够抓住这些难捉的蛋白并将它们送往细胞的垃圾处理系统。对于读者而言,这项工作展示了化学与纳米技术如何可能为长期对传统药物顽抗的癌症开辟治疗选项。
一个灵活的骨架,而不是单一片剂
大多数靶向抗癌药是小分子,像钥匙进入锁一样嵌入蛋白表面的口袋。但像 MYC 这样的蛋白柔软无定型且缺乏良好口袋,而 KRAS 常通过突变改变使经典药物失效。作者改为设计由重复单元组成的长链状聚合物。在这些链上他们连接两类成分:识别目标(如 MYC 或 RAS)的短蛋白结合片段,以及招募细胞自有降解机械的“降解标签”片段。由于每条链上装饰着许多相同的成分拷贝,单个 HYDRAC 分子可以同时接触多个蛋白和酶,这一点是单一刚性药物难以实现的。
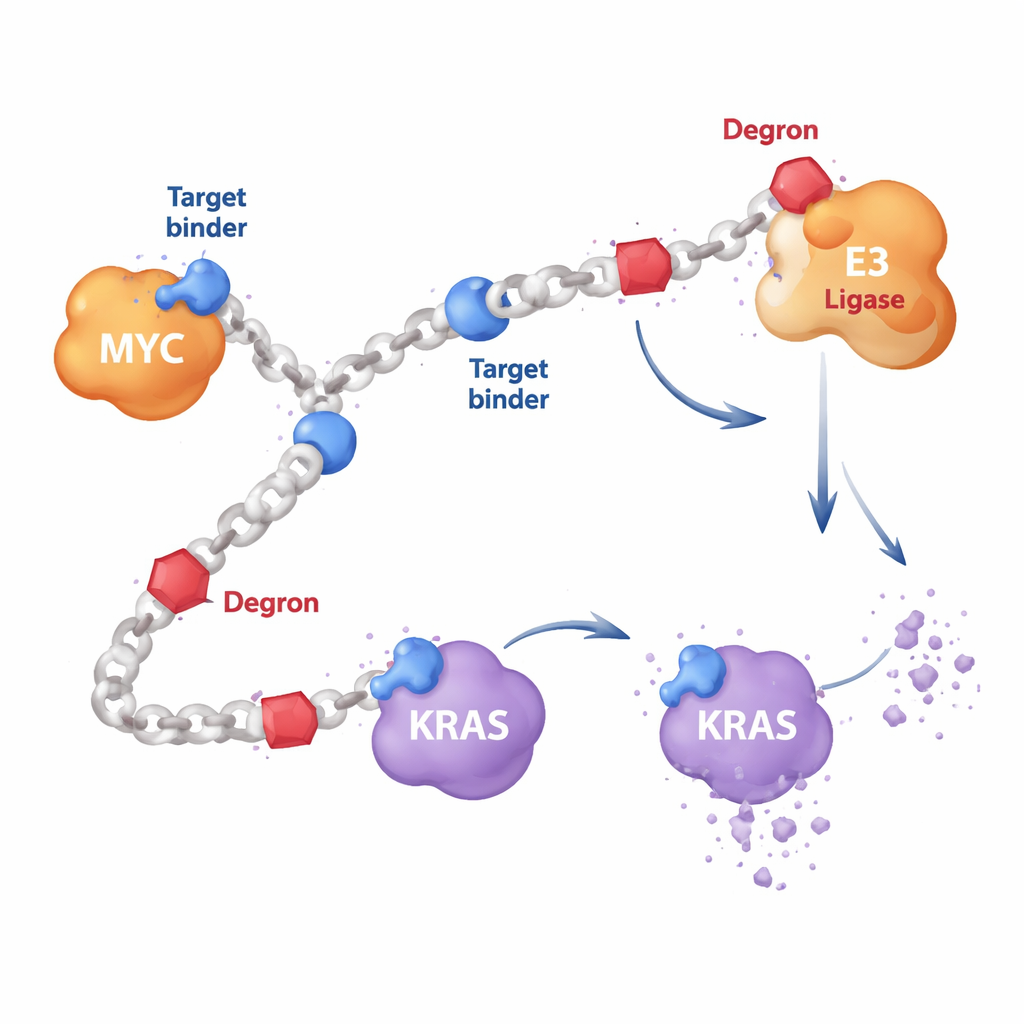
教会细胞分解 MYC
作为首次测试,研究者将注意力集中在 MYC——这一驱动众多癌症生长的主开关,但数十年来一直难以直接攻击。他们构建了在聚合物上展示已知 MYC 结合肽以及一个简单的降解基序(将蛋白标记为由细胞蛋白酶体降解)的 HYDRAC 聚合物。在试管实验中,这些聚合物折叠成紧凑、类蛋白的构象并紧密结合 MYC,但对无关蛋白则无明显结合。在癌细胞内,HYDRAC 易于进入细胞、扰乱 MYC 控制的基因程序并引发细胞死亡——这些效应依赖于靶向片段与降解片段同时存在于同一聚合物链上。
从细胞培养到肿瘤缩小
在细胞内部,HYDRAC 治疗导致 MYC 蛋白水平显著下降,但 MYC 的 RNA 水平并未减少,这表明是真正的蛋白破坏而非简单的转录关闭。阻断蛋白酶体或某些激活特定降解通路的关键酶可以恢复 MYC 水平,显示这些聚合物通过重新定向细胞自身的废物处理系统起作用。蛋白组范围的分析揭示很少有其他蛋白受影响,提示其选择性相当高。在 MYC 驱动肿瘤的小鼠模型中,荧光标记的 HYDRAC 在注射后优先在肿瘤中积累并停留数日。重复给药减缓了肿瘤生长且未导致明显体重下降或组织损伤,肿瘤样本显示分裂细胞减少并有更多程序性细胞死亡的迹象。
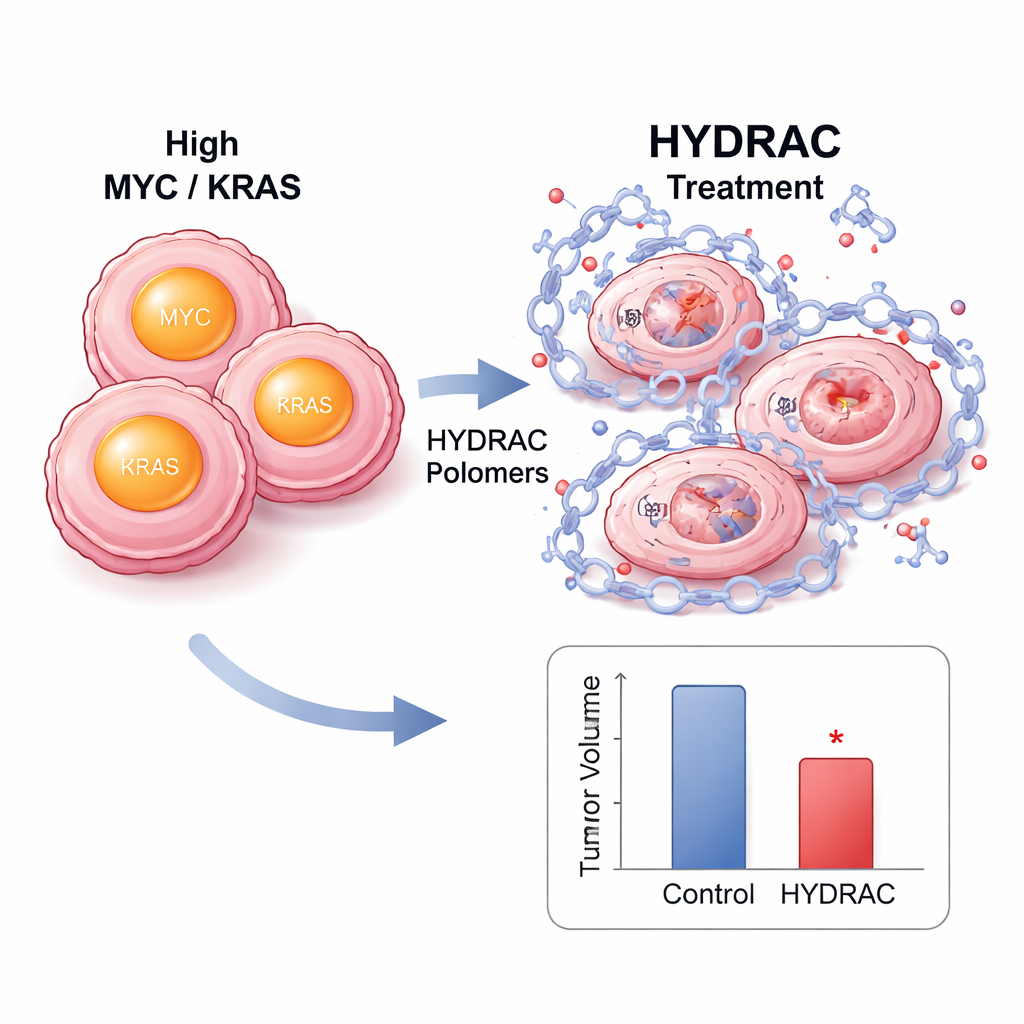
一种可插拔的平台,可对付多种疾病靶点
HYDRAC 方法的一大优势是其侧基可以像可互换部件一样替换。团队用其他招募元件替换了原始降解基序,这些元件可调用不同的细胞酶,包括识别药物沙利度胺的酶。每一种版本仅当目标酶存在且功能正常时才降解 MYC,证实了聚合物可调控以利用不同的细胞通路。为测试通用性,研究者随后用识别 RAS 蛋白的肽构建了针对 RAS 的 HYDRAC。这些构建体在两种不同的癌细胞系中成功降解突变型 KRAS,暗示其具有不依赖特定突变的“全 KRAS”潜力——对于存在多种 KRAS 变体的癌症而言,这是重要的一步。
这对未来癌症治疗为何重要
该工作将 HYDRAC 引入为一类可编程材料,这类材料不仅阻断问题蛋白——还帮助细胞将其抹去。通过在灵活的聚合物上结合多重靶向与降解单元,HYDRAC 绕开了传统小分子药物和 PROTAC 常见的设计限制(通常只能携带各一)。尽管在这些材料进入临床之前仍需大量工作,但在 MYC 和 KRAS 驱动模型中取得的结果表明,那些长期被认为“不可成药”的癌症蛋白,实际上在医学将分子设计更像定制刷而非单一小片剂时,可能会变得可攻克。
引用: Wang, M.M., Truica, M.I., Gattis, B.S. et al. Heterobifunctional proteomimetic polymers for targeted degradation of MYC and KRAS. Nat Commun 17, 1706 (2026). https://doi.org/10.1038/s41467-026-68913-3
关键词: 靶向蛋白降解, MYC, KRAS, 聚合物治疗学, 癌症纳米医学