Clear Sky Science · zh
阿尔茨海默病大脑的综合表观基因组图谱揭示与tau相关的少突胶质细胞分子扰动
这项大脑研究为何重要
阿尔茨海默病最著名的表现是记忆丧失以及两种有问题的蛋白在大脑中的堆积:淀粉样蛋白和tau。然而,即便诊断相同,患者的损伤模式也可能大不相同。本研究提出一个关键问题:脑细胞内哪些开关决定了这些有害蛋白的堆积程度,以及它们如何影响不同细胞类型?通过在数百个大脑样本中研究DNA上的化学标记,研究者发现了一个令人惊讶的联系:tau与负责大脑“线路”运作的细胞存在关联。
DNA上的化学标记作为隐藏的开关
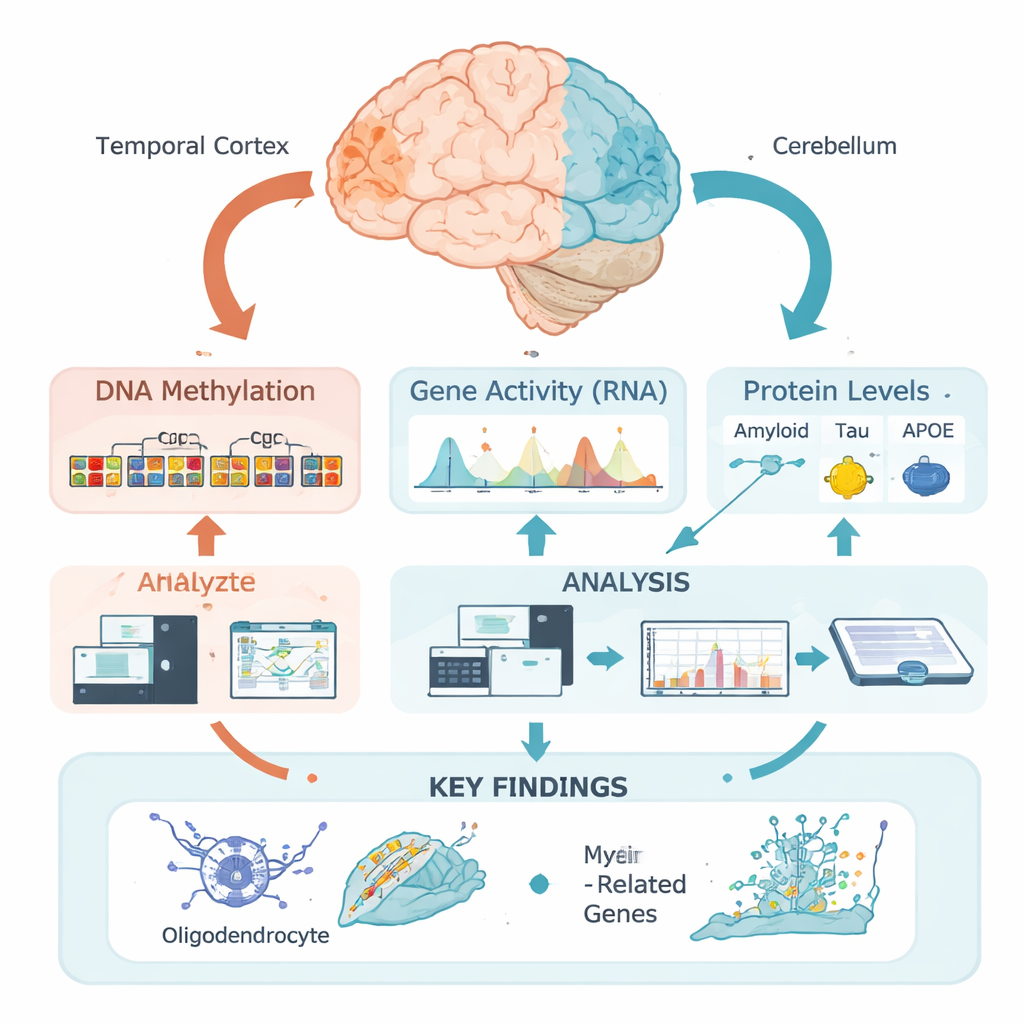
我们的DNA携带构建和维持脑细胞的基本指令,但这些指令由表观遗传标记管理——即不改变基因序列却能调节基因表达的化学标签。其中最重要的一类标记是DNA甲基化,即小的化学基团附着在特定DNA位点上。研究团队没有孤立地检查单个位点,而是采用了一种新的“区域性”方法:基于颞叶皮质(阿尔茨海默病受影响严重的区域)和小脑(相对受累较少的区域)中DNA的包装方式,将相邻多个位点分组为功能区。这使他们能够从生物学意义上询问甲基化模式在与疾病特征相关时在哪里发生改变。
将DNA标记与阿尔茨海默蛋白连接起来
研究者分析了472例经病理解剖确诊为阿尔茨海默病的脑组织。对每个颞叶皮质样本,他们详细测量了不同生化形式的淀粉样蛋白、tau和APOE蛋白水平,以及经典的显微镜学评分如淀粉样斑块和tau缠结。随后他们进行了表观基因组范围的关联研究,检验区域性DNA甲基化水平是否与这些测量值相关。引人注目的是,他们几乎所有的强关联都与tau有关——尤其是可溶性总tau和一种被认为特别有毒的膜结合磷酸化(化学修饰)形式。
在大脑“线路”细胞中发现的强烈信号
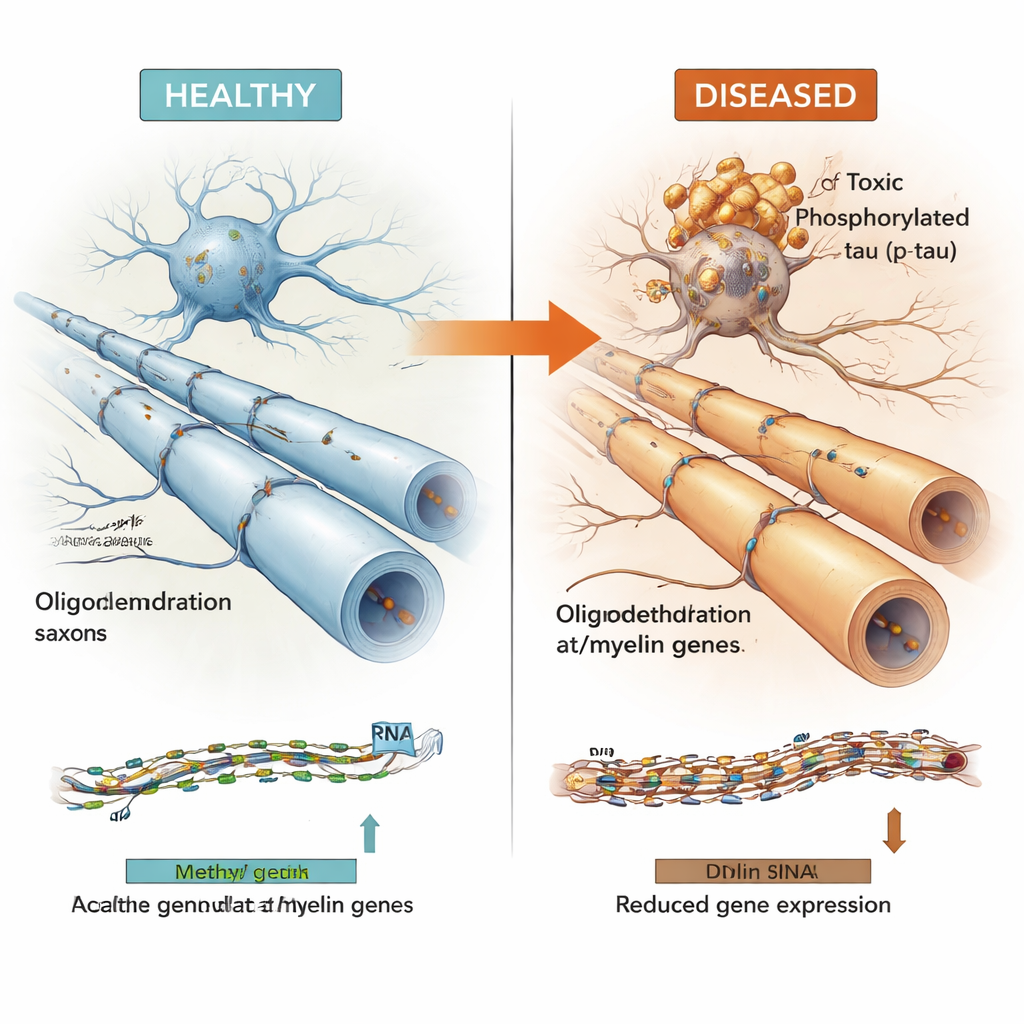
许多与tau相关的DNA区域位于影响附近基因的“活跃”基因组片段中。通过将甲基化数据与来自同一批大脑的基因活性测量结合,团队证明这些区域常常调控少突胶质细胞使用的基因。少突胶质细胞负责将神经纤维用髓鞘包裹,从而使电信号快速且可靠地传导。关键的髓鞘相关基因如MBP、MAG和MYRF,以及阿尔茨海默风险基因BIN1和一个新的候选基因LDB3,都出现在这一组中。更高水平的有毒磷酸化tau通常与这些区域甲基化增加和相关少突胶质细胞及髓鞘基因表达降低同时出现,而更为“温和”的可溶性总tau则呈相反模式。
在多种脑病中观察到的模式
为检验这些发现的稳健性和普遍性,作者考察了来自其他阿尔茨海默病大脑集合的庞大独立数据集,以及受原发性“tau病”影响的大脑,如进行性核上性麻痹和Pick病。尽管这些队列使用了不同技术并常常来自不同脑区,许多相同的DNA区域和少突胶质细胞基因表现出一致的行为:它们的甲基化水平与tau缠结负荷相关,其表达在病变大脑和专门针对少突胶质细胞的单细胞研究中均被降低。重要的是,这些模式似乎不能仅用遗传因素或细胞总体丧失来解释,提示少突胶质细胞功能发生了真正的表观遗传学转变。
这对理解阿尔茨海默病意味着什么
综合起来,结果支持这样一种模型:有害tau水平上升与少突胶质细胞中表观遗传改变紧密相关,这些改变抑制了髓鞘相关基因,可能削弱大脑的传导线路并促成认知衰退。目前仍不清楚二者哪个先发生——是tau堆积还是这些髓鞘基因的扰动——但在数千个样本和若干疾病中反复出现的紧密关联指向一种共同机制。通过绘制这些DNA开关并将其整合到公开的“多组学图谱”中,这项工作突出了少突胶质细胞及其表观遗传调控,作为未来旨在稳定脑路而非仅针对神经元或淀粉样斑块的治疗策略的有前景靶点。
引用: Oatman, S.R., Reddy, J.S., Atashgaran, A. et al. Integrative epigenomic landscape of Alzheimer’s Disease brains reveals oligodendrocyte molecular perturbations associated with tau. Nat Commun 17, 2116 (2026). https://doi.org/10.1038/s41467-026-68864-9
关键词: 阿尔茨海默病, tau蛋白, DNA甲基化, 少突胶质细胞, 髓鞘