Clear Sky Science · zh
ASCT2 的棕榈酰化受 JNK1–ZDHHC14 轴调控,协调谷氨酰胺代谢与非小细胞肺癌进展
为肺癌“添柴加火”
许多快速生长的肺癌依赖谷氨酰胺——一种常见氨基酸,既是重要能量来源也是合成构件。本研究揭示了肿瘤细胞如何精细调控表面的主要谷氨酰胺“闸门”,以及破坏该控制系统如何减缓癌症生长。理解这一隐藏的燃料阀有助于解释为何某些肿瘤难以被“断粮”,并指向可能更有效切断其能量供应的新药物组合。
细胞的谷氨酰胺通道
谷氨酰胺主要通过位于细胞膜外侧并将其运入细胞的转运蛋白 ASCT2 进入细胞。非小细胞肺癌(NSCLC)是最常见的肺癌类型,常严重依赖谷氨酰胺以支持快速分裂和存活。肿瘤中高水平的 ASCT2 与侵袭性疾病和较差的患者预后相关。然而 ASCT2 自身在不断合成、修饰和降解,这提出了一个问题:到底是什么决定了任何时刻有多少“守门员”留在细胞表面?
为 ASCT2 打上降解标签
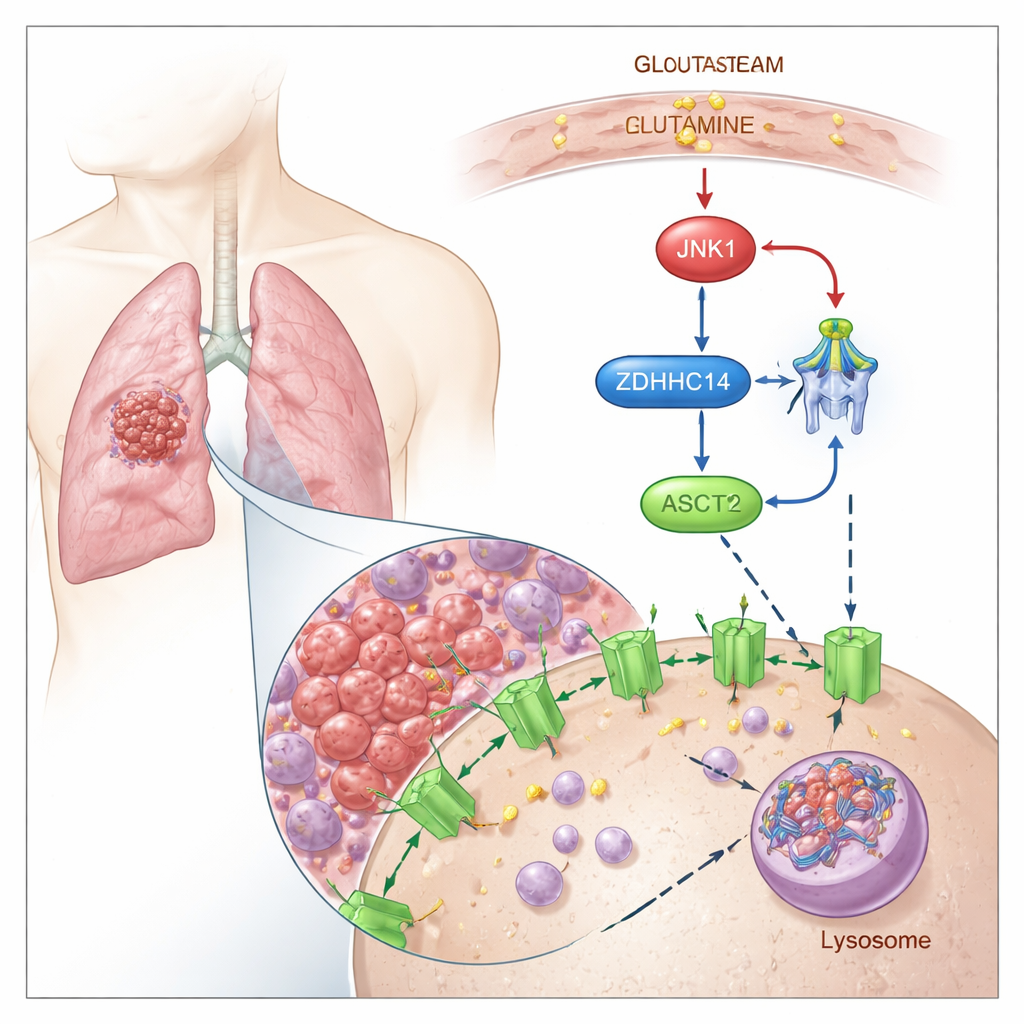
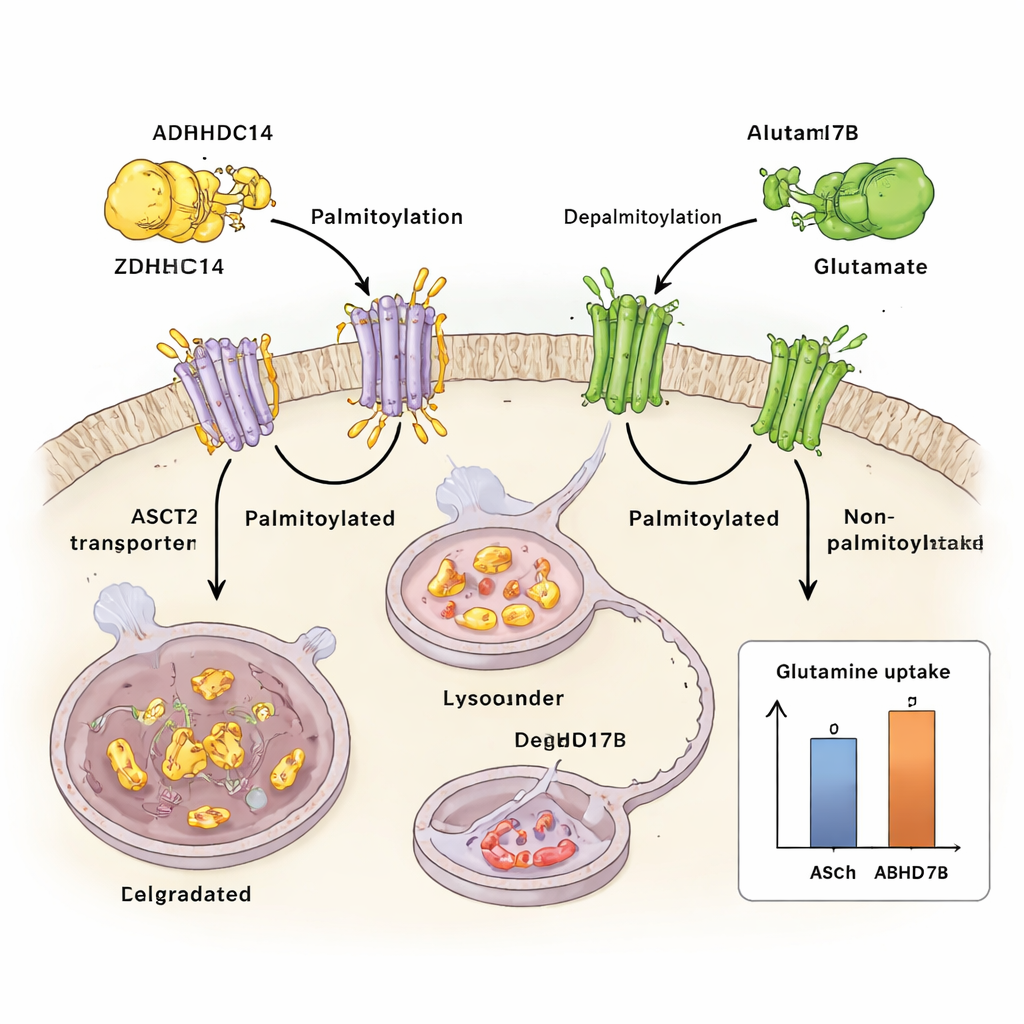
研究者表明,ASCT2 受一种称为棕榈酰化的化学“标签”调控,即在蛋白特定的半胱氨酸残基上连接一种脂肪酸。他们发现酶 ZDHHC14 将该脂质标签加到 ASCT2 的两个保守位点(Cys39 和 Cys48)。一旦被标记,ASCT2 就会从细胞表面被转运到称为溶酶体的细胞回收中心,在那里被降解。阻断棕榈酰化可阻止 ASCT2 被标记和降解,导致 ASCT2 蛋白水平升高并增强谷氨酰胺摄取,而不改变其基因的基础转录活性。
保护“闸门”的反向酶
与 ZDHHC14 对抗的是另一种酶 ABHD17B,它可以从 ASCT2 上去除脂质标签。当 ABHD17B 活性增强时,ASCT2 的棕榈酰化减少,更加稳定,并更可能被回收到细胞表面而不是送往溶酶体。这样的标记与去标记往复作用,就像对谷氨酰胺流量的精细调节旋钮:ZDHHC14 将 ASCT2 推向降解,而 ABHD17B 则拯救它以维持谷氨酰胺转运。在肺癌细胞中,将这一平衡移向更少的棕榈酰化会增加谷氨酰胺摄取,并在体外培养和小鼠模型中支持肿瘤生长。
营养胁迫如何重接该系统
团队随后考察了当肿瘤细胞缺乏谷氨酰胺时发生的变化。在谷氨酰胺匮乏下,一种对胁迫敏感的信号蛋白 JNK1 被激活。JNK1 与 ZDHHC14 直接结合,并在其特定位点(Thr440)添加一个磷酸基,标记 ZDHHC14 以供自身被溶酶体降解。随着 ZDHHC14 水平下降,ASCT2 收到的棕榈酰化标签减少,逃避降解并在细胞表面累积——恰恰是在细胞最需要抢夺稀缺谷氨酰胺的时候。突变这个单一的 JNK1 敏感位点可以稳定 ZDHHC14、恢复 ASCT2 的标记并降低谷氨酰胺摄取,凸显了营养胁迫如何被紧密接入该控制环路。
将机制转化为治疗策略
由于 ASCT2 对肿瘤代谢至关重要,阻断其功能的药物(如实验性化合物 V9302)正被探索用于癌症治疗。本研究表明 JNK1 信号可以抵消 ASCT2 的降解,有效地保护了谷氨酰胺“闸门”。在 NSCLC 的细胞和小鼠模型中,联合使用 JNK 抑制剂和 V9302 比单独使用任一药物更强烈地降低了谷氨酰胺摄取、肿瘤细胞生长和肿瘤体积。患者样本和公共数据集进一步显示,NSCLC 中常见低 ZDHHC14 和高 ASCT2 的表达模式与较差生存相关,提示这种分子特征可能有助于识别最有可能从靶向该通路中获益的患者。
这对患者意味着什么
通俗地说,这项工作表明某些肺癌通过调节细胞表面的分子阀来控制其最爱的燃料。由 JNK1、ZDHHC14 和 ABHD17B 三者组成的网络决定了谷氨酰胺通道 ASCT2 是被打上降解标签还是保持开放。当谷氨酰胺稀缺时,系统会转向保护 ASCT2 并保持燃料流动,帮助肿瘤在艰难环境中存活。通过同时阻断 ASCT2 和保护它的 JNK 通路,研究者在体外与动物模型中更有效地“饿死”了癌细胞。尽管仍需更多测试,这一磷酸化—棕榈酰化轴为旨在切断谷氨酰胺饥饿型肺瘤营养生命线的治疗提供了有前景的新角度。
引用: Chen, X., Ke, Z., Wei, S. et al. ASCT2 palmitoylation regulated by JNK1-ZDHHC14 axis orchestrates glutamine metabolism and NSCLC progression. Cell Discov 12, 13 (2026). https://doi.org/10.1038/s41421-026-00870-z
关键词: 谷氨酰胺代谢, 非小细胞肺癌, ASCT2 转运蛋白, 蛋白质棕榈酰化, JNK 信号通路