Clear Sky Science · zh
AdipoR1–AMPK 轴通过包括铁死亡和细胞凋亡在内的多模态细胞死亡途径抑制各分子亚型的乳腺癌
为什么脂肪细胞对乳腺癌重要
我们大多数人把体内脂肪看作被动的能量储备,但脂肪细胞实际上是活跃的工厂,会向血液释放激素和信号分子。本研究探讨了其中一种来自脂肪的信号通过乳腺癌细胞上的受体分子 AdipoR1 如何减缓肿瘤生长。该研究具有重要意义,因为它提示了一种利用脂肪组织与肿瘤之间通讯来治疗多种乳腺癌的新途径,可能还可增强现有药物的疗效。
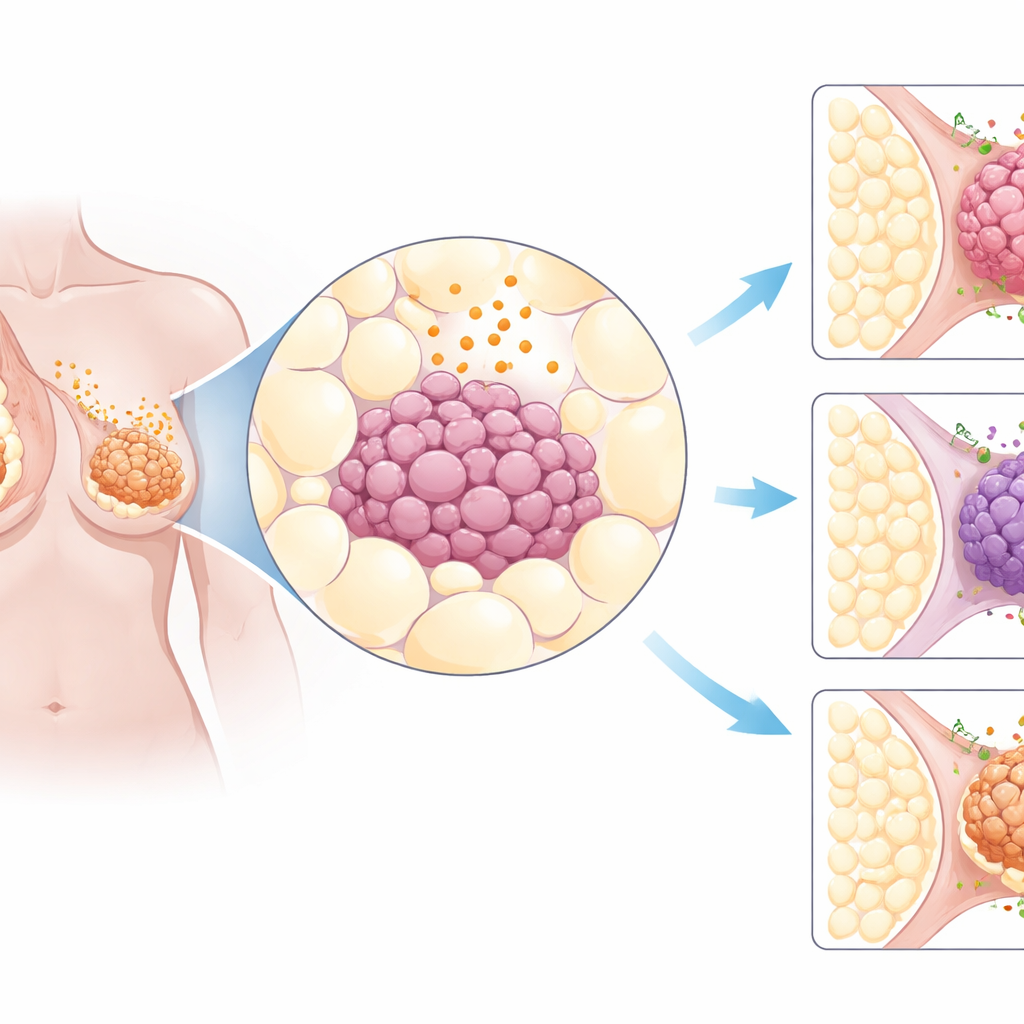
跨多种癌症的比较
研究人员首先挖掘了包含数千例患者肿瘤基因信息的大型公共癌症数据库。他们关注大约三打参与脂肪组织信号及接收这些信号的细胞结构的基因。将来自 31 个不同器官的肿瘤与健康组织比较时,一个模式很突出:与脂肪相关的这些信号在乳腺癌中表现出特别显著的改变。尤其是受体 AdipoR1 在乳腺肿瘤中常常呈现高于正常水平的表达,无论肿瘤是激素驱动、HER2 阳性,还是更具侵袭性的三阴性类型。超过 600 例乳腺癌的组织样本证实,AdipoR1 蛋白在肿瘤细胞中广泛存在。
在癌细胞上测试脂肪信号药物
为了弄清 AdipoR1 在肿瘤内的具体作用,团队使用了在实验室培养的代表几种常见亚型的乳腺癌细胞系。他们用 AdipoRon 处理这些细胞,AdipoRon 是一种能激活 AdipoR1 的小分子。AdipoRon 快速触发了细胞内已知的能量感应开关 AMPK,表明信号已传递进去。随着 AdipoRon 剂量增加,癌细胞增殖变慢,在伤口愈合试验中移动减少,且许多细胞发生程序性自毁。研究人员有意降低细胞中的 AdipoR1 水平后,AdipoRon 的作用大为减弱;反之提升 AdipoR1 则使药物更有效,表明该效应与该受体直接相关。
将癌细胞推向死亡的多种途径
通过分析处理后的基因活性,科学家们发现 AdipoRon 在乳腺癌细胞内启动了应激反应。它激活了与常规程序性细胞死亡相关的基因,也激活了与一种较新识别的铁依赖性细胞破坏形式——铁死亡(ferroptosis)相关的基因。该过程的关键标志在 RNA 和蛋白水平均有所上升,尤其在激素敏感型乳腺癌细胞中明显,细胞脂质损伤的化学检测也支持这一发现。与此同时,AdipoRon 降低了通常帮助癌细胞生存的蛋白水平,包括 DNA 修复相关蛋白(BRCA1 和 BRCA2)、驱动许多肿瘤生长的雌激素受体,以及与侵袭性行为相关的表面分子 TROP2。
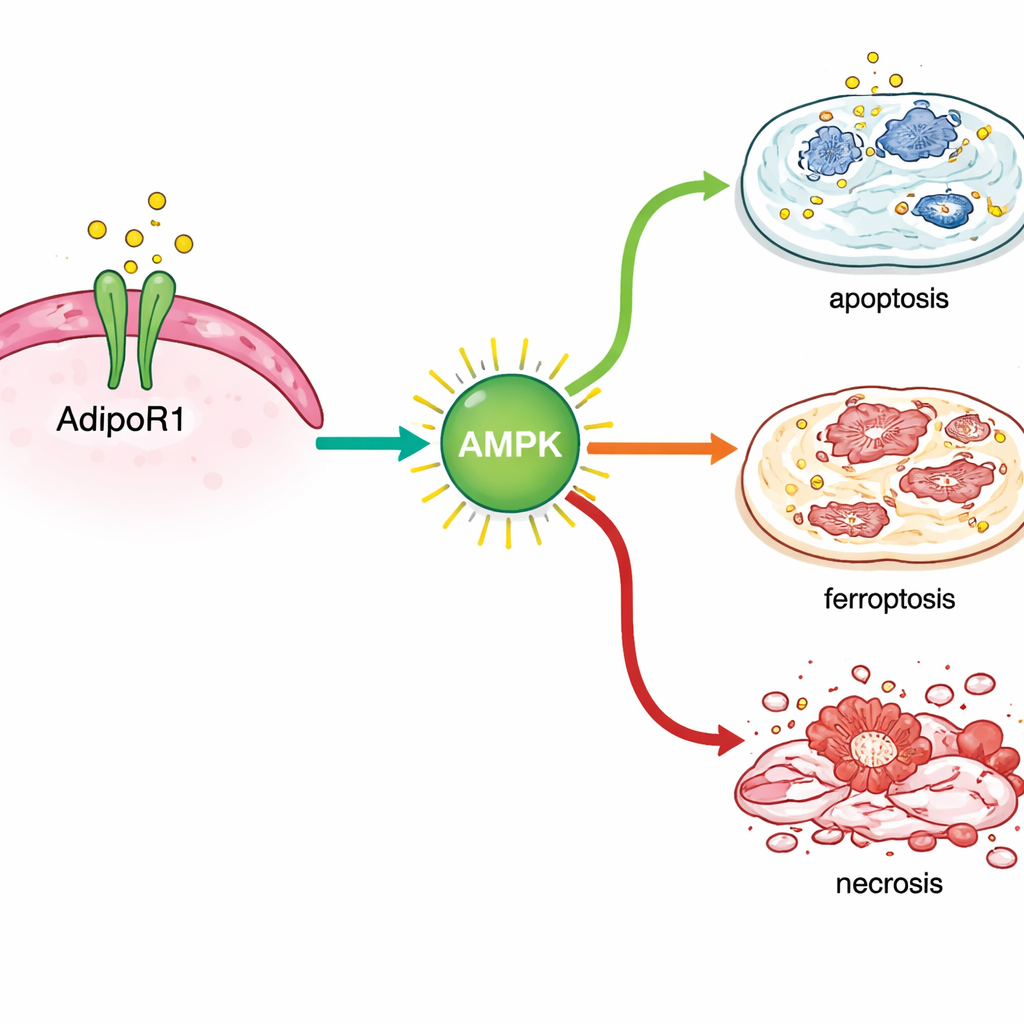
与现有治疗协同,而非对抗
接着团队探讨了激活 AdipoR1 是否能补充标准药物。在激素敏感型乳腺癌细胞中,AdipoRon 与他莫昔芬联用比各自单用产生更强的生长抑制。在三阴性细胞系中,AdipoRon 增强了紫杉醇和阿霉素等常用化疗药物的效果。在带有激素敏感型乳腺肿瘤的小鼠模型中,研究者通过口服给予 AdipoRon。处理组动物的肿瘤生长更慢,切片显微镜下显示更大的坏死区域。重要的是,在治疗期间小鼠在行为、体重或肝脏健康方面没有出现明显的不良反应。
这对患者可能意味着什么
综上所述,这些发现表明在乳腺癌细胞中激活 AdipoR1 会同时动员多条重叠的细胞死亡通路并削弱关键的生存系统,而且这种方法在不同遗传形态的疾病中均有效。与其替代现有疗法,像 AdipoRon 这样的靶向 AdipoR1 的药物更可能作为加成疗法,使肿瘤对激素疗法、化疗或未来的靶向药物更易受攻击。在这一策略进入临床之前,研究者还需要开发更强效、选择性更高的 AdipoR1 激活剂,明确哪些患者的肿瘤对该受体有更高表达,并仔细评估安全性。尽管如此,这项工作提出了一个发人深省的想法:我们自身脂肪组织发出的信号或可被重新利用,帮助对抗乳腺癌,而不是助长它的发展。
引用: Sato, S., Yamanaka, T., Komori, Y. et al. AdipoR1–AMPK axis suppresses breast cancer across molecular subtypes via multimodal cell death pathways, including ferroptosis and apoptosis. Cell Death Dis 17, 384 (2026). https://doi.org/10.1038/s41419-026-08583-7
关键词: 乳腺癌, 脂肪因子, AdipoR1, 细胞死亡途径, 癌症代谢