Clear Sky Science · zh
脂筏在通过TRPA1通道参与的FGFR2c介导的致癌信号传导中对胰腺导管腺癌细胞的作用
为何细胞膜上的小“岛屿”重要
胰腺癌是最致命的癌症之一,部分原因在于其细胞异常善于从原发肿瘤脱落并侵入邻近组织。本研究聚焦于癌细胞外层膜上由胆固醇和脂质构成的微小“岛屿”,提出了一个看似简单但影响深远的问题:这些“岛屿”是否有助于开启一种使胰腺癌更具侵袭性的生长信号?破坏它们能否减缓这一过程?
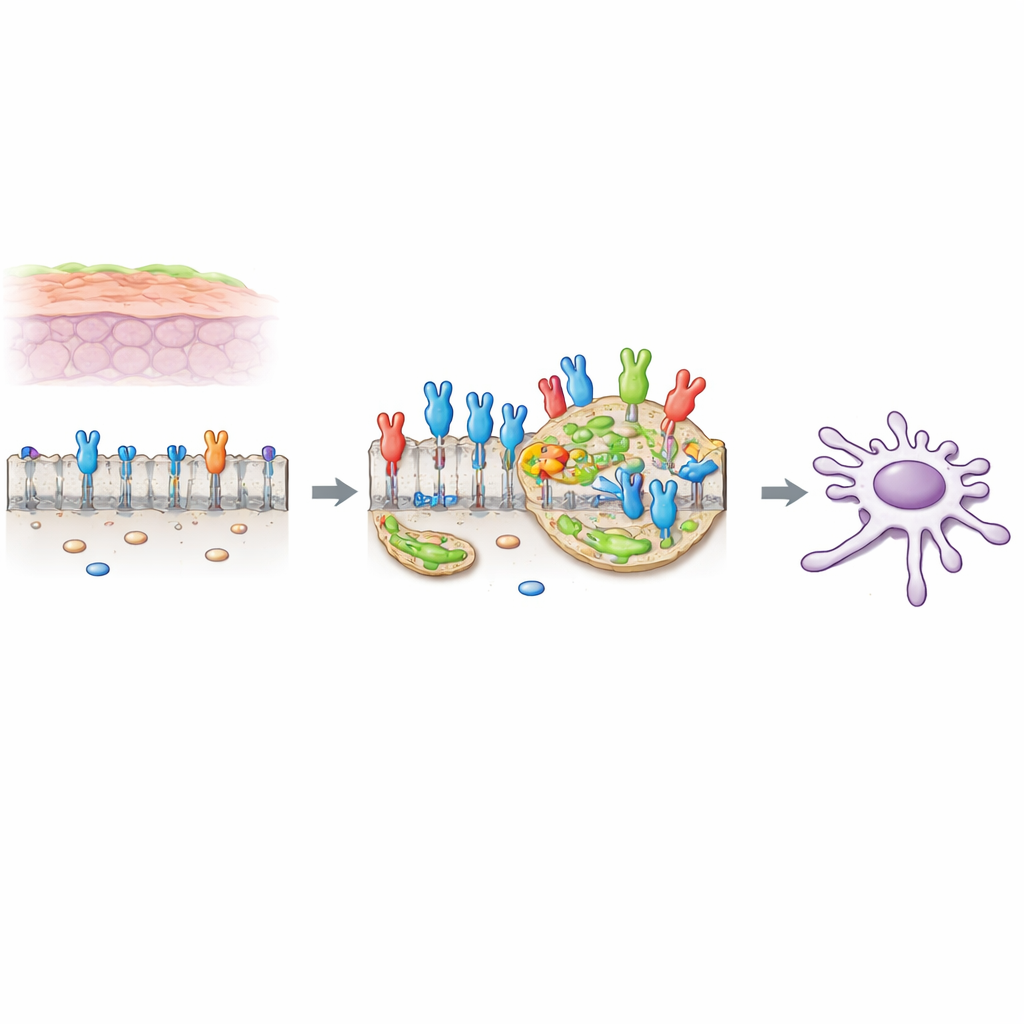
细胞表面的致癌开关
许多细胞在表面携带对生长信号作出反应的开关。其中一种称为FGFR2c的变体通常存在于更具可塑性和迁移性的细胞中,但在胰腺导管腺癌(PDAC)细胞中异常过表达。当该开关被外部配体激活时,会驱动被称为上皮–间质转化(EMT)的变化,使细胞黏附性降低、迁移和侵袭能力增强。作者早期的工作表明,在PDAC细胞中,FGFR2c激活一条涉及PKCε蛋白及若干经典生长通路的信号级联,提升细胞存活、运动和侵袭能力。
富胆固醇“岛屿”作为信号放大器
细胞的外膜并非均一,其中含有富含胆固醇的小斑块,称为脂筏,它们充当微型平台,使信号分子更易聚集与交流。研究人员发现,当FGFR2c被外部信号激活时,更多受体移动到这些脂筏中。通过荧光示踪和生化分级分离,他们显示出活化的FGFR2c在这些斑块中富集,而位于筏外的受体分布则由平滑变为点状,符合受体在这些“岛屿”上聚集的图景。
破坏“岛屿”削弱癌性特征
为测试这些脂筏是否对FGFR2c的致癌效应必不可少,研究团队使用了一种化合物(甲基-β-环糊精),该物质可选择性地从膜中去除胆固醇并破坏脂筏结构,而不致死细胞。在富含FGFR2c的PDAC细胞中,破坏脂筏显著降低了受体下游关键信号分子的激活,并抑制了EMT程序:与迁移、侵袭状态相关的基因和蛋白水平下降,而上皮特征部分恢复。同样的处理也降低了与侵袭相关的蛋白(例如MCL-1、SRC和基质降解酶)的水平,并削弱了癌细胞在模拟周围组织的凝胶中移动和穿透的能力。FGFR2c含量很低的细胞几乎没有反应,强调了该受体与脂筏协同在这些肿瘤中的核心地位。
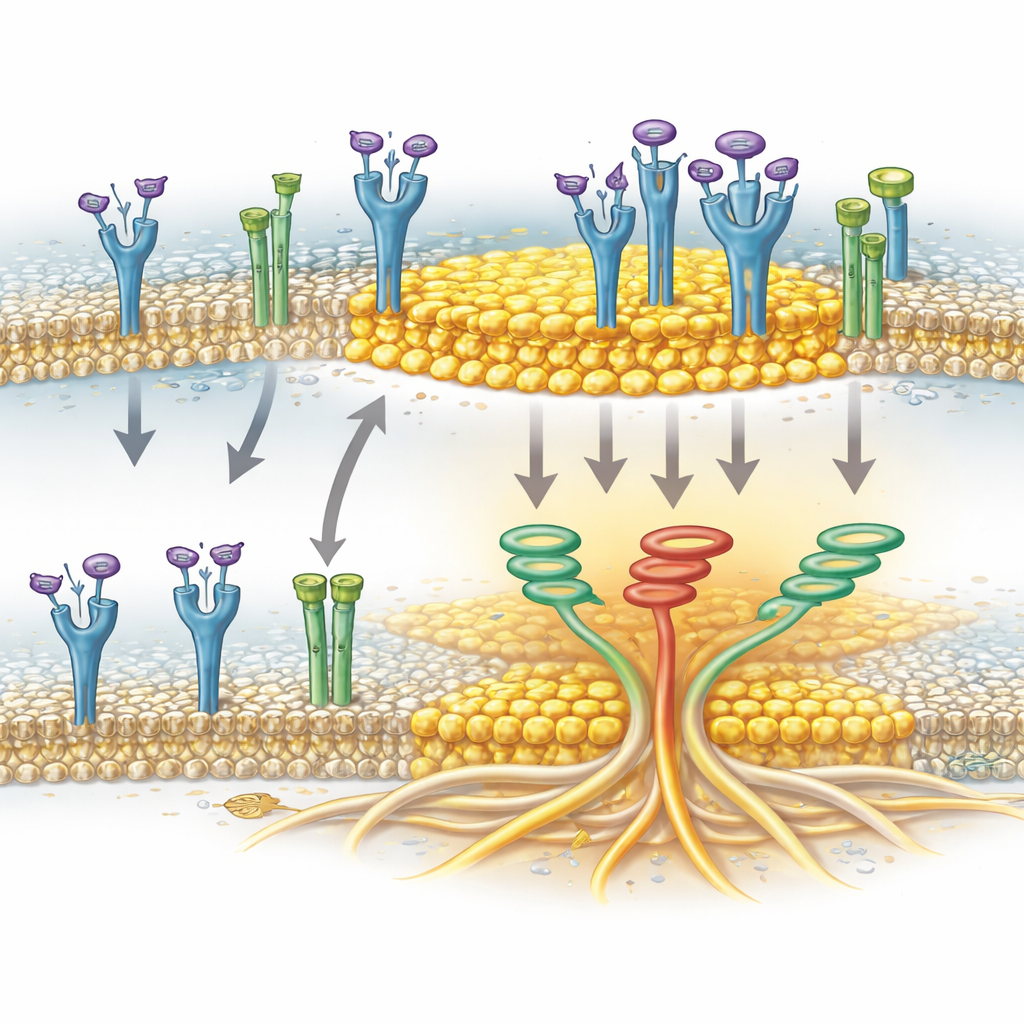
作为聚集助力的离子通道
该研究还发现了一个令人意外的助力者:TRPA1,一种在神经中以感知刺激物和氧化应激著称的通道蛋白。在胰腺癌细胞中,TRPA1存在于膜上并可驻留于脂筏中。作者表明,当FGFR2c被激活时,TRPA1与其发生物理相互作用,并且这种相互作用与FGFR2c在筏区的富集同时出现。当降低TRPA1水平时,尽管脂筏本身仍然存在,活化的FGFR2c不再能有效在脂筏区积聚。这表明TRPA1不仅是被动的“乘客”,而是积极帮助引导或稳定FGFR2c进入这些富含胆固醇的平台,使受体能够更有效地触发促侵袭的信号网络。
对未来治疗的启示
综述来看,研究勾画出FGFR2c、TRPA1与脂筏构成协同单元,共同增强胰腺癌细胞的侵袭性。FGFR2c提供生长信号,脂筏提供信号复合体组装的物理舞台,而TRPA1则协助将受体带到这一舞台上。对非专业读者而言,关键结论是:决定肿瘤危险性的,不仅是致癌分子本身,还有它们所占据的微小膜景观。通过单独或联合靶向FGFR2c、TRPA1或这些富胆固醇“岛屿”的稳定性,未来的治疗或可更精确、肿瘤特异性地削弱胰腺癌细胞的侵袭机制。
引用: Mancini, V., Manganelli, V., Garofalo, T. et al. Role of lipid rafts in the FGFR2c-mediated oncogenic signaling by involvement of TRPA1 channel in pancreatic ductal adenocarcinoma cells. Cell Death Dis 17, 259 (2026). https://doi.org/10.1038/s41419-026-08513-7
关键词: 胰腺癌, 脂筏, FGFR2c, TRPA1通道, 细胞侵袭