Clear Sky Science · zh
OTUD4去泛素化稳定EGFR并激活PI3K/AKT通路以促进三阴性乳腺癌的侵袭性
这项研究为何对乳腺癌重要
三阴性乳腺癌是最难治疗的乳腺癌类型之一,因为它缺乏许多药物可以针对的激素和生长标志物。本研究揭示了一个隐藏的“保护者”分子,帮助癌细胞维持一个强大的生长开关处于开启状态。了解这一看不见的支持体系,可能为切断驱动肿瘤生长与扩散的信号提供新方法。
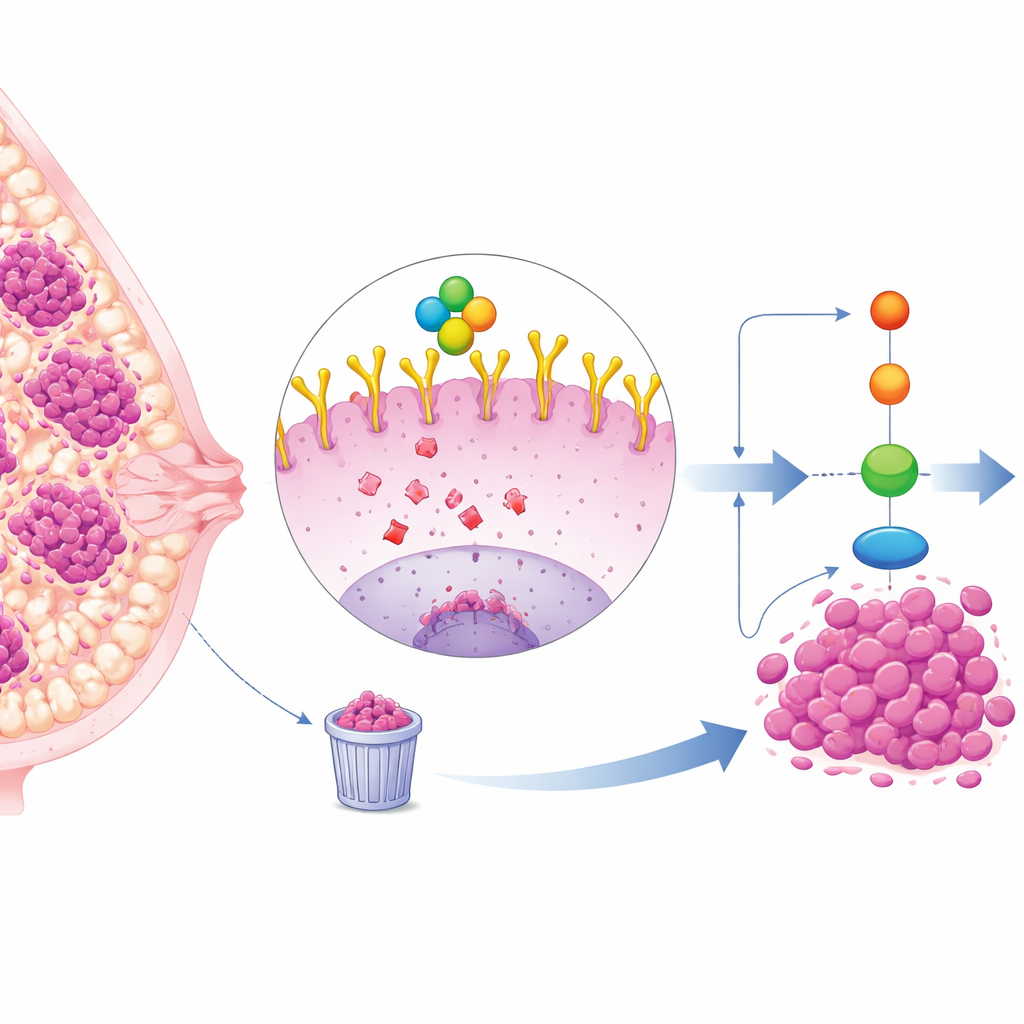
难以治疗的乳腺癌亚型
三阴性乳腺癌(TNBC)约占乳腺癌病例的四分之一,且往往比其他亚型生长和扩散更快。由于TNBC细胞不表达雌激素、孕激素或HER2受体,常规的靶向治疗效果有限,化疗和手术因此仍为主要选择。然而,许多TNBC肿瘤显示出高水平的细胞表面蛋白EGFR,EGFR像天线一样接收生长和存活信号。EGFR水平升高与预后不良相关,但直接阻断EGFR的药物在临床上效果令人失望,这提示存在更深层次的调控机制。
发现肿瘤生长的隐秘助手
研究人员将注意力集中在OTUD4上,这是一种从其他蛋白上切除小蛋白标记(泛素)的酶。这些标记常常充当处置信号,将蛋白标记为应被降解,因此去除它们可以稳定并保护被标记的蛋白。通过分析大型癌症数据库和患者组织样本,团队发现OTUD4在TNBC肿瘤和细胞系中的表达高于正常乳腺组织。肿瘤中OTUD4较高的患者通常生存较差,提示OTUD4表现出类似癌基因的特性,促进癌症进展。
OTUD4如何使癌细胞更具侵袭性
为评估OTUD4在TNBC细胞中的实际作用,科学家在两种广泛研究的TNBC细胞系中降低了其表达。当敲低OTUD4时,癌细胞增殖变慢、克隆形成减少,并在伤口愈合和Transwell迁移实验中迁移能力下降,这些都是侵袭性降低的迹象。相反,过表达OTUD4会导致细胞增殖更快、迁移能力增强,进一步支持OTUD4推动恶性行为的观点。在小鼠体内,由缺失OTUD4的细胞形成的肿瘤生长更慢,并表现出较少的细胞分裂和生长信号标志,证实了这些在有机体中的作用。
保护EGFR的分子盾牌
在机制研究中,团队通过蛋白相互作用筛选和生化检测鉴定出EGFR是OTUD4的直接结合伙伴。他们发现OTUD4结合EGFR的特定区域并切除K48连接的泛素链,这类泛素通常将蛋白标记为被细胞回收系统降解。当降低OTUD4时,EGFR降解更快,而其基因表达水平并未改变,表明OTUD4作用于EGFR翻译后阶段,而非DNA或RNA水平。阻断细胞的蛋白质降解系统可以恢复EGFR水平,强调关键步骤是防止被降解。细胞表面EGFR更稳定后,一个主要的内部信号通路——PI3K/AKT/mTOR通路——持续被开启,从而驱动细胞生长和存活。
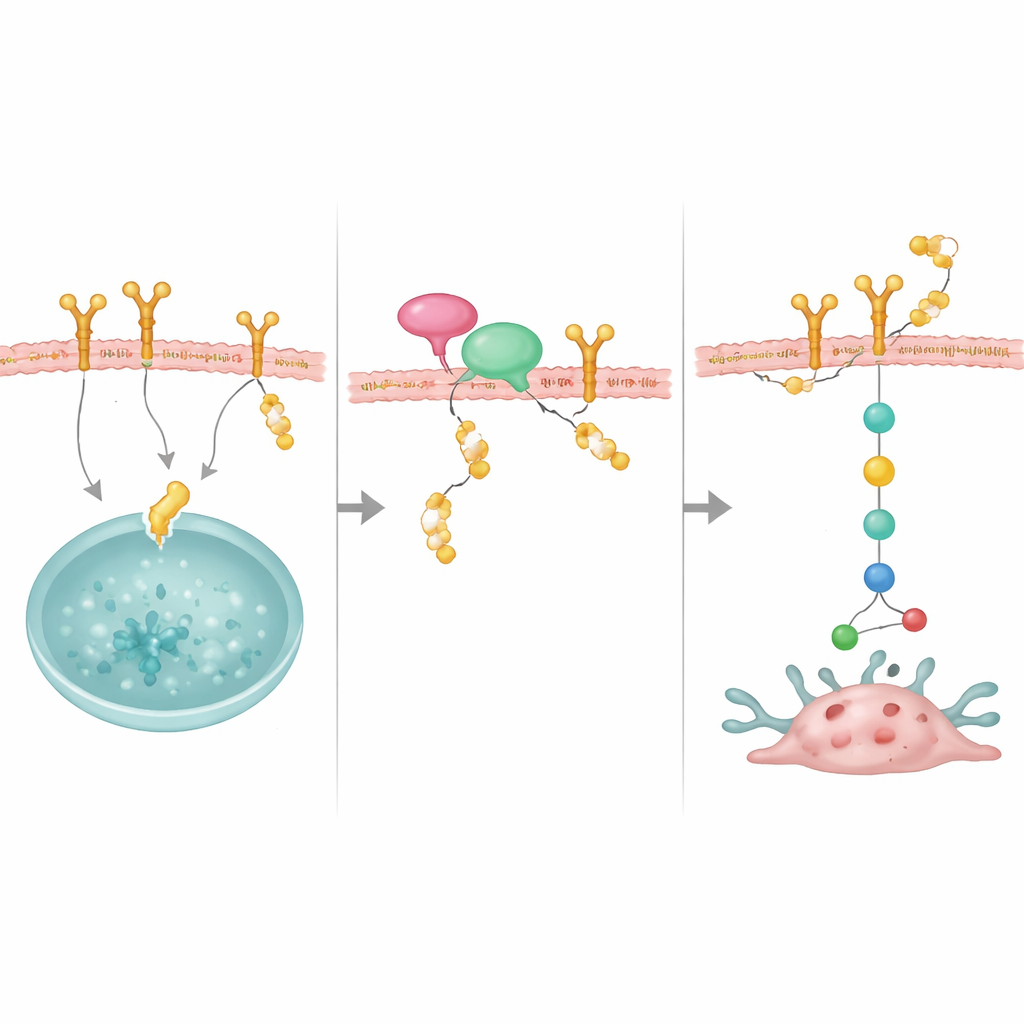
将保护者带到目标处的连接子
研究还发现了一个重要的伙伴NRP1,这是一种先前与侵袭性乳腺癌相关的膜蛋白。NRP1同时与OTUD4和EGFR结合,帮助将OTUD4定位到位以挽救EGFR免于被破坏。当降低NRP1时,EGFR变得不稳定且生长信号减弱,尽管OTUD4水平未发生变化。过表达OTUD4可以部分弥补NRP1丧失的影响,提示NRP1像停靠平台一样招募OTUD4到EGFR。这些分子共同形成一个稳定复合体,使EGFR在细胞表面保持充足。
对未来治疗的意义
通过揭示OTUD4与NRP1如何协同保护EGFR免遭降解,本研究确定了三阴性乳腺癌中一个关键生长信号的新调控点。与其直接阻断EGFR的活性位点,未来的治疗策略可能旨在破坏OTUD4的保护作用或阻断其被NRP1招募,从而降低EGFR水平并抑制驱动肿瘤生长的PI3K/AKT通路。尽管仍需更多工作来寻找安全有效的OTUD4抑制剂并了解癌细胞可能采取的逃逸路径,但这些发现为对抗这一棘手乳腺癌亚型提供了有前景的更精确治疗途径。
引用: Ren, Y., Zhou, F., Tan, Z. et al. OTUD4 deubiquitination stabilizes EGFR and activates the PI3K/AKT pathway to promote the invasiveness of triple-negative breast cancer. Cell Death Dis 17, 245 (2026). https://doi.org/10.1038/s41419-026-08482-x
关键词: 三阴性乳腺癌, EGFR信号, OTUD4, PI3K AKT通路, 蛋白质降解