Clear Sky Science · zh
靶向融合蛋白FUS:治疗特发性肺纤维化的新型反义策略
为何肺部瘢痕重要
特发性肺纤维化(IPF)是一种无情的肺部疾病,细小的气囊逐渐被僵硬的瘢痕组织取代,使每一次呼吸都变得困难。现有药物可以减慢瘢痕的进展,但无法阻止或逆转这一过程。本研究探讨了一个名为FUS的新靶点——一种帮助细胞处理遗传信息的蛋白——并测试是否可用一种设计性的类DNA短链将其关闭,从而抑制瘢痕形成并帮助受损肺组织自我修复。
失控的细胞交通指挥官
FUS通常位于细胞核内,参与管理RNA(基因的工作拷贝)如何被加工和利用。在如ALS等脑部疾病中,FUS会异常行为,离开细胞核,在细胞质中聚集,干扰正常功能。作者提出疑问:类似的异常行为是否也会驱动IPF中的瘢痕形成。他们研究了来自IPF患者和健康供体的肺成纤维细胞——这些结缔组织细胞负责沉积瘢痕物质。在IPF细胞中,FUS总体水平更高,且关键在于,细胞质中的FUS远多于健康细胞。通过高分辨率电子显微镜,他们确认该蛋白在细胞核外异常丰富,暗示其对RNA的正常调控在纤维化肺组织中可能被扭曲。 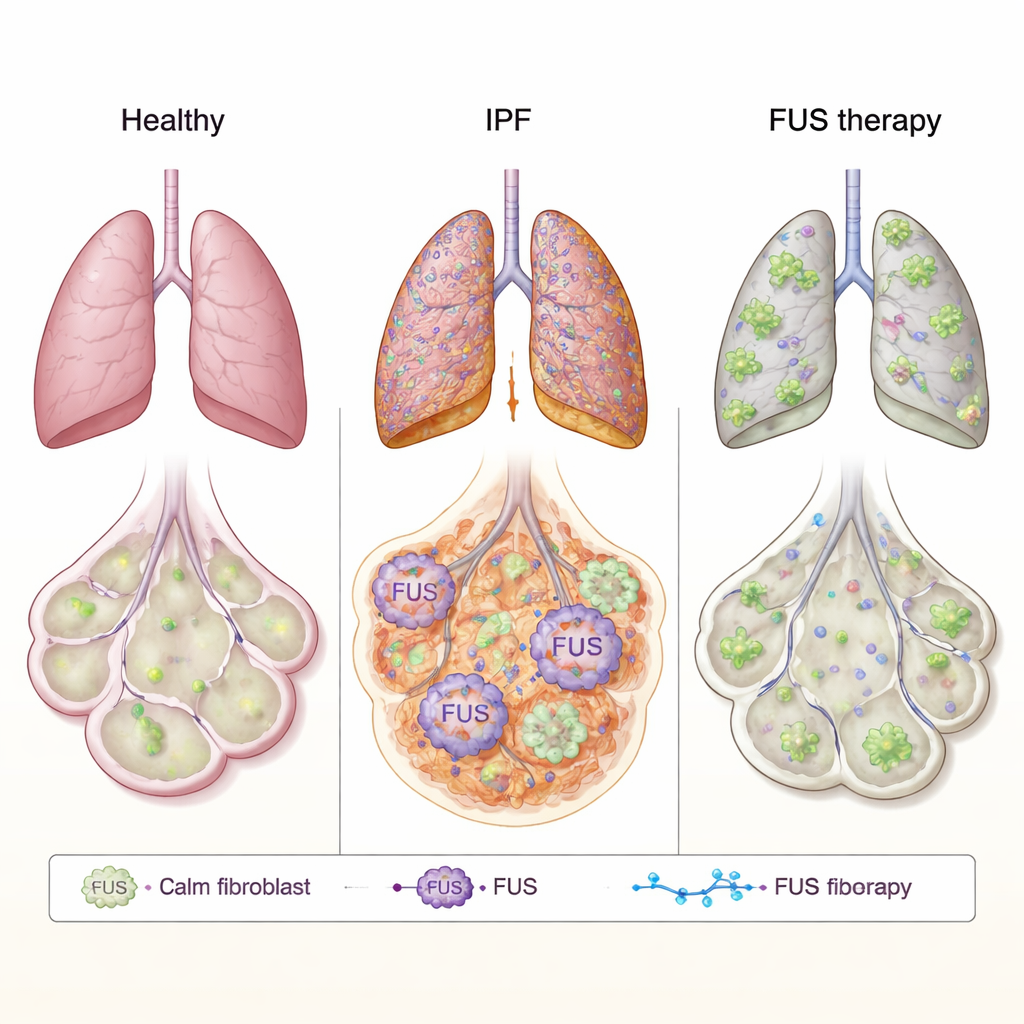
FUS如何助长纤维形成细胞
为弄清该异常蛋白的实际作用,研究者在健康成纤维细胞中增强FUS表达,并在IPF成纤维细胞中降低其水平。额外的FUS促使健康细胞分裂加快,而在IPF细胞中降低FUS则减缓了其增殖和迁移——这两种行为均是瘢痕形成的核心。团队还使用了一种“冻结”蛋白–RNA结合并识别与FUS结合的RNA的技术。在IPF成纤维细胞中,FUS被发现与许多促进纤维化的遗传信息紧密结合,包括编码胶原、像TGF‑β这样的生长因子以及炎症信号。换言之,FUS充当了连接一整套促瘢痕信息的枢纽。
用精准药物沉默信号
研究测试了一种名为ION363的反义寡核苷酸——一种短小、化学修饰的链条,旨在与FUS的RNA结合并触发其降解。当用ION363处理IPF成纤维细胞时,FUS水平下降,细胞增殖和迁移减慢,关键的构瘢痕基因被压低。重要的是,这种效应并非通过杀死细胞或强迫其进入衰老状态来实现;相反,似乎是重置了它们的行为。当相同处理施用于在体外维持活性的IPF肺组织薄片时,与细胞外基质、炎症和异常上皮相关的大量基因被抑制,而与健康表面活性物质生成和肺泡功能相关的基因则上调。该治疗还减少了胶原染色并增加了功能性肺表面细胞的标志物,表明组织从瘢痕化向修复方向转变。
助力受损气囊再生
鉴于被称为II型肺泡细胞的小型气囊衬里细胞对肺修复至关重要,研究者用患者细胞构建了三维“肺泡球”以模拟微型肺单元。在IPF患者的培养物中,这些结构通常存活不良。经ION363处理后,更多肺泡球形成、体积更大,并显示出更高的溶酶体活性——这是活跃更新的标志。详细染色显示具有成熟气体交换细胞标志的细胞更多,表明沉默FUS不仅抑制了成纤维细胞的过激行为,也鼓励受损上皮重建更健康的表面。 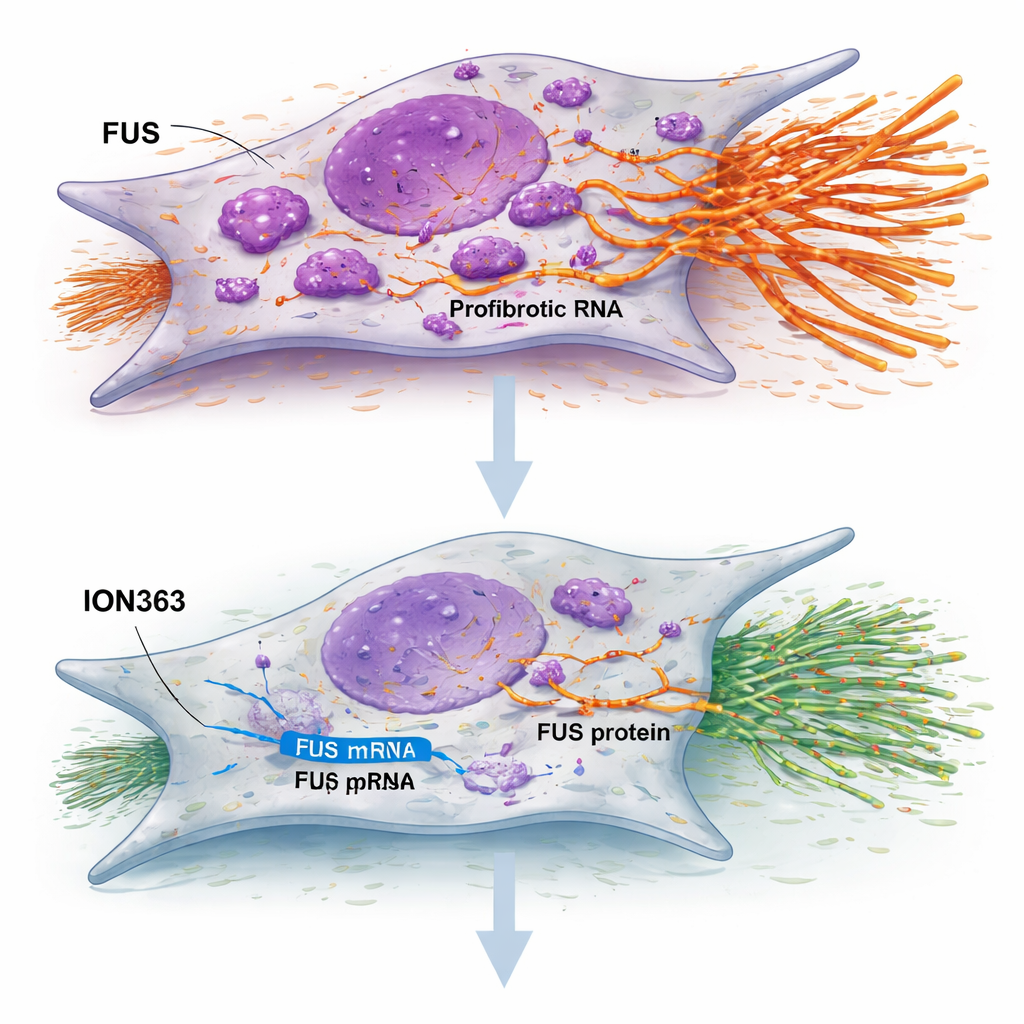
这对病人意味着什么
综合来看,这项工作将FUS描绘为IPF中的一个主开关,连接了过度活跃的成纤维细胞与无法修复的细小气囊。通过用有针对性的反义药物下调FUS,研究者能够抑制促纤维化的基因程序、缓解胶原堆积并在患者来源的肺模型中促进再生。尽管这一方法仍处于实验室阶段,需要在动物模型和临床试验中进行谨慎验证,但它表明未来IPF的治疗可能不仅仅是减慢瘢痕形成,而是通过直接重新平衡控制肺损伤与修复的细胞程序来修复肺功能。
引用: Katariya, B.B., Chillappagari, S., Arnold, L. et al. Targeting fused in sarcoma (FUS): a novel antisense strategy for treating idiopathic pulmonary fibrosis. Sig Transduct Target Ther 11, 70 (2026). https://doi.org/10.1038/s41392-026-02585-9
关键词: 特发性肺纤维化, 反义寡核苷酸, FUS 蛋白, 肺纤维化, 肺泡修复