Clear Sky Science · tr
Tümöre özgü HORMAD1 ifadesi mitotik arresti bozar ve mitotik kinaz inhibitörlerine duyarlılık yaratır
Kanser tedavisi için neden önemli
Hücrelerimiz çoğalırken doğru kromozom setini aktarmak için karmaşık güvenlik kontrollerine güvenirler. Kanser sıklıkla bu koruyucu mekanizmaları kaçırır veya zayıflatır; bu durum, hem hastalığı ilerleten hem de tümörlerin ilaçlara yanıtını belirleyen kaotik genomlara yol açar. Bu çalışma, normalde yalnızca üreme hücrelerinde aktif olan HORMAD1 adlı alışılmadık bir proteinin birçok agresif meme kanseri ve diğer bazı tümörlerde etkinleştiğini ortaya koyuyor. HORMAD1, hücre bölünmesinin önemli bir kontrol noktasını ince bir şekilde sabote ederek kanser hücrelerini daha istikrarsız hale getiriyor—ancak aynı zamanda bu hücreleri deneysel bir ilaç sınıfına karşı beklenmedik derecede savunmasız kılıyor.
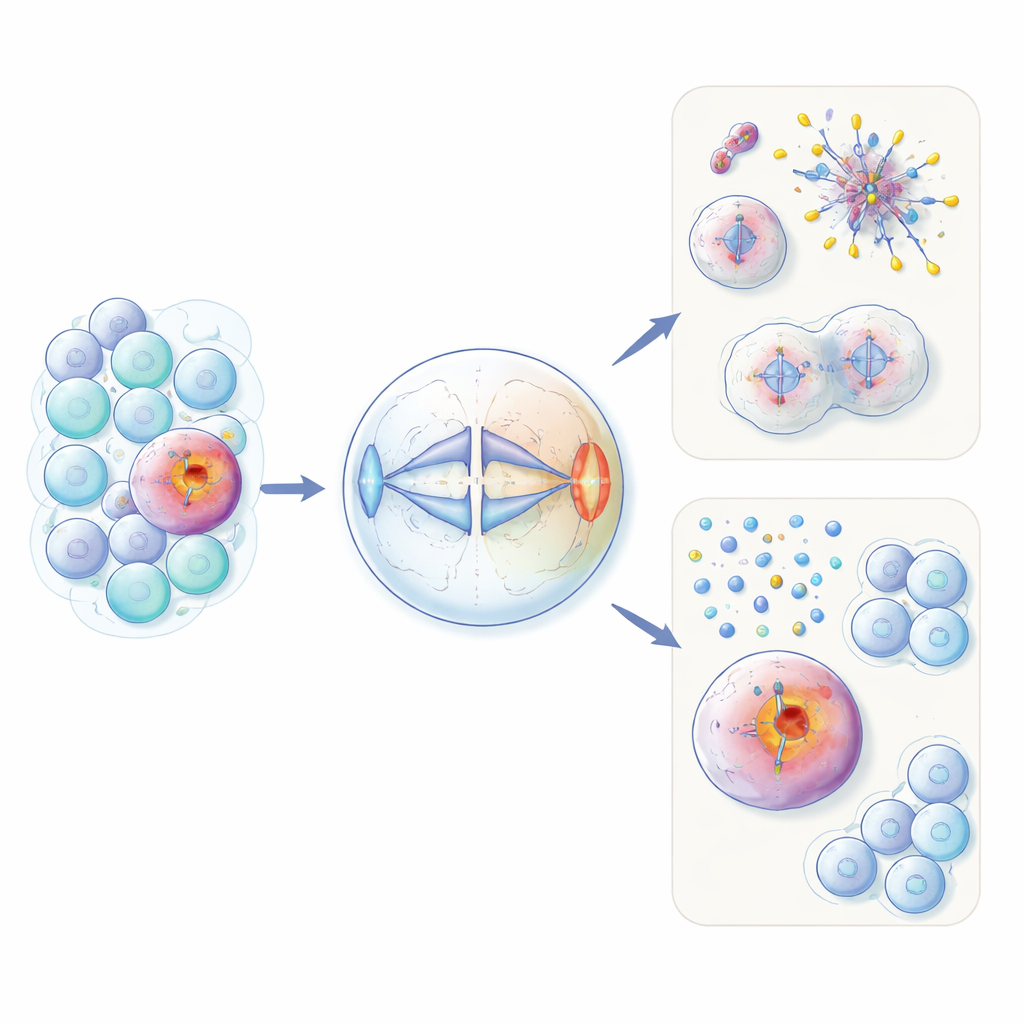
Kanser hücrelerinde yanlış yerde açığa çıkan bir üreme proteini
HORMAD1 normalde yalnızca yumurta ve sperm yapılan germ hücrelerinde görülür. Orada, mayoz adı verilen özel bölünme sırasında DNA yeniden düzenlemesini ve kalite kontrolünü yönetmeye yardımcı olur. Yazarlar, üçlü negatif meme kanserlerinin yaklaşık %60’ında—ve birkaç diğer tümör tipinin alt kümelerinde—bu proteinin uygunsuz şekilde yeniden açıldığını gösteriyor. Hem mühendislik yapılan kansersiz hücrelerde hem de kanser hücre hatlarında, fazladan HORMAD1’in normal hücre bölünmesi sırasında kromozomların eşit ayrılmasını bozduğunu buldular. HORMAD1 ifade eden hücreler daha fazla geciken kromozom, fazladan veya eksik kromozomlar (aneuploidy) ve küçük DNA içeren “mikronükleerere” sahip oldu; bunların tümü agresif kanserlerde görülen genomik kargaşanın ayırt edici işaretleridir.
Hücre bölünmesi güvenlik kontrolleri normalde nasıl çalışır
Doğru bölünmek için bir hücre, her kromozoma bağlanan mikrotübül liflerinden oluşan bir iğ yapısı kurar. İğ montaj kontrolü (spindle assembly checkpoint) olarak bilinen gözetim sistemi, gerilime duyarlı bir fren gibi davranır: herhangi bir kromozom düzgün bağlanmamışsa fren ilerlemeyi engeller ve hatalar giderilene kadar ayrılmayı durdurur. MPS1, Aurora B ve BUB1 dahil olmak üzere birkaç mitotik kinaz, kötü bağlantıları algılamaya yardımcı olur ve her yavru hücrenin doğru kromozom setini almasını sağlamak için “hata düzeltme”yi teşvik eder. Bu sistemin bozulması hem kanser gelişimini besleyebilir hem de belirli ilaçların hedefleyebileceği özel zayıflıklar yaratabilir.
HORMAD1 fren sistemini sessizce zayıflatıyor
Araştırmacılar HORMAD1’in bu güvenlik frenini ince ama önemli bir şekilde zayıflattığını keşfettiler. Klasik kontrol noktası bileşenleri olan HORMA proteini MAD2L1 gibi yapılarla doğrudan etkileşime girmemek yerine, HORMAD1 kinaz Aurora B’ye doğrudan bağlanır. Aurora B normalde tam aktif hale gelmek ve sentromerler ile kinetokorlardaki hedef proteinleri modifiye etmek için INCENP adlı başka bir proteinle ortaklık kurar—bu bölgeler, iğ liflerinin kromozomlara bağlandığı kritik noktalardır. Bölünen tümör hücrelerinde HORMAD1 bulunduğunda, HORMAD1 INCENP ile Aurora B arasındaki erişim için rekabet eder; bu ortaklığı azaltır ve Aurora B aktivitesini baskılar. Sonuç olarak, Aurora B’nin birkaç hedef üzerindeki fosforilasyon sinyalleri zayıflar, hata düzeltme daha az etkili olur ve kontrol noktası ‘sızgan’ hale gelir: hücreler hatalı bağlantılar olsa bile mitozu çok erken sonlandırır, bu da yanlış ayrışmış kromozomlara ve genomik istikrarsızlığa yol açar.
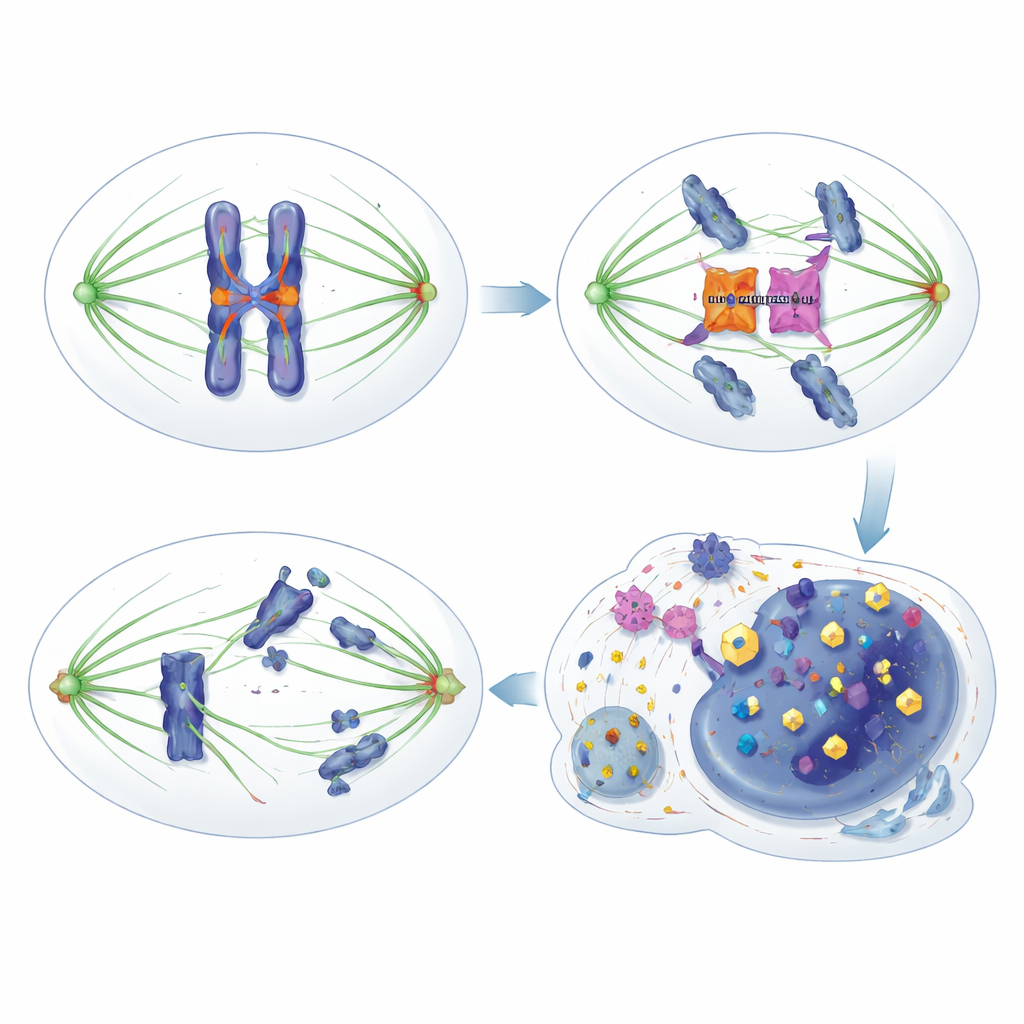
Zayıflıktan terapötik fırsata
HORMAD1 yalnızca Aurora B ve ilgili koruyucuları kısmen devre dışı bıraktığı için, kanser hücreleri büyümek için yeterince hayatta kalmaya devam eder, ancak tekrar eden hatalı bölünmelerde hayatta kalmak için mitotik kinazların kalan işlevine güçlü şekilde bağımlı hale gelir. Ekip bunu, HORMAD1-pozitif ve HORMAD1-negatif hücreleri MPS1, Aurora B ve BUB1’in deneysel inhibitörlerine maruz bırakarak test etti. Birçok modelde HORMAD1 ifadesi hücreleri bu ilaçlara karşı çok daha hassas hale getirdi ve proliferasyonlarını veya koloni oluşturma yeteneklerini dramatik şekilde azalttı. BUB1’in genetik olarak düşürülmesi, yalnızca HORMAD1 varlığında özellikle öldürücü oldu ve güçlü, seçici bir bağımlılığı ortaya koydu. Hasta kaynaklı üçlü negatif meme tümörleri kullanan fare modellerinde, yüksek HORMAD1 düzeyine sahip olan tümörler Aurora B inhibitörünün nanoparçacık formülasyonu ile tedavi edildiğinde küçüldü veya daha yavaş büyüdü; oysa HORMAD1-negatif tümörler aynı tedaviye büyük ölçüde direnç gösterdi.
Hastalar için ne anlama geliyor
Genel gözlemci için HORMAD1 kanserde çift uçlu bir kılıç gibi iş görür: tümör hücrelerini daha büyük kromozomal düzensizliğe iterek hastalığı ilerletebilir, ancak bunu yaparken onları birkaç kalan hücre bölünmesi koruyucusuna aşırı bağımlı hâle getirir. Çalışma, bu yanlış yerde etkinleşmiş üreme proteininin Aurora B’yi yanlış yönlendirerek önemli bir kontrol noktasını zayıflattığını ve HORMAD1-pozitif tümörleri Aurora B, MPS1 veya BUB1’i hedef alan ilaçlara karşı özellikle savunmasız bıraktığını gösteriyor. HORMAD1 normal dokularda büyük ölçüde yokken belirli bir kanser alt kümesinde bulunması, bu proteinin bu gelişmekte olan mitotik kinaz inhibitörlerinden muhtemel fayda sağlayacak hastaları tanımlamak için bir biyobelirteç olarak kullanılabileceğini öne sürüyor ve üçlü negatif meme kanseri gibi tedavisi zor kanserler için yeni hedefli tedavi yolları açma potansiyeli taşıyor.
Atıf: Walker, C., Kollarovic, G., Weekes, D. et al. Tumour specific HORMAD1 expression perturbs mitotic arrest and drives sensitivity to mitotic kinase inhibitors. Nat Commun 17, 2157 (2026). https://doi.org/10.1038/s41467-026-69561-3
Anahtar kelimeler: HORMAD1, üçlü negatif meme kanseri, kromozomal istikrarsızlık, Aurora B kinaz, mitotik kontrol noktası inhibitörleri