Clear Sky Science · tr
MYC ve KRAS’ın hedefe yönelik parçalanması için heterobifonksiyonel proteomimetik polimerler
Kanserin en zorlu proteinlerini devirmek için yeni araçlar
MYC ve KRAS gibi en tehlikeli kanser sürücü proteinlerin birçoğu, ilaçların kolayca tutunamaması nedeniyle uzun süredir “ilaçlanamaz” olarak sınıflandırıldı. Bu çalışma, bu kaygan proteinleri yakalayıp hücrenin çöp imha sistemiyle buluşturabilen bir tür yumuşak, sentetik malzeme—HYDRAC polimerleri—sunuyor. Okuyucular için bu çalışma, kimya ve nanoteknolojinin geleneksel ilaçlara dirençli kanserler için yeni tedavi seçenekleri açabileceğine dair bir pencere aralıyor.
Tek bir hap yerine esnek bir iskelet
Çoğu hedefe yönelik kanser ilacı, bir anahtarın kilide girmesi gibi bir proteinin yüzeyindeki ceplere uyan küçük moleküllerdir. Ancak MYC gibi proteinler gevşek yapıya sahip olup iyi ceplere sahip değildir, KRAS ise klasik ilaçları etkisiz kılan mutasyonlar geliştirebilir. Yazarlar bunun yerine tekrarlayan birimlerden oluşan uzun, zincir benzeri polimerler tasarladı. Bu zincirler boyunca iki tür bileşen takıldığında: MYC veya RAS gibi hedefleri tanıyan kısa protein-bağlayıcı segmentler ve hücrenin kendi imha mekanizmasını çağıran “degron” segmentleri. Her bileşenin zincir üzerinde birçok kopyasının bulunması sayesinde tek bir HYDRAC molekülü aynı anda birden çok protein ve enzime ulaşabilir; bu, tek ve sert bir ilaç molekülüyle başarması zor bir şeydir.
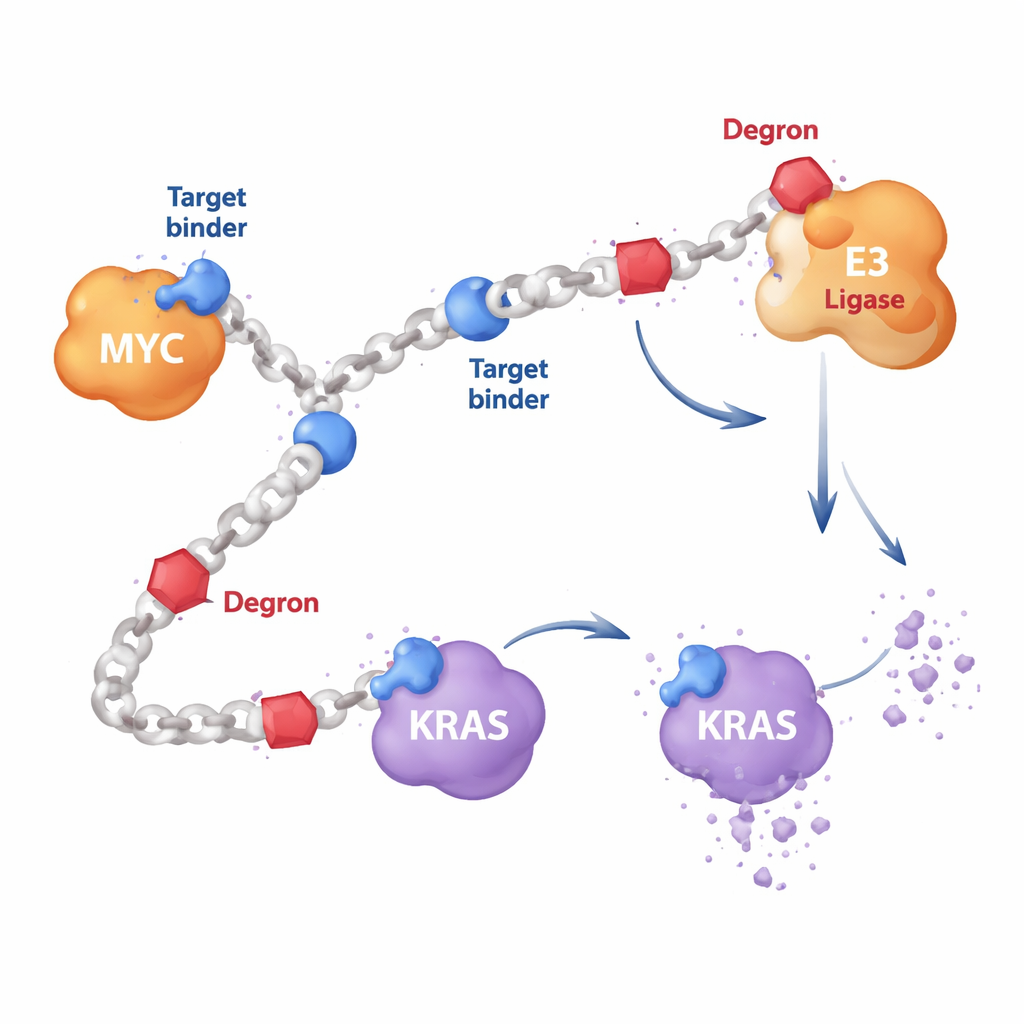
Hücrelere MYC’i parçalatmayı öğretmek
İlk bir test olarak araştırmacılar, onlarca yıldır doğrudan saldırıya direnç gösteren fakat birçok kanserde büyümeyi yöneten bir anahtar anahtar regülatör olan MYC’e odaklandı. Bilinen bir MYC-bağlayıcı peptidi ve proteini hücrenin ana protein öğütücüsü olan proteazoma işaretleyen basit bir degron motifi gösteren HYDRAC polimerleri inşa ettiler. Deney tüpü deneylerinde bu polimerler kompakt, protein benzeri şekillere katlanıp MYC’e sıkı bağlanırken ilgisiz proteinlere bağlanmadı. Kanser hücrelerinde HYDRAC’lar kolayca hücrenin içine girdi, MYC kontrollü gen programlarını bozdu ve hücre ölümünü tetikledi—bu etkiler, hedefleme ve degron bileşenlerinin aynı polimer zinciri üzerinde birlikte bulunmasına bağlıydı.
Hücre kültüründen tümörlerin küçülmesine
Hücre içinde HYDRAC tedavisi MYC protein düzeylerinde keskin düşüşlere neden oldu ancak MYC’in RNA’sını azaltmadı; bu, basit bir kapatma değil gerçek bir parçalanma olduğunu gösteriyor. Proteazomu veya belirli parçalanma yollarını etkinleştiren anahtar enzimleri bloke etmek MYC düzeylerini kurtardı; bu da polimerlerin hücrenin kendi atık-bertaraf sistemlerini yeniden yönlendirerek çalıştığını gösteriyor. Proteom çapında analizler çok az sayıda diğer proteinin etkilendiğini ortaya koydu; bu da dikkat çekici bir seçiciliği işaret ediyor. MYC kaynaklı tümörlerin bulunduğu fare modellerinde, floresan işaretli HYDRAC’lar enjeksiyondan sonra tercihen tümörlerde birikti ve günlerce orada kaldı. Tekrarlayan dozlama tümör büyümesini yavaşlattı; önemli kilo kaybı veya belirgin doku hasarı olmadı ve tümör örnekleri daha az bölünen hücre ve daha fazla programlı hücre ölümü belirtisi gösterdi.
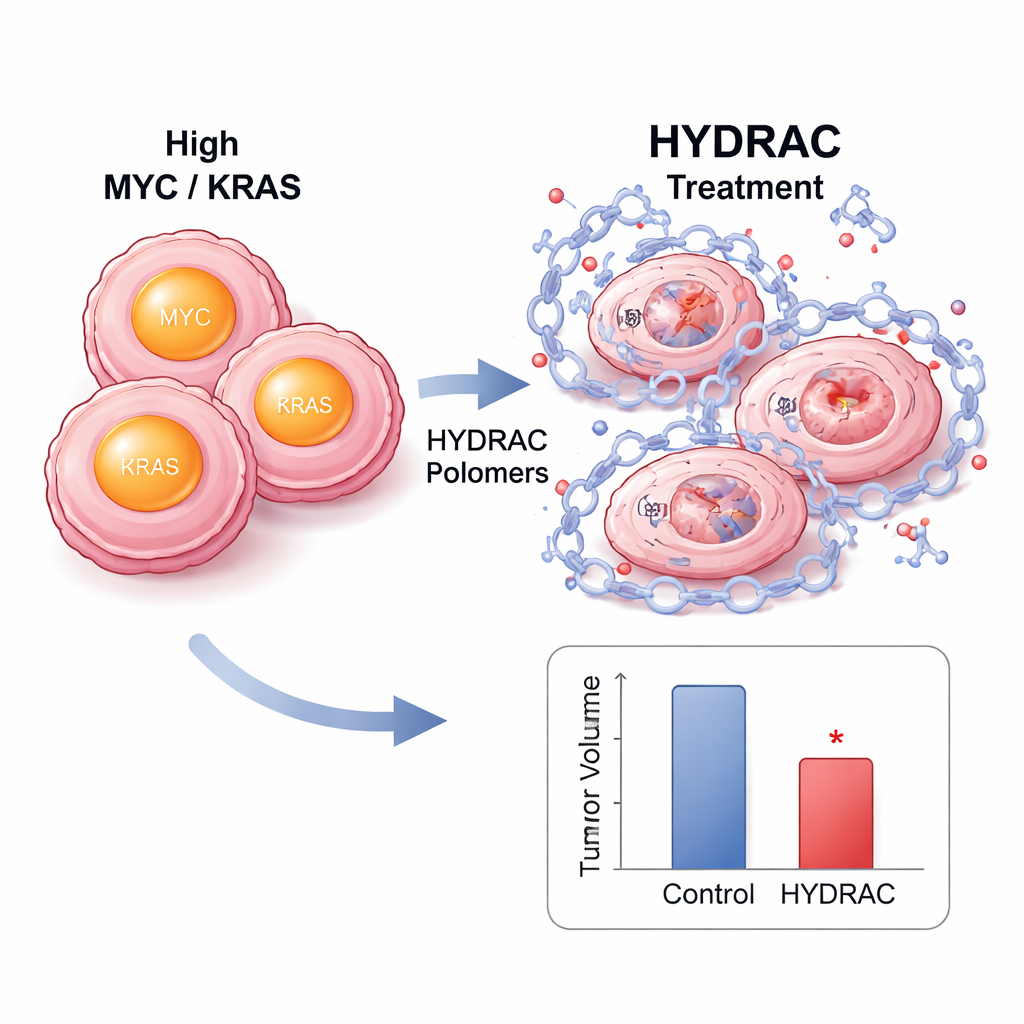
Birçok hastalık hedefi için tak-çalıştır platformu
HYDRAC yaklaşımının güçlü yönlerinden biri, yan gruplarının değiştirilebilir parçalar gibi yer değiştirilebilmesidir. Ekip, orijinal degronu başka hücresel enzimleri çağıran farklı işe çağırıcı elementlerle değiştirdi; bunlar arasında talidomidin tanıdığı enzimleri çağıranlar da vardı. Her versiyon yalnızca amaçlanan enzim mevcut ve işlevsel olduğunda MYC’i parçaladı; bu da polimerlerin farklı hücresel yolları kullanacak şekilde ayarlanabileceğini doğruladı. Genellik test etmek için araştırmacılar daha sonra RAS proteinlerini tanıyan bir peptidi kullanarak RAS-hedefleyen HYDRAC’lar yaptılar. Bu yapıların iki farklı kanser hücre hattında mutant KRAS’ı başarıyla parçaladığı görüldü; bu, belirli bir mutasyona bağlı olmayan “pan-KRAS” potansiyeline işaret ediyor—çok sayıda KRAS varyantının bir arada bulunduğu kanserler için önemli bir adım.
Geleceğin kanser bakımında bunun önemi
Bu çalışma HYDRAC’ları sadece sorunlu proteinleri engellemeyen, aynı zamanda hücrelerin onları silmesine yardımcı olan programlanabilir bir malzeme sınıfı olarak tanıtıyor. Esnek bir polimer üzerinde birçok hedefleme ve parçalanma birimini birleştirerek HYDRAC’lar, tipik olarak yalnızca birer tane taşıyabilen geleneksel küçük moleküllü ilaçlar ve PROTAC’ların tasarım sınırlarının ötesine geçiyor. Bu malzemelerin klinik kullanıma ulaşmasına kadar yapılması gereken çok iş olsa da, MYC ve KRAS kaynaklı modellere ilişkin sonuçlar, uzun süre “ilaçlanamaz” kabul edilen kanser proteinlerinin aslında, tıp tek bir küçük hap gibi değil de özel yapılmış bir moleküler fırça gibi yaklaştığında savunmasız olabileceğini öne sürüyor.
Atıf: Wang, M.M., Truica, M.I., Gattis, B.S. et al. Heterobifunctional proteomimetic polymers for targeted degradation of MYC and KRAS. Nat Commun 17, 1706 (2026). https://doi.org/10.1038/s41467-026-68913-3
Anahtar kelimeler: hedefe yönelik protein parçalanması, MYC, KRAS, polimer terapötikleri, kanser nanomedisini