Clear Sky Science · tr
Alzheimer Hastalığı beyinlerinin bütünleyici epigenomik haritası, tau ile ilişkili oligodendrosit moleküler bozulmalarını ortaya koyuyor
Bu beyin araştırmasının önemi
Alzheimer hastalığı en çok hafıza kaybı ve beyinde biriken iki problemli protein olan amiloid ve tau ile bilinir. Ancak Alzheimer’lı kişiler aynı tanıyı paylaşsalar bile hasar desenleri oldukça farklı olabilir. Bu çalışma temel bir soruyu soruyor: bu zararlı proteinlerin ne kadar biriktiğini ve farklı hücre tiplerini nasıl etkilediğini belirlemede beyin hücrelerindeki hangi anahtarlar rol oynuyor? Yüzlerce beyindeki DNA üzerindeki kimyasal işaretleri inceleyerek araştırmacılar tau ile beynin kablolamasını sağlayan hücreler arasında şaşırtıcı bir bağlantı ortaya çıkarıyorlar.
Gizli anahtarlar olarak DNA üzerindeki kimyasal işaretler
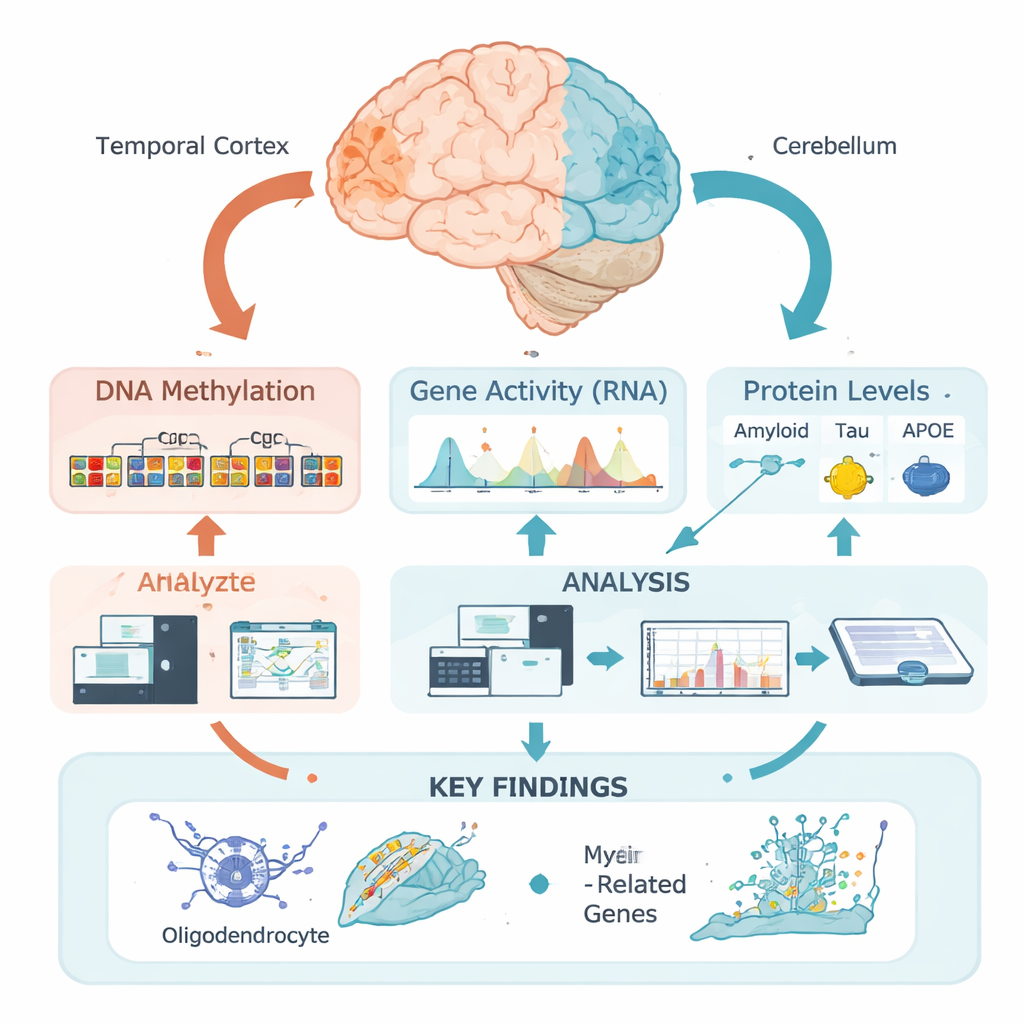
DNA’mız, beyin hücrelerini inşa etmek ve çalıştırmak için temel talimatları taşır; ancak bu talimatlar epigenetik işaretler—genetik kodu değiştirmeden yakınlardaki genleri açıp kapatabilen kimyasal etiketler—tarafından yönetilir. En önemli işaretlerden biri, küçük kimyasal grupların belirli DNA bölgelerine bağlandığı DNA metilasyonudur. Bu ekip tek tek bölgeleri izole şekilde incelemek yerine yeni bir “bölgesel” yaklaşım kullandı: temporal korteks (Alzheimer’da ağır etkilenen bir bölge) ve nispeten korunmuş olan beyincikte DNA’nın paketlenme şeklini temel alarak yakın bölgeleri işlevsel zonlarda gruplayıp bunların değişimini hastalık özellikleriyle ilişkili biçimde sordu. Bu, biyolojik açıdan metilasyon desenlerinin nerede değiştiğini saptamalarına olanak verdi.
DNA işaretlerini Alzheimer proteinleriyle ilişkilendirmek
Araştırmacılar, ölüm sonrası Alzheimer tanısı konmuş 472 kişiden alınan beyin dokularını analiz etti. Her temporal korteks örneği için farklı biyokimyasal formlarda amiloid, tau ve APOE proteinlerinin ayrıntılı düzeylerini ve klasik mikroskopik amiloid plak ve tau yumak skorlarını ölçtüler. Ardından bölgesel DNA metilasyon düzeylerinin bu ölçümlerle ilişkisinin olup olmadığını test eden epigenom çapında ilişki çalışmalarını gerçekleştirdiler. Çarpıcı biçimde, buldukları güçlü ilişkilerin neredeyse tamamı amiloide değil tauya bağlıydı—özellikle toplam çözünür tau ve zarla ilişkili, fosforile olmuş (kimyasal olarak modifiye) ve özellikle toksik olduğuna inanılan form ile.
Beyin kablolama hücrelerinde güçlü bir sinyal
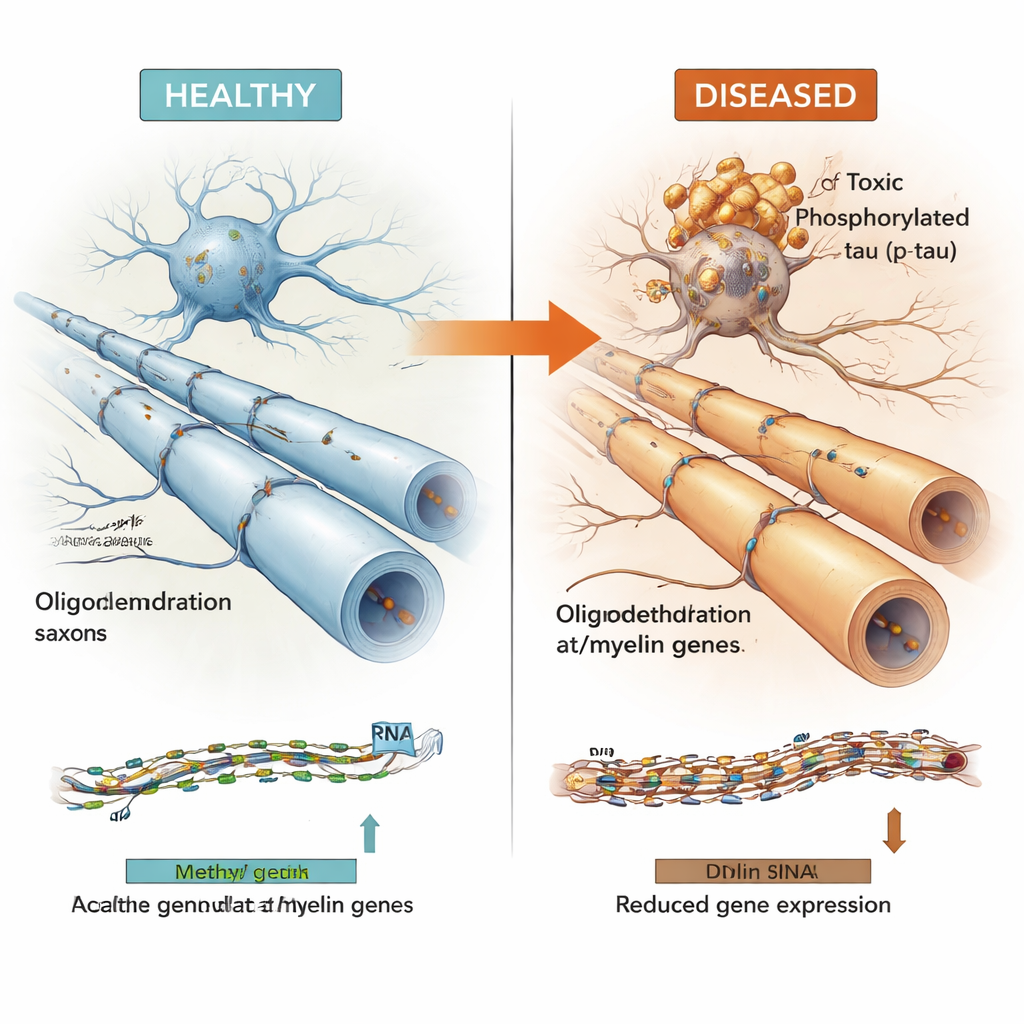
Tau ile ilişkili birçok DNA bölgesi, yakınlardaki genleri etkileyen “aktif” genom bölgelerinde yer alıyordu. Aynı beyinlerden elde edilen metilasyon verilerini gen ifade ölçümleriyle birleştirerek ekip, bu bölgelerin sıklıkla oligodendrositlerin kullandığı genleri kontrol ettiğini gösterdi—oligodendrositler sinir liflerini yalıtan miyelin kılıfı ile sararak elektriksel sinyallerin hızlı ve güvenilir iletimini sağlar. MBP, MAG ve MYRF gibi anahtar miyelin ilişkili genler ile Alzheimer risk geni BIN1 ve yeni adaylardan LDB3 bu kümede yer aldı. Toksik fosforile tau düzeylerinin yüksek olması genellikle bu bölgelerde daha fazla metilasyon ve ilişkili oligodendrosit ile miyelin genlerinin daha düşük ekspresyonu ile örtüşürken, daha zararsız kabul edilen toplam çözünür tau havuzu ters bir desen gösterdi.
Birden fazla beyin hastalığında görülen bir desen
Yazarlar bu bulguların sağlam ve genel geçer olup olmadığını test etmek için diğer Alzheimer beyin koleksiyonlarından ve progresif supranükleer felç ile Pick hastalığı gibi primer “tauopatiler”den etkilenen beyinlerden gelen büyük, bağımsız veri setlerini incelediler. Bu kohortlar farklı teknolojilerle ve sıklıkla farklı beyin bölgelerinde ölçülmüş olsa da birçok aynı DNA bölgesi ve oligodendrosit geni tutarlı davranış gösterdi: metilasyon düzeyleri tau yumak yükü ile ilişkiliydi ve ifadeleri hasta beyinlerde ile oligodendrositlere odaklanan tek hücre çalışmalarında azalmıştı. Önemli olarak, bu desenlerin sadece genetik farklılıklarla veya genel hücre kaybıyla açıklanamayacağı, oligodendrositlerin işleyişinde gerçek bir epigenetik değişime işaret ettiği görüldü.
Alzheimer’ı anlamak için ne anlama geliyor
Birlikte ele alındığında sonuçlar, zararlı tau düzeylerinin artmasının oligodendrositlerde miyelin ilişkili genlerin baskılanmasıyla yakından bağlantılı olduğu bir modeli destekliyor; bu durum beynin kablolamasını zayıflatabilir ve bilişsel gerilemeyi katkıda bulunabilir. Hangi olayın önce geldiği—tau birikimi mi yoksa bu miyelin genlerinin bozulması mı—henüz net değil, ancak binlerce örnek ve birkaç hastalıkta tekrar eden sıkı ilişkiler paylaşılan bir mekanizmaya işaret ediyor. Bu DNA anahtarlarını haritalandırıp bunları kamusal bir "Multiomic Atlas"a entegre ederek, bu çalışma oligodendrositleri ve bunların epigenetik düzenlemesini, sadece nöronlara veya amiloid plaklara odaklanmak yerine beyin devrelerini istikrara kavurtmayı hedefleyen gelecekteki tedaviler için umut verici hedefler olarak öne çıkarıyor.
Atıf: Oatman, S.R., Reddy, J.S., Atashgaran, A. et al. Integrative epigenomic landscape of Alzheimer’s Disease brains reveals oligodendrocyte molecular perturbations associated with tau. Nat Commun 17, 2116 (2026). https://doi.org/10.1038/s41467-026-68864-9
Anahtar kelimeler: Alzheimer hastalığı, tau proteini, DNA metilasyonu, oligodendrositler, miyelin