Clear Sky Science · tr
İnsan çinko-aktif kanalının (ZAC) sinyal iletimi ve modülasyonunun yapısal temeli
İz bir metal sinir hücrelerinin iletişimine nasıl yardımcı olur
Çinko, çokvitamin tabletlerinde bir besin olarak bilinse de vücut içinde bu metal beyinde hızlı bir kimyasal habercı görevi de görür. Burada anlatılan çalışma, hücre dışındaki çinkoyu algılayan ve bu sinyali elektriksel bir yanıta dönüştüren az bilinen bir protein olan çinko‑aktif kanalın (ZAC) atomik çözünürlükte nasıl çalıştığını ortaya koyuyor. Hücre zarındaki bu özel kapıyı anlamak, çinkonun beyin aktivitesini nasıl şekillendirdiğini aydınlatabilir ve sağlıklı ya da hastalıklı durumlarda sinir sinyallerini ince ayarlamanın yeni yollarını önerebilir.
Çinko sinyalleri için özel bir kapı
Sinir hücreleri arasındaki birçok hızlı mesaj, serotonin veya asetilkolin gibi tanıdık organik kimyasallar tarafından taşınır; bunlar hücre zarında halka biçimli kanalları açar. ZAC, bu reseptörlerin uzaktan bir akrabasıdır, ancak organik bir moleküle yanıt vermek yerine çinko, bakır ve protonlar gibi metal iyonları tarafından etkinleştirilir. ZAC beyindeki dâhil birçok insan dokusunda bulunur, ancak fare ve sıçan gibi standart laboratuvar hayvanlarında yoktur; bu da ilerlemeyi yavaşlatmıştır. Bu çalışma, insan ZAC’ının dinlenme hali, çinko bağlı hali ve kanalı kapatan iki farklı ilaçla yakalanmış yüksek çözünürlüklü kryo‑elektron mikroskopisi ile birkaç üç boyutlu anlık görüntüsünü sunuyor. Birlikte bu yapılar, çinkonun kanalın tepesine nasıl demirlediğini, iyonların nasıl geçtiğini ve engelleyicilerin kapıyı nasıl kapattığını veya iletimsiz bir durumda nasıl kama yaptığını ortaya koyuyor.
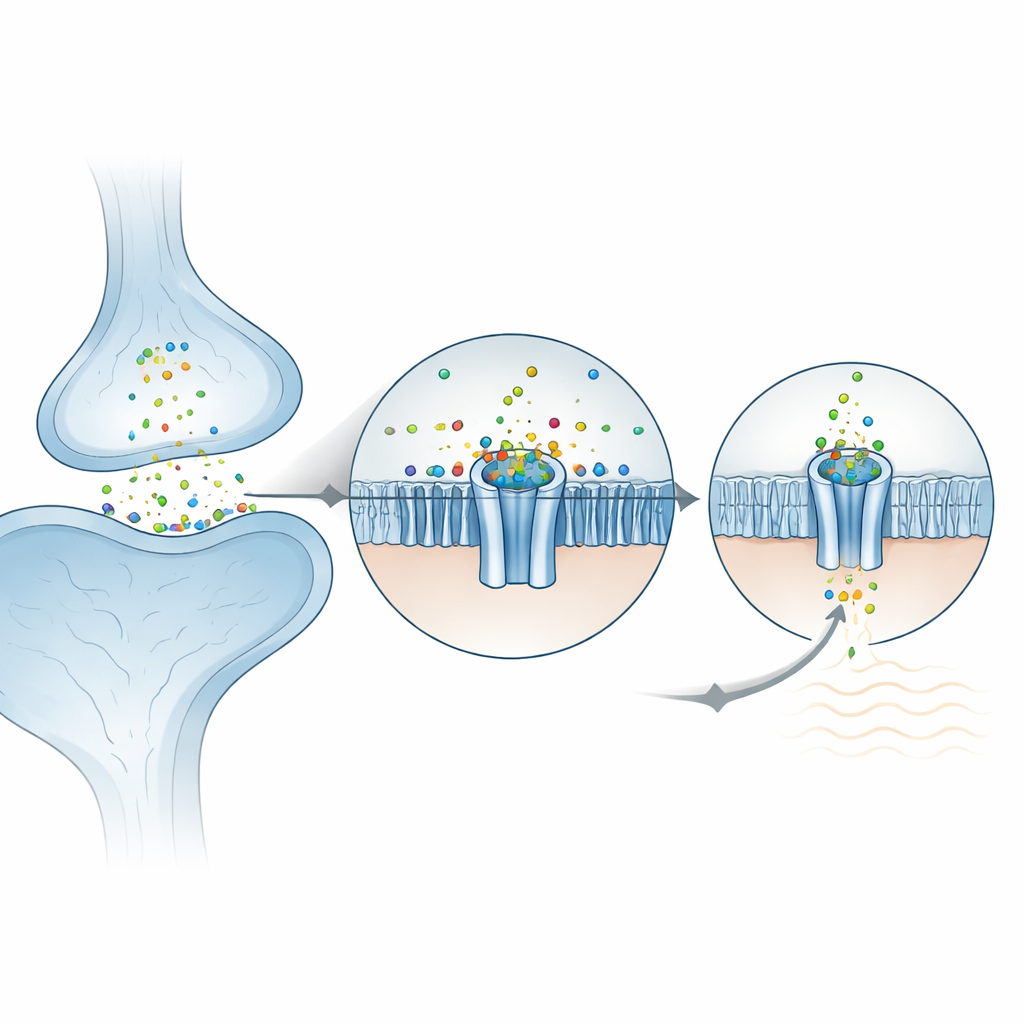
Çinko kanalın içine nasıl kilitlenir
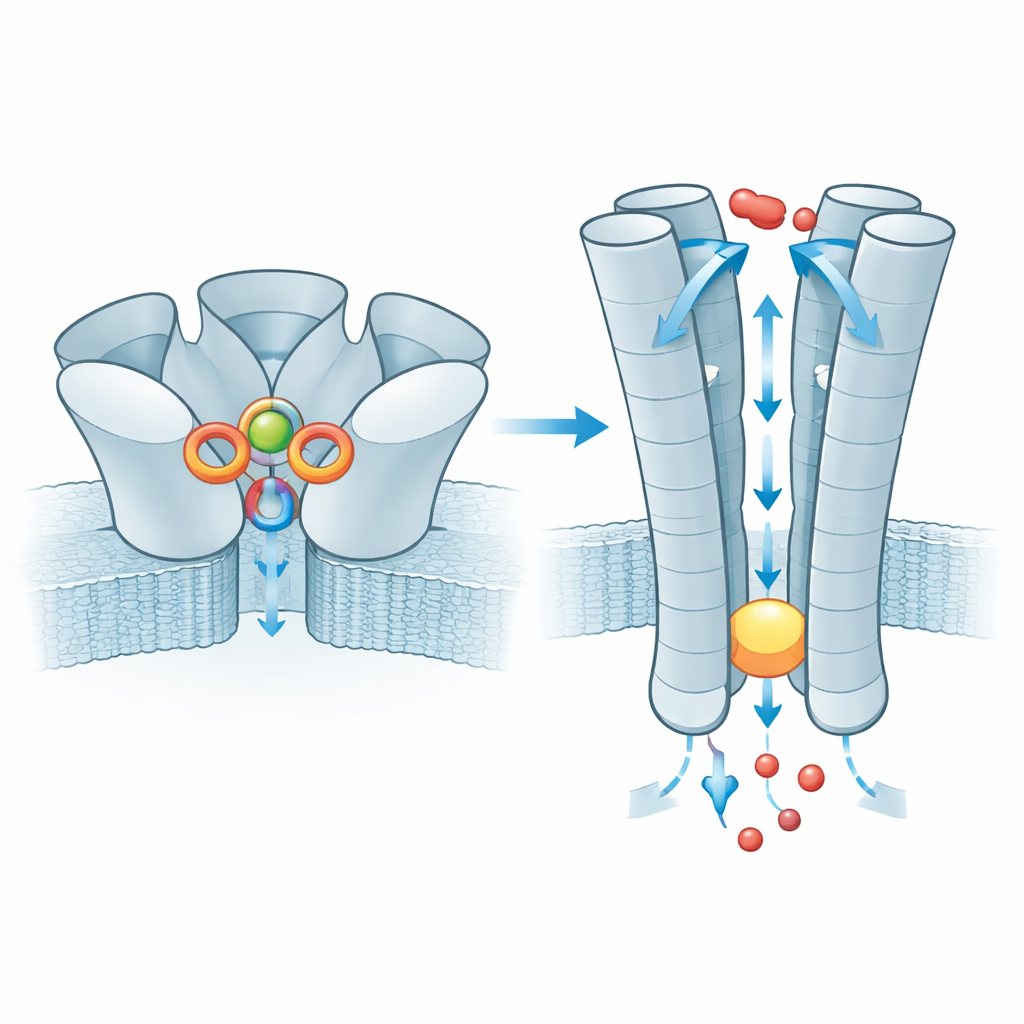
Hücrenin dış yüzeyinde ZAC, beş özdeş alt birimden oluşan bir rulo şeklinde inşa edilmiştir. Araştırmacılar, çinko iyonlarının her biri komşu iki alt birim arasında yer alan beş eşdeğer cebe yerleştiğini buldu. Şaşırtıcı bir şekilde, çinko yaygın olarak metalleri bağlayan tipik “tutucu” amino asitlerle (histidin veya sistein gibi) tutulmuyor. Bunun yerine esas olarak iki halka‑şeklinde aromatik yan zincir tarafından kucaklanıyor ve pozitif yüklü iyonu katyon–π etkileşimleriyle stabilize ediyor. Bu anahtar kalıntılar kurbağa yumurta hücrelerinde elektriksel kayıtlar için mutasyona uğratıldığında kanal çinkoya yanıt vermez hale geldi; bu da onların merkezi rolünü doğruluyor. Çevre zaten önceden düzenlenmiş durumda; bu da ZAC’ın çinko olmadan bile belirgin bir spontan aktivite göstermesini açıklamaya yardımcı oluyor: protein kapalı ile açık durum arasındaki eşikte oturuyor ve çinko dengeyi hafifçe itiyor.
İyonların yolu ve yaygın bir genetik varyant
Çinko bağlandıktan sonra etki, ZAC’ın zarı geçen kısmına iletilir; burada beş iç heliks poru oluşturur. Dinlenme halinde bu tüp, iyon hareketini engelleyen bir hidrofilik tıkacın oluşturulduğu lösin kalıntılarının bir halkasında daralır. Çinko bağlandığında tıkaç, sodyum ve potasyum gibi küçük pozitif iyonların geçmesine yetecek kadar genişler; porun yüklü astarı bu iyonlar için seçim yapmaya yardımcı olur. Ekip ayrıca tıkaçın üstündeki kısa bir dize içinde tek bir amino asidin (treonin) alanin ile değiştirildiği çok yaygın bir insan ZAC varyantını inceledi. Bu küçük değişiklik, normalde çinko bağlanmasını kapıya iletmeye yardımcı olan komşu alt birimler arasındaki etkileşim ağını zayıflatır ve elektriksel ölçümler bu varyanttan oluşan kanalların çok daha küçük akımlar ilettiğini gösterir. Bu nedenle varyant, daha az verimli bir sinyal dönüştürücü olarak davranır, ancak bunun insan fizyolojisi üzerindeki etkisi bilinmemektedir.
İki ilaç kanalı nasıl sessize alır
Çinkonun ötesinde çalışma, iki antagonist olan TTFB ve d‑tubokurarin (d‑TC) moleküllerinin ZAC’ı nasıl kapattığını da araştırıyor. TTFB, kapıya hemen üstteki iki por‑oluşturan heliks arasına sıkışarak zar bölgesinde derinlemesine yerleşen özel tasarım bir küçük moleküldür. Orada sıkı bir hidrofobik cebe ve yakınlardaki polar kalıntılara etkileşimde bulunarak heliksleri tam açık iletken duruma geçemeyecek şekilde destekler. Daha eski bir zamanlarda kas gevşetici olarak kullanılan d‑TC ise daha geniş kapsamlı davranır. Bir d‑TC molekülü normalde çinkonun bulunduğu dış cebin aynısına bağlanır; çinkonun pozitif yükünü taklit eder fakat gerçek çinkonun doğru şekilde bağlanmasını engeller. İkinci bir d‑TC molekülü ise porun girişine oturarak fiziksel olarak tüneli tıkar. Birlikte bu bağlanmalar ZAC’ı protein biçimi nispeten açık kalırken duyarsızlaşmış, iletimsiz bir konformasyonda tutar.
Buluntuların çinko ve sağlık için anlamı
Bu yapısal çalışma, ZAC’ın sıradan bir çinko sensörü olduğunu moleküler düzeyde açıkça gösteriyor; metalik iyonu aile üyelerinin nörotransmitter bağladığıyla aynı tür bir bölgede algılamak için alışılmadık bir aromatik kucaklama kullanıyor. Ayrıca kanalın açılmasını ve kapanmasını ayarlayan belirli etkileşim ağlarını tanımlıyor ve kapıyı sıkıştırabilecek veya poru tıkayabilecek iki ayrı ilaç bağlanma bölgesinin haritasını çıkarıyor. Uzman olmayanlar için ana mesaj şu: çinko yalnızca statik bir besin değildir, aynı zamanda aktif bir sinyaldir ve ZAC onun adanmış alıcılarından biridir. Bilim insanları ZAC’ın insan vücudundaki rollerini ve çinko dengesizliği ile ilişkili nörolojik bozukluklardaki yerini ararken, bu atomik düzeydeki planlar bu kanalı daha hassas şekilde modüle edecek ve potansiyel olarak bozulmuş çinko sinyalleşmesini düzeltebilecek moleküller tasarlamak için bir yol haritası sağlar.
Atıf: Zhou, Z., Long, Y., Chao, Y. et al. Structural basis of human zinc-activated channel (ZAC) signaling and modulation. Cell Discov 12, 23 (2026). https://doi.org/10.1038/s41421-026-00878-5
Anahtar kelimeler: çinko sinyalleşmesi, ligand-bağlı iyon kanalları, sinirbilim, kryo-EM yapı, kanal modülasyonu