Clear Sky Science · tr
JNK1-ZDHHC14 ekseni tarafından düzenlenen ASCT2 palmitoilasyonu glutamin metabolizmasını ve NSCLC ilerlemesini koordine ediyor
Akciğer Kanserinin Ateşini Beslemek
Hızlı büyüyen birçok akciğer kanseri, ana yakıt ve yapı taşı olarak görev yapan yaygın bir amino asit olan glutamine bağımlıdır. Bu çalışma, tümör hücrelerinin yüzeylerindeki büyük bir glutamin “kapısını” nasıl ince ayarladığını ve bu kontrol sisteminin bozulmasının kanser büyümesini nasıl yavaşlatabileceğini ortaya koyuyor. Bu gizli yakıt vanasını anlamak, bazı tümörlerin neden bu kadar zor aç kaldığını açıklamaya yardımcı oluyor ve enerji kaynaklarını daha etkili biçimde kesebilecek yeni ilaç kombinasyonlarına işaret ediyor.
Glutamin İçin Hücresel Bir Kapı
Glutamin, hücrelere esas olarak dış zarında yer alan ve glutamini içeri taşıyan ASCT2 adlı bir taşıyıcı protein aracılığıyla girer. En yaygın akciğer kanseri türü olan küçük hücre dışı akciğer kanseri (NSCLC) genellikle hızlı bölünme ve hayatta kalmayı desteklemek için glutamine yoğun şekilde bağımlıdır. Tümörlerde yüksek ASCT2 düzeyleri agresif hastalık ve kötü hasta sonuçları ile ilişkilidir. Yine de ASCT2 kendisi sürekli üretilir, modifiye edilir ve parçalanır; bu da şu soruyu gündeme getirir: bu bekçi olarak görev yapan proteinin ne kadarının her an hücre yüzeyinde kaldığını ne belirliyor?
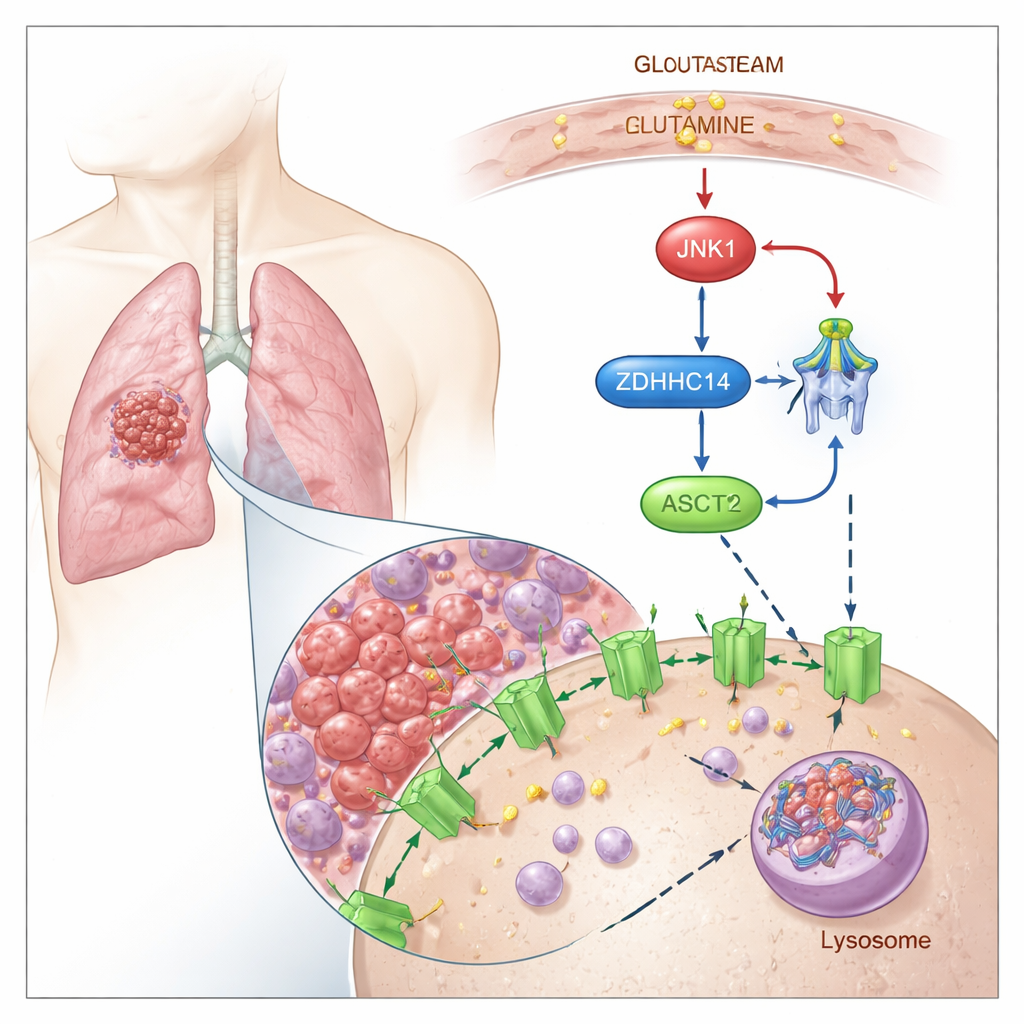
ASCT2'yi Parçalanma İçin Etiketlemek
Araştırmacılar, ASCT2'nin palmitoilasyon adlı kimyasal bir “etiket” ile kontrol edildiğini gösteriyor; bu işlemde bir yağ asidi proteindeki belirli sistein kalıntılarına bağlanır. ZDHHC14 adlı bir enzimin ASCT2 üzerindeki iki korunumlu noktaya (Cys39 ve Cys48) bu lipid etiketini eklediği bulunmuştur. Etiketlendikten sonra ASCT2, hücre yüzeyinden lizozomlar adı verilen hücresel geri dönüşüm merkezlerine yönlendirilir ve burada parçalanır. Palmitoilasyonu engellemek, ASCT2'nin etiketlenip parçalanmasını önler; bu da alttaki gen aktivitesi değişmeden daha yüksek ASCT2 protein düzeyleri ve artmış glutamin alımına yol açar.
Kapıyı Koruyan Karşı-Enzim
ZDHHC14'e karşıt bir rol oynayan başka bir enzim olan ABHD17B, ASCT2'deki yağ etiketini söker. ABHD17B etkin olduğunda ASCT2 daha az palmitoil olur, daha kararlı olur ve lizozoma gönderilmek yerine hücre yüzeyine geri döndürülme olasılığı artar. Bu etiketleme ve etiketi kaldırma arasındaki gidip gelme, glutamin akışı üzerinde hassas ayarlı bir düğme gibi çalışır: ZDHHC14 ASCT2'yi yok etmeye iterken, ABHD17B onu kurtarır ve glutamin taşınmasını sürdürür. Akciğer kanseri hücrelerinde bu dengenin daha az palmitoilasyona kayması, glutamin alımını artırır ve kültür ortamında ve fare modellerinde tümör büyümesini destekler.
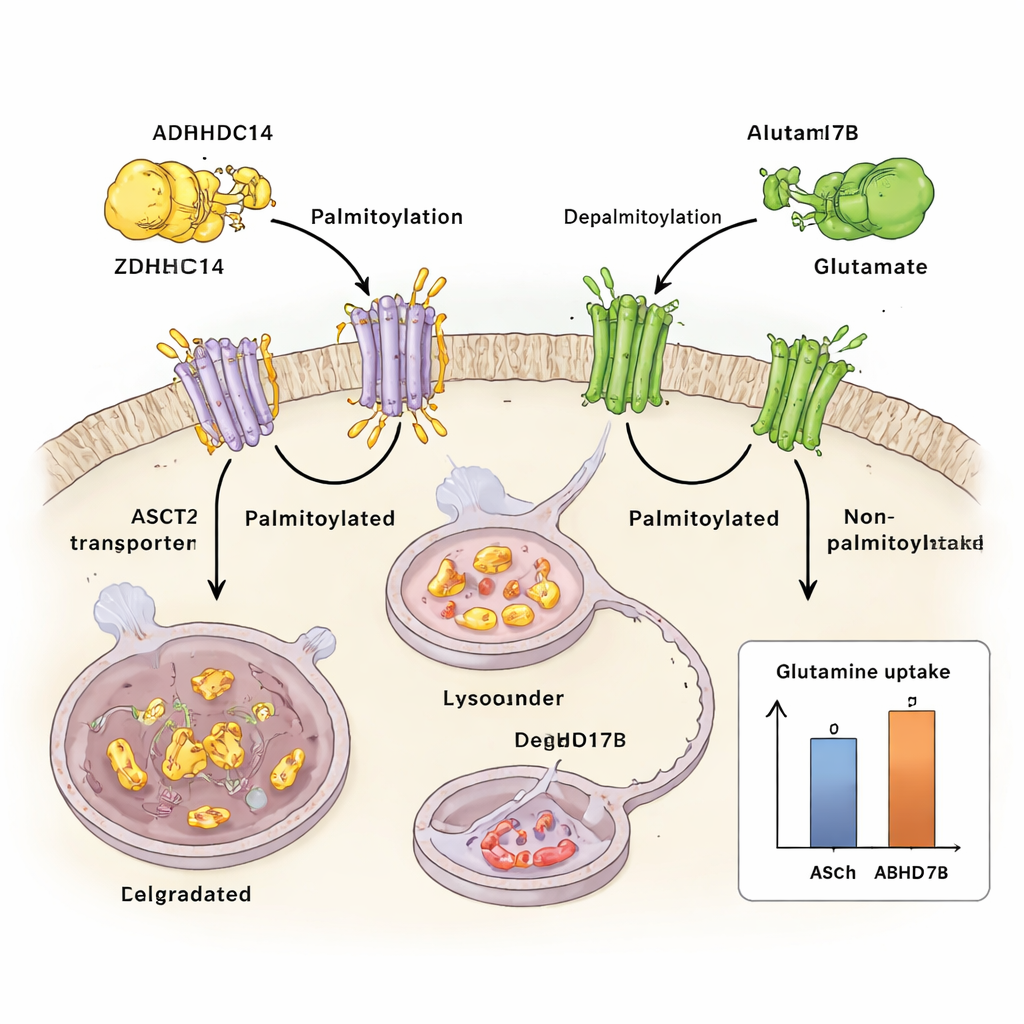
Besin Stresi Sistemi Nasıl Yeniden Kabloluyor
Araştırma ekibi daha sonra tümör hücreleri glutamin tükenmesi yaşadığında ne olduğunu inceledi. Glutamin yoksunluğu altında, strese duyarlı bir sinyal proteini olan JNK1 aktifleşir. JNK1 fiziksel olarak ZDHHC14'e bağlanır ve belirli bir konumda (Thr440) bir fosfat grubu ekleyerek ZDHHC14'ü kendi lizozomal parçalanması için işaretler. ZDHHC14 düzeyleri düştükçe ASCT2 daha az palmitoilasyon etiketi alır, parçalanmaktan kurtulur ve hücre yüzeyinde birikir—tam da hücrenin nadir glutamini toplaması en çok gerektiğinde. Bu tek JNK1-e duyarlı bölgenin mutasyonu ZDHHC14'ü stabilize eder, ASCT2 etiketlemesini geri getirir ve glutamin alımını azaltır; bu da besin stresinin bu kontrol döngüsüne ne kadar sıkı bağlandığını vurgular.
Mekaniği Terapilere Çevirmek
ASCT2 tümör metabolizması için bu kadar önemli olduğundan, deneysel bileşik V9302 gibi onu engelleyen ilaçlar kanser tedavisi olarak araştırılıyor. Bu çalışma JNK1 sinyalinin ASCT2 parçalanmasını karşılayabileceğini, yani glutamin kapısını fiilen koruyabileceğini ortaya koyuyor. NSCLC hücre ve fare modellerinde bir JNK inhibitörü ile V9302'ün birlikte kullanılması, glutamin alımını, tümör hücresi büyümesini ve tümör boyutunu tek bir ilaçtan daha güçlü biçimde azalttı. Hasta örnekleri ve halka açık veri setleri ayrıca düşük ZDHHC14 ve yüksek ASCT2 düzeylerinin NSCLC'de yaygın olduğunu ve daha kötü sağkalımla ilişkili olduğunu gösteriyor; bu moleküler desen, bu yolun hedeflenmesinden en çok yararlanacak hastaları belirlemeye yardımcı olabilir.
Hastalar İçin Anlamı
Günlük terimlerle bu çalışma, belirli akciğer kanserlerinin yüzeylerindeki moleküler bir valfi ayarlayarak favori yakıtlarını kontrol ettiğini gösteriyor. JNK1, ZDHHC14 ve ABHD17B adlı üç oyuncu, glutamin kapısı ASCT2'nin yok edilmek üzere mi etiketleneceğine yoksa açık mı tutulacağına karar veriyor. Glutamin kıt olduğunda sistem ASCT2'yi korumak ve yakıt akışını sürdürmek üzere kayıyor, bu da tümörlerin zorlu koşullarda hayatta kalmasına yardımcı oluyor. ASCT2'yi ve onu koruyan JNK yolunu birlikte bloke ederek araştırmacılar, laboratuvar ve hayvan modellerinde kanser hücrelerini daha etkili biçimde aç bırakabildi. Daha fazla test gerekse de, bu fosforilasyon–palmitoilasyon ekseni glutamin açlığı çeken akciğer tümörlerinin besin hatlarını kesmeye yönelik terapiler için umut verici yeni bir açı sunuyor.
Atıf: Chen, X., Ke, Z., Wei, S. et al. ASCT2 palmitoylation regulated by JNK1-ZDHHC14 axis orchestrates glutamine metabolism and NSCLC progression. Cell Discov 12, 13 (2026). https://doi.org/10.1038/s41421-026-00870-z
Anahtar kelimeler: glutamin metabolizması, küçük hücre dışı akciğer kanseri, ASCT2 taşıyıcı, protein palmitoilasyonu, JNK sinyalleşmesi