Clear Sky Science · tr
HSP27'nin inhibisyonu XBP1s/CerS1 etkileşimini aktive eder; bu da DRP1 kaynaklı mitofajiyi tetikleyerek hücre ölümüne karşı korur ve primer effüzyon lenfoma hücrelerinde KSHV lizitik döngüsünü destekler
Hücre Stresi Çift Kenarlı Bir Kılıç Olduğunda
Hücrelerimiz günlük saldırılardan hasarı onarıp hayatta kalmak için acil durum programlarını devreye sokar. Ancak kanser hücreleri bu aynı programları büyümek ve içinde saklı virüsleri korumak için ele geçirebilir. Bu makale, nadir bir lenfomada tek bir stres‑koruyucu proteinin engellenmesinin tümör hücrelerini ölüme doğru itmekle kalmayıp aynı zamanda içlerindeki gizli bir virüse uyanma ve çoğalma fırsatı verdiğini inceliyor. Bu hassas dengenin anlaşılması, kanseri öldürürken virüse yayılma şansı tanımayan tedaviler tasarlamaya yardımcı olabilir.
Agresif Lenfomada Gizli Bir Virüs
Primer effüzyon lenfoma, bir tür beyaz kan hücresi olan B hücrelerinin çok agresif bir kanseridir. Bu tümör hücrelerinin çoğu uykuda bir yolcu taşır: Kaposi sarkom‑ilişkili herpesvirüsü (KSHV). Virüs latan hâlindeyken yalnızca birkaç protein üretir ve konak genomu içinde saklanır. Bazı stresler virüsü aktif, lizitik bir evreye itebilir; bu evrede virüs kendini kopyalar ve yeni viral partiküller üretir, genellikle konak hücreyi öldürür. Tümör hücreleri, yanlış katlanmış proteinler, bozulmuş yağ metabolizması ve enerji üreten mitokondrilerdeki hasarla başa çıkmalarına yardımcı olan ısı şoku proteinleri ve açılmamış protein yanıtı gibi çeşitli stres‑yanıt sistemlerine bağımlıdır. 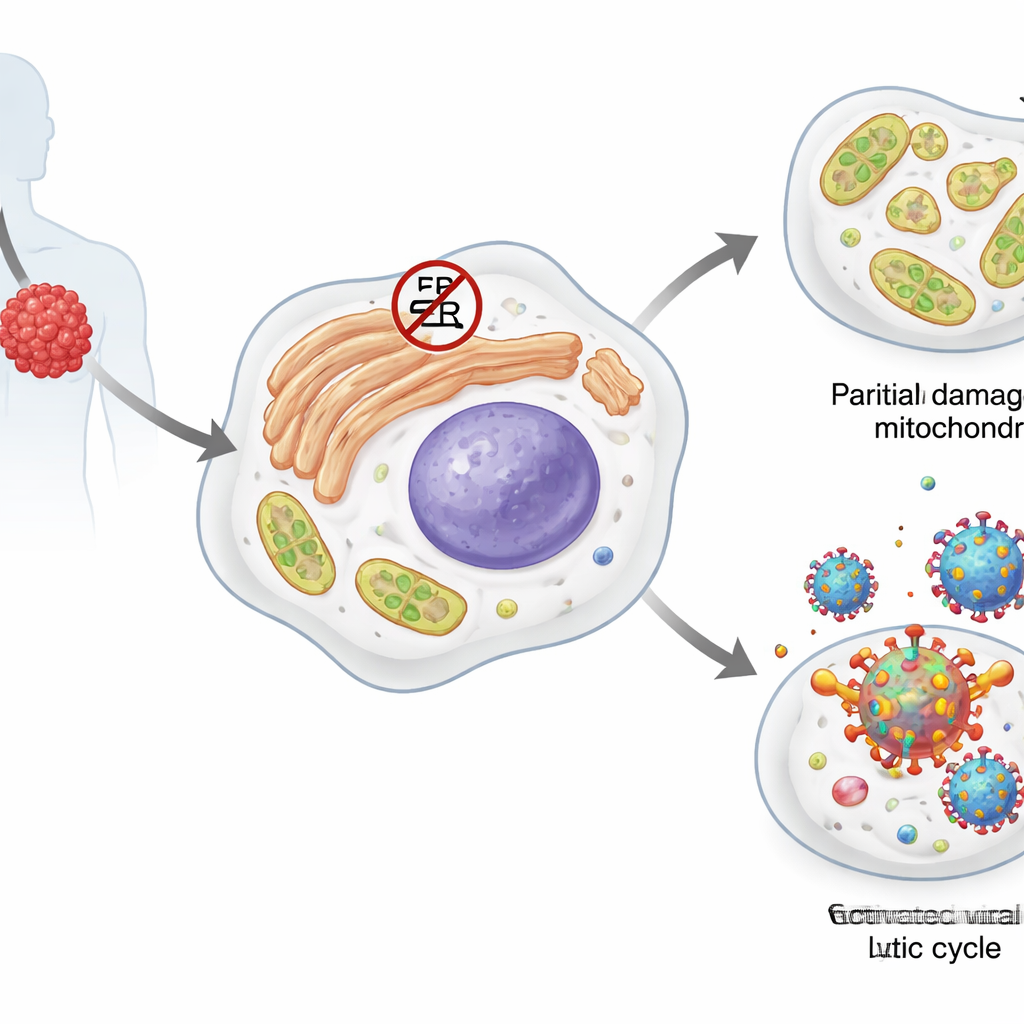
Hücresel Bir Koruyucunun Engellenmesi
Araştırmacılar, hücreleri stresten koruduğu bilinen küçük bir ısı şoku proteini olan HSP27’ye odaklandı. J2 adlı kimyasal bir inhibitör kullanarak ya da küçük RNA’larla gen susturularak, laboratuvarda büyüyen lenfoma hücrelerinde HSP27 aktivitesi azaltıldı. Bu, hücrelerin hayatta kalma olasılığını düşürdü ve endoplazmik retikulum olarak adlandırılan iç zar ağında güçlü bir stres sinyalini tetikledi. Koruyucu ve hücre ölümü yönünde faktörler dahil bu yanıtın belirteçleri arttı ve XBP1s adlı anahtar bir anahtar açık konuma geçti. Aynı zamanda hücrelerde programlı hücre ölümü belirtileri arttı; bu da HSP27’nin giderilmesinin hücreleri hayatta kalma ile yok olma arasındaki kritik noktaya ittiğini doğruladı.
Hücre Yağlarıyla Konuşan Bir Stres Döngüsü
Endoplazmik retikulumdaki stres, hücrelerin yağları nasıl işlediğiyle yakından iç içedir. Ekip, HSP27’nin engellenmesinin, C18‑seramid adı verilen belirli bir yağ molekülünü üreten CerS1 enziminin seviyelerini artırdığını buldu. XBP1s kimyasal olarak bloke edildiğinde CerS1’deki artış ortadan kalktı; bu da XBP1s’nin bu koşullarda CerS1 genini açmaya yardımcı olduğunu gösterdi. Dikkat çekicidir ki CerS1’in inhibisyonu ise XBP1s’yi düşürdü ve pozitif bir geri besleme döngüsünü ortaya koydu: her faktör diğerini destekliyor. Bu moleküler etkileşim yalnızca yağ metabolizmasını yeniden şekillendirmekle kalmıyor, aynı zamanda hücrenin endoplazmik retikulum stresine uyum sağlama yeteneğini güçlendiriyor; oysa hücre ölümü sinyalleri bir yandan birikiyor.
Yok Edilmek Yerine Geri Dönüştürülen Mitokondriler
Hücrenin bir bölümündeki stres sıklıkla enerji üreten küçük santraller olan mitokondrilere sızar. HSP27 bloke edildikten sonra lenfoma hücreleri daha fazla reaktif oksijen türü üretti; bu, mitokondri sorununun bir işaretiydi ve mitokondrileri daha küçük parçalara bölen bir protein olan DRP1 seviyeleri yükseldi. Yazarlar XBP1s–CerS1 döngüsünün DRP1’i artırmaktan sorumlu olduğunu gösterdi. Bu da mitofajiyi tetikledi; mitofaji, hasarlı mitokondrilerin zarlarla sarılıp lizozom adı verilen hücresel “geri dönüşüm merkezlerine” teslim edildiği bir kalite kontrol sürecidir. Floresan boyalar ve protein belirteçleri kullanarak, mitokondrilerin seçici olarak uzaklaştırıldığını doğruladılar. DRP1 kimyasal veya genetik olarak bloke edildiğinde bu mitofaji azaldı ve hücreler daha kolay öldü; bu da mitokondri geri dönüşümünün gerçekte stres altındaki tümör hücrelerinin dayanmasına yardımcı olduğunu gösterdi. 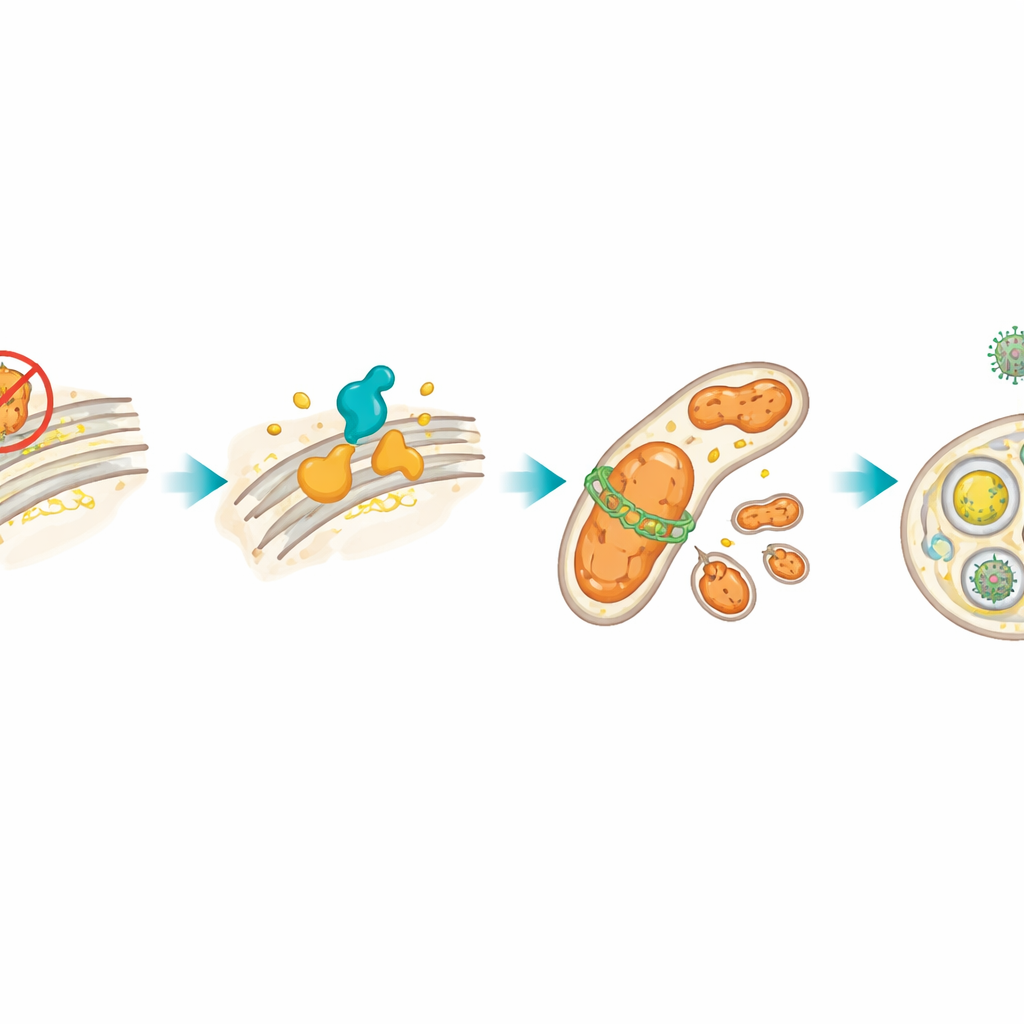
Virüse Kaçmak İçin Zaman Vermek
Tümör hücrelerini koruyan aynı mitofaji KSHV’ye de fayda sağladı. XBP1s aktivasyonu, C18‑seramid birikimi ve artmış mitokondri fisyonu bu virüsün yeniden uyanmasıyla ilişkilendirilmiştir. Burada HSP27 bloke edildiğinde daha fazla hücre erken ve geç viral proteinler ifade etti; bunlar lizitik çoğalmanın açık işaretleriydi. DRP1’nin ve dolayısıyla mitofajinin bloke edilmesi bu viral yeniden aktivasyonu azalttı. Yazarlar, mitofajinin stres altında hücrelerin hayatta kalmasını hafifçe uzatarak KSHV’ye çoğalma döngüsünü tamamlamak ve ölen hücreden ayrılarak potansiyel olarak yeni hedefleri enfekte etmek için zaman verdiğini ve böylece kanser gelişimine katkıda bulunabileceğini öne sürüyorlar.
Gelecek Tedaviler İçin Anlamı
Uzman olmayan biri için temel mesaj şudur: HSP27, lenfoma hücrelerinin stresle nasıl başa çıktığına, hasarlı mitokondrileri nasıl geri dönüştürdüğüne ve kanserle ilişkili bir virüsün ne zaman uyanacağına yönelik merkezi bir yönlendirici görevi görür. HSP27 kapatıldığında, hem hücre hayatta kalmasını zayıflatan hem de paradoksal olarak mitofaji yoluyla hücreleri geçici olarak koruyan ama KSHV’nin çoğalmasına olanak tanıyan bir olay zinciri açığa çıkar. Terapötik açıdan HSP27 inhibisyonunu DRP1 kaynaklı mitofajiyi bloke eden ilaçlarla birleştirmek, tümör hücrelerini daha hızlı ölmek üzere zorlayabilir ve virüsün yayılma şansını sınırlayarak bu ölümcül lenfomaya karşı iki yönlü bir strateji sunabilir.
Atıf: Gonnella, R., Corrado, V., Scaffidi, G.F. et al. Inhibiting HSP27 activates the XBP1s/CerS1 interplay, which triggers DRP1-driven mitophagy, thereby protecting against cell death and promoting the KSHV lytic cycle in primary effusion lymphoma cells. Cell Death Discov. 12, 118 (2026). https://doi.org/10.1038/s41420-026-02979-2
Anahtar kelimeler: primer effüzyon lenfoma, Kaposi sarkom virüsü, hücre stres yanıtı, mitofaji, ısı şoku proteini HSP27