Clear Sky Science · tr
Kısa zincirli acyl-CoA dehidrogenazı, kolorektal kanserde antitumör bağışıklığı beslemek için mtDNA demetilasyonunu ve sızıntısını başlatır
Neden kendi hücrelerimiz bazen kanseri bağışıklıktan gizler
Kolorektal kanser, kısmen vücudun bağışıklık savunmalarının sıklıkla tanıyıp saldırmaması nedeniyle dünyanın en ölümcül tümörlerinden biridir. Bu çalışma, kanser hücrelerinin yağları nasıl yaktığı, küçük enerji santralleri olan mitokondrilerin DNA’sını nasıl yönettiği ve bunun bağışıklık sisteminin tümöre tepki verip vermemesiyle beklenmedik bir bağlantı ortaya koyuyor. Araştırmacılar bu olay zincirini izleyerek, kolorektal kanserde bağışıklık saldırısını yeniden uyandırmanın olası bir yolu olarak eski bir doğal bileşik olan hiperisini de vurguluyor.
Kolon tümörlerinde eksik bir mitokondriyal “koruyucu”
Ekip, kolorektal kanserde tutarlı şekilde değişen metabolik genleri bulmak için büyük insan ve fare veri setlerini taramakla başladı. Bir enzim öne çıktı: kısa zincirli acyl-CoA dehidrogenaz veya ACADS; normalde mitokondrilerde kısa yağ asitlerini parçalamaya yardımcı olur. Hem hasta örneklerinde hem de birkaç fare modelinde, ACADS seviyeleri tümör dokusunda çevresindeki sağlıklı kolon dokusuna göre belirgin şekilde daha düşüktü. Bilim insanları fare kolon kanseri hücrelerinde ACADS’i azalttıklarında, tümörler daha hızlı ve daha agresif büyüdü; ACADS’i artırmak tümör büyümesini yavaşlattı. ACADS’i özellikle bağırsak epitelinde kaybetmiş şekilde genetik olarak oluşturulmuş fareler, kolit ilişkili kanserin kimyasal modelinde daha çok ve daha büyük tümörler geliştirdi; bu da ACADS’in bağırsakta tümör baskılayıcı bir rol oynadığını destekliyor.
Tümörlerin bağışıklık alarm sinyallerini nasıl azaltması
Bu büyüme etkileri sadece kanser hücrelerinin bir kültürde ne kadar çabuk çoğaldığıyla açıklanamadı; bu pek değişmiyordu. Bunun yerine, ACADS kaybı sadece sağlam bir bağışıklık sistemine sahip hayvanlarda tümör büyümesini tetikledi; bu da tümör mikroçevresinde değişiklikler olduğunu işaret ediyor. İnsan kolorektal kanserlerinin tek hücreli analizleri, ACADS’i düşük olan tümörlerin daha fazla tümör hücresi ve baskılayıcı immün hücrelerle—örneğin myeloid kaynaklı baskılayıcı hücreler, belirli makrofaj alt tipleri ve düzenleyici T hücreleri—çevrili olduğunu ve daha az yardımcı T hücresi ile doğal öldürücü hücre içerdiğini gösterdi. Bu desen, kanseri saldırıdan koruyan bir “immünsüpresif mahalle”ye işaret ediyor. 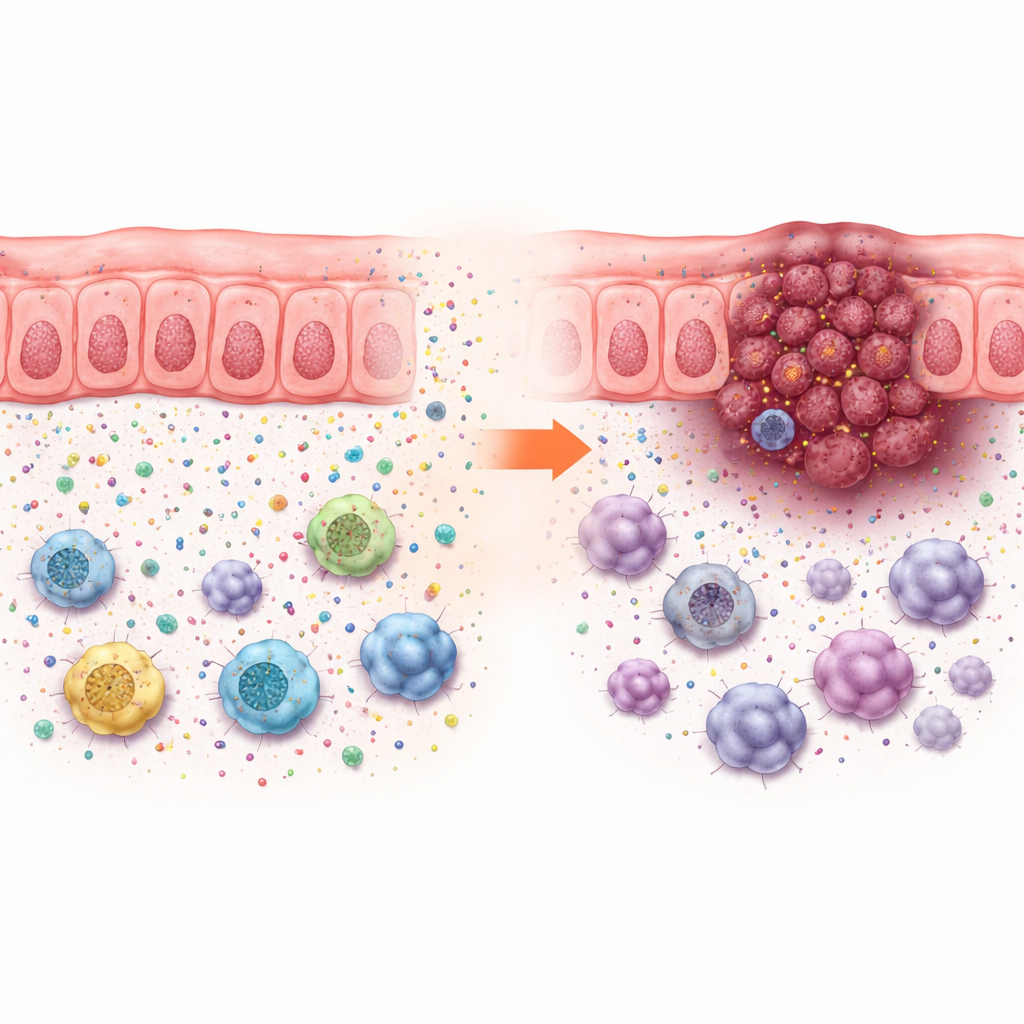
Gizli tetikleyici: mitokondriyal DNA sızıntısı
Bir yağ yakan enzim ile bir immün DNA sensörü arasındaki bağlantı nedir? Yanıt mitokondriyal DNA (mtDNA) içinde yatıyor. Stres altında, mtDNA parçaları mitokondriden hücre sıvısına sızabilir ve burada cGAS bunları bir tehlike sinyali olarak algılar. Araştırmacılar, ACADS eksikliği olan kanser hücrelerinin bu bölgede daha az mtDNA içerdiğini gösterdi, oysa toplam mtDNA değişmemişti. ACADS-yüksek hücrelerde mtDNA sızıntısını engellemek cGAS–STING’i kapattı ve bu kaçmış DNA parçalarının kritik alarm olduğunu doğruladı. Şaşırtıcı olarak, reaktif oksijen türleri, kalsiyum dalgalanmaları ve mitokondriyal şekilde büyük değişiklikler gibi klasik mitokondriyal stres faktörleri farkı tam olarak açıklayamıyordu. Bunun yerine çalışma, mitokondriyal zarın “kapıları”na ve daha önemlisi mtDNA üzerindeki kimyasal işaretlere işaret ediyor. 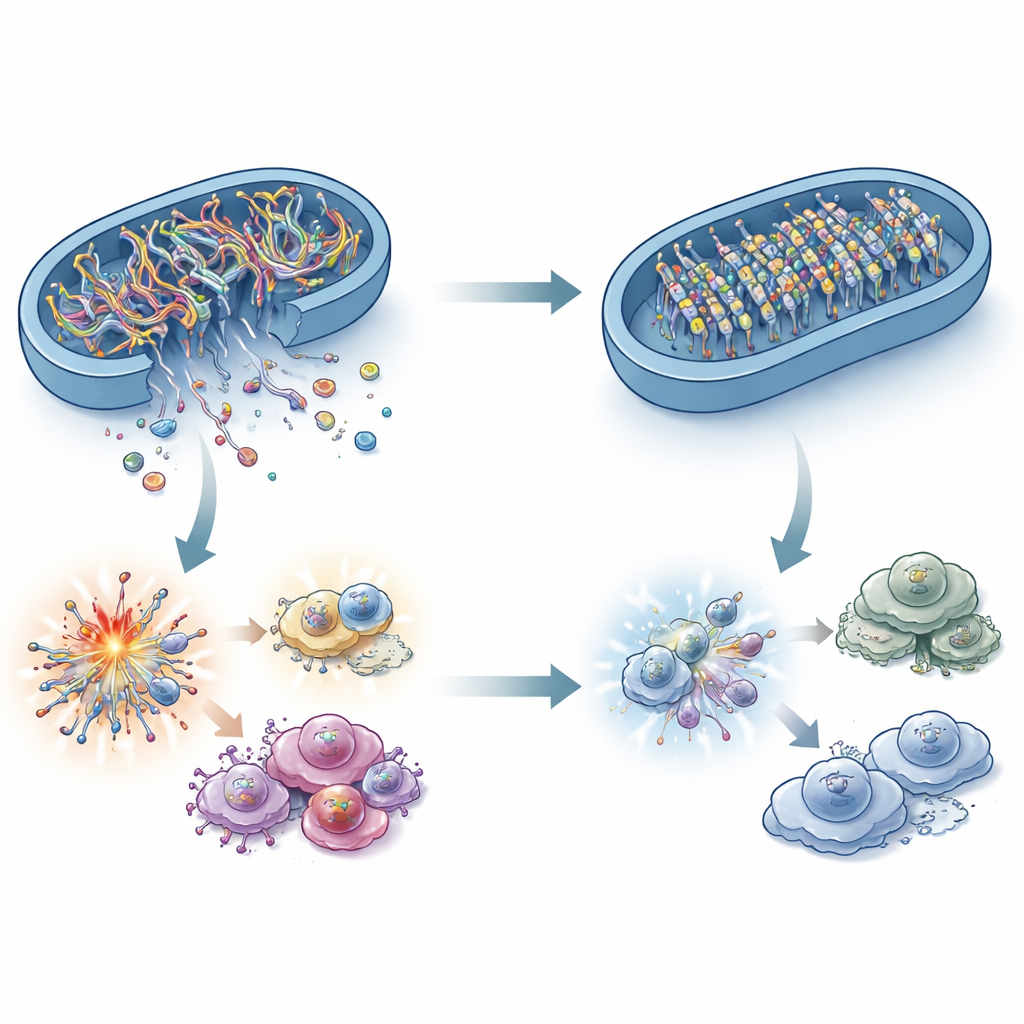
Alarmı içeride kilitleyen bir DNA metilasyonu ortağı
Protein etkileşim taramaları aracılığıyla ACADS’in mitokondriye lokalize olan bir DNA metilasyon enzimi biçimi olan DNMT1 ile ilişki içinde olduğu bulundu. ACADS kaybolduğunda, bu mitokondriyal DNMT1 birikti ve mtDNA üzerine ekstra metil grupları ekledi. Bu işaretler mtDNA’yı daha kararlı hale getiriyor ve kırılma ile sızıntıya karşı daha az eğilimli kılıyordu. Hücrelere aşırı miktarda mitokondriyal DNMT1 yüklemek, mtDNA kaçışını azalttı, cGAS–STING sinyalini bastırdı ve tümör büyümesini hızlandırdı; DNMT1’i decitabin ile bloke etmek ise mtDNA sızıntısını geri getirdi ve ACADS-eksik tümörleri yavaşlattı. Hasta örnekleri bu bulguları yansıttı: düşük ACADS, yüksek mitokondriyal DNMT1, zayıf STING sinyallemesi, daha az efektör T hücresi, daha fazla baskılayıcı immün hücre ve engelleyici immünoterapiye öngörülen daha kötü yanıtlarla bağlantılıydı.
Eski bir bileşikle bağışıklık savunmalarını yeniden uyandırmak
Bu yolun terapötik olarak kullanılıp kullanılamayacağını görmek için araştırmacılar, ACADS’e bağlanan molekülleri aramak üzere bilgisayar tabanlı tarama kullandılar. Daha önce bazı deri lenfomaları için ışığa duyarlı tedavi olarak test edilmiş doğal bir pigment olan hiperisini tanımladılar. Kolorektal kanser hücrelerinde hiperisin ACADS seviyelerini artırdı, mitokondriyal DNMT1’i azalttı, mtDNA sızıntısını artırdı ve cGAS–STING sinyalini yeniden etkinleştirdi—bunlar ACADS varlığına bağlı değişikliklerdi. Fare tümör modellerinde ve insan kolorektal tümörlerin kısa süreli kültürlerinde hiperisin tedavisi tümörleri küçülttü veya immün hücreleri daha aktif, T hücresi açısından zengin bir duruma kaydırdı. Klinik kullanımdan önce daha fazla çalışma gerekse de, bu sonuçlar farmakolojik olarak ACADS’i “yeniden açmanın” soğuk, immünsüpresif bir tümörü immünoterapiye daha iyi yanıt veren bir hale getirmeye yardımcı olabileceğini öneriyor.
Bu hastalar ve gelecekteki tedaviler için ne anlama geliyor
Günlük ifadeyle, bu çalışma bazı kolorektal kanserlerin kısmen, normalde hücrenin iç ortamına minik DNA parçacıkları sızdırmaya yardımcı olan bir mitokondriyal enzimi susturarak büyüdüğünü gösteriyor; bu parçacıklar bağışıklığı çağıran işaret fişekleri gibi davranır. Bir DNA metilasyon ortağının o mitokondriyal DNA’yı yerinde kilitlemesine izin vererek, ACADS-eksik tümörler bu işaret fişeklerini gizli tutuyor ve bağışıklık tanımadan kaçıyorlar. ACADS aktivitesini, örneğin hiperisin benzeri ilaçlarla geri getirmek, bu mitokondriyal alarm sistemini yeniden açabilir, antitumör bağışıklığı güçlendirebilir ve mevcut immünoterapilere yanıtları iyileştirebilir. Bu nedenle ACADS, mitokondriyal DNMT1 ve STING yolunun aktivitesi daha etkili kolorektal kanser tedavileri arayışında yararlı belirteçler ve hedefler olabilir.
Atıf: Yang, F., Wang, M., Hu, S. et al. Short-chain acyl-CoA dehydrogenase initiates mtDNA demethylation and leakage to fuel antitumor immunity in colorectal cancer. Sig Transduct Target Ther 11, 113 (2026). https://doi.org/10.1038/s41392-026-02675-8
Anahtar kelimeler: kolorektal kanser, tümör bağışıklığı, mitokondriyal DNA, lipid metabolizması, cGAS-STING yolu