Clear Sky Science · tr
Fused in sarcoma (FUS) hedeflemek: idiyopatik pulmoner fibrozisi tedavi etmek için yeni bir antisens stratejisi
Neden Yaralı Akciğerler Önemli
İdiyopatik pulmoner fibrozis (IPF), hassas hava keseciklerinin zamanla sert skar dokusuna dönüştüğü ve her nefesi zorlaştıran ilerleyici bir akciğer hastalığıdır. Bugünkü ilaçlar bu skarlaşmayı yavaşlatabiliyor ancak durduramıyor ya da geri çeviremiyor. Bu çalışma, hücrelerin genetik mesajlarını işlemelerine yardımcı olan FUS adlı yeni bir hedefi araştırıyor ve bu proteini DNA benzeri tasarlanmış bir zincirle kapatarak skarlaşma sürecini yatıştırıp hasarlı akciğerlerin kendini onarmasına yardımcı olup olamayacağını test ediyor.
Hücre Trafik Kontrolörünün Bozulması
FUS, genellikle RNA—genlerimizin işleyen kopyası—işlenmesini ve kullanılmasını yöneten hücre çekirdeğinde bulunan bir proteindir. ALS gibi beyin hastalıklarında FUS yanlış davranabilir: çekirdekten çıkar, hücrenin dış bölgelerinde kümelenir ve normal hücre işlevini bozar. Yazarlar, benzer bir yanlış davranışın IPF’de skarlaşmayı tetikleyip tetiklemediğini sordular. IPF’li hastalardan ve sağlıklı bağışçılardan alınan akciğer fibroblastlarını—skar maddesini bırakan bağ dokusu hücrelerini—çalıştılar. IPF hücrelerinde FUS düzeyleri genel olarak daha yüksekti ve kritik olarak, sağlıklı hücrelere kıyasla sitoplazmada çok daha fazla FUS bulunuyordu. Yüksek çözünürlüklü elektron mikroskobu kullanarak, bu proteinin çekirdek dışında anormal derecede bol olduğunu doğruladılar; bu da fibrotik akciğerlerde RNA üzerindeki normal kontrolünün bozulmuş olabileceğine işaret ediyor. 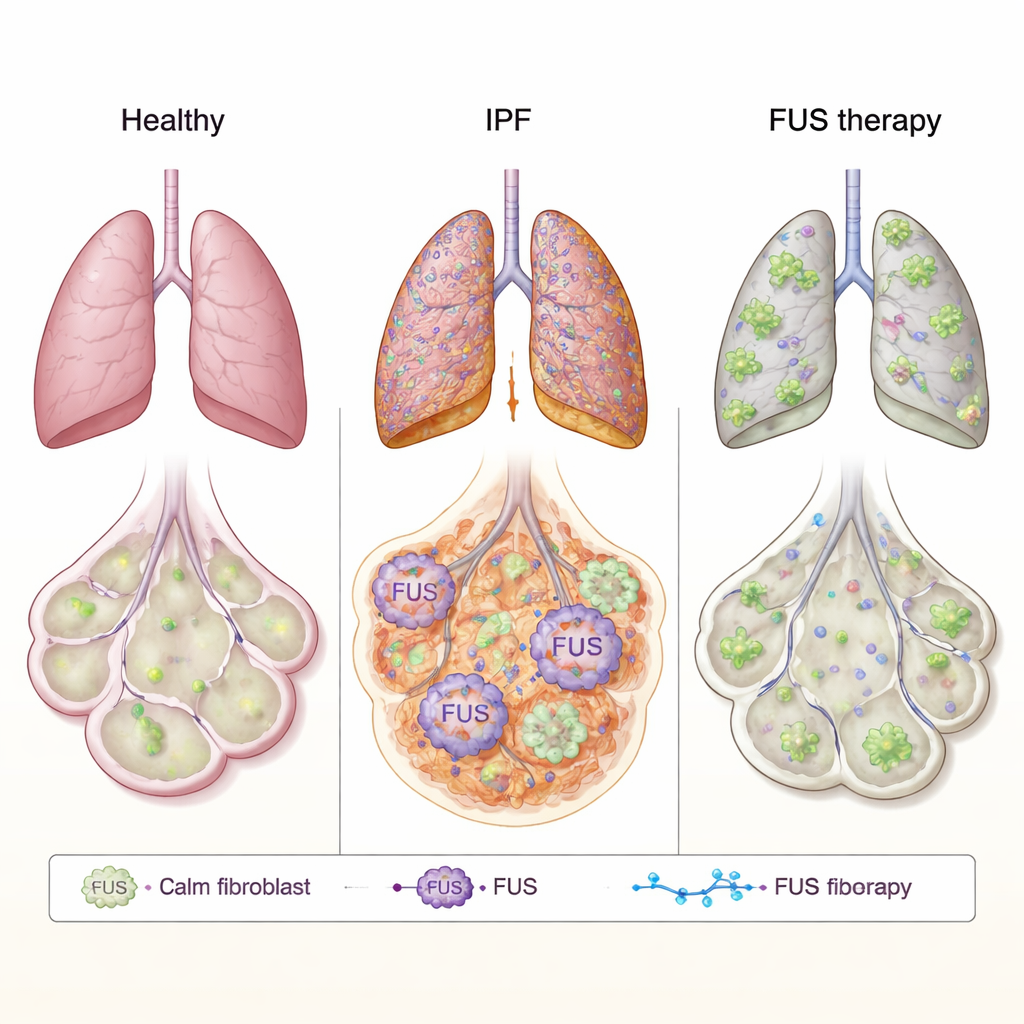
FUS’un Skarlaşan Hücreleri Nasıl Beslediği
Bu yanlış davranan proteinin aslında ne yaptığını görmek için araştırmacılar sağlıklı fibroblastlarda FUS’u artırdılar ve IPF fibroblastlarında azalttılar. Fazladan FUS, sağlıklı hücrelerin daha hızlı bölünmesini sağlarken, IPF hücrelerinde FUS’u azaltmak onların büyümesini ve hareketini yavaşlattı—skar oluşumunda merkezi öneme sahip iki davranış. Ekip daha sonra protein–RNA ortaklıklarını “donduran” ve FUS’a bağlı hangi RNA’ların olduğunu okuyan bir teknik kullandı. IPF fibroblastlarında FUS, kolajen, TGF‑β gibi büyüme faktörleri ve inflamatuar sinyaller de dahil olmak üzere fibrozisi teşvik eden birçok genetik mesaja yapışmış halde bulundu. Başka bir deyişle, FUS pro-skarlaşma mesajlarının tüm bir ağını birbirine bağlayan bir merkez olarak davranıyordu.
Hassas Bir İlaçla Sinyali Susturmak
Çalışma, FUS RNA’sına bağlanıp onun yok edilmesini tetikleyecek şekilde tasarlanmış kısa, kimyasal olarak modifiye bir zincir olan ION363 adlı bir antisens oligonükleotidi test etti. IPF fibroblastlarına ION363 uygulandığında FUS düzeyleri düştü, hücrelerin proliferasyonu ve göçü yavaşladı ve anahtar skar‑oluşturan genler sessizleşti. Önemli olarak, bu etki hücreleri öldürmeye ya da onları yaşlanmaya zorlamaya dayanmıyordu; bunun yerine davranışlarını yeniden ayarlıyor gibi görünüyordu. Aynı tedavi laboratuvarda canlı tutulan IPF akciğer dokusu ince dilimlerine uygulandığında, ekstrasellüler matris, inflamasyon ve anormal epitel kaplamayla ilişkili geniş gen grupları aşağı doğru düzenlendi, sağlıklı surfaktan üretimi ve alveolar işleve bağlı genler ise arttı. Tedavi ayrıca kolajen boyamasını azalttı ve fonksiyonel akciğer yüzey hücrelerinin belirteçlerini artırdı; bu da skarlaşmadan onarıma doğru bir kaymayı öneriyor.
Hasarlı Hava Keseciklerinin Yeniden Büyümesine Yardımcı Olmak
Minik hava keseciklerini kaplayan tip II alveolar hücreler akciğer onarımı için kritik olduğundan, araştırmacılar hasta hücrelerinden üç boyutlu “alveolosfer”ler oluşturarak minyatür akciğer birimlerini taklit ettiler. IPF hastalarından alınan kültürlerde bu yapılar normalde kötü hayatta kalır. ION363 tedavisiyle daha fazla alveolosfer oluştu, daha büyük büyüdü ve aktif yenilenmenin bir işareti olan daha yüksek lizozomal aktivite gösterdi. Ayrıntılı boyamalar, olgun gaz değişimi yapan hücre işaretçileri taşıyan daha fazla hücreyi ortaya koydu; bu da FUS’u susturmanın yalnızca fibroblastları yatıştırmakla kalmayıp aynı zamanda hasarlı epitelin daha sağlıklı bir yüzey yeniden inşa etmesini teşvik ettiğini gösteriyor. 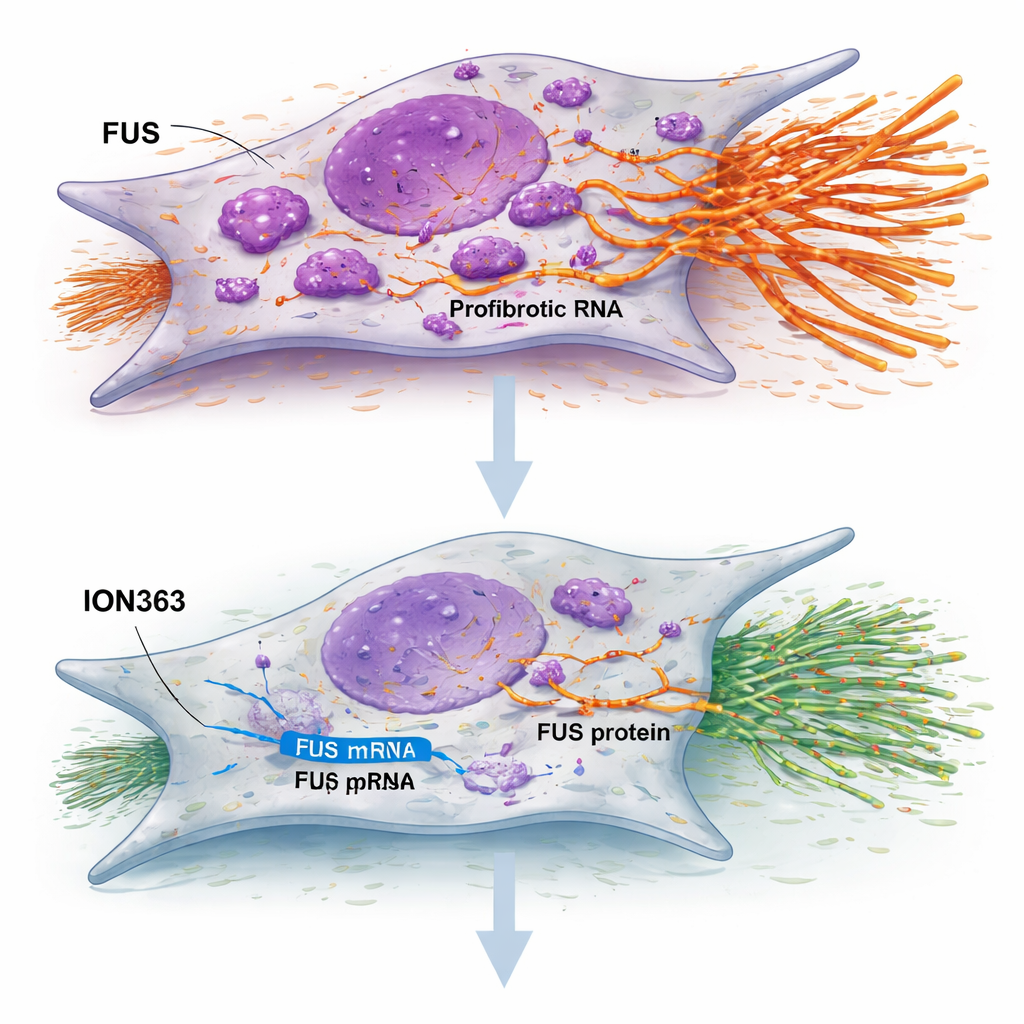
Bu Hastalar İçin Ne Anlama Gelebilir
Bir araya getirildiğinde, bu çalışma FUS’u IPF’de aşırı aktif skar‑oluşturan fibroblastları hassas hava keseciklerinin başarısız onarımıyla bağlayan bir ana anahtar olarak resmediyor. Hedefe yönelik bir antisens ilaçla FUS’u azaltarak araştırmacılar profibrotik gen programlarını düşürebilmiş, kolajen birikimini hafifletebilmiş ve hasta kökenli akciğer modellerinde rejenerasyonu teşvik edebilmişlerdir. Bu yaklaşım hâlâ laboratuvar aşamasında olup hayvan modellerinde ve klinik deneylerde dikkatli testler gerektirse de, IPF’nin bir gün yalnızca skarlaşmayı yavaşlatmak yerine akciğer yaralanması ve onarımını kontrol eden hücresel programları doğrudan dengeleyerek tedavi edilebileceğini öne sürüyor.
Atıf: Katariya, B.B., Chillappagari, S., Arnold, L. et al. Targeting fused in sarcoma (FUS): a novel antisense strategy for treating idiopathic pulmonary fibrosis. Sig Transduct Target Ther 11, 70 (2026). https://doi.org/10.1038/s41392-026-02585-9
Anahtar kelimeler: idiyopatik pulmoner fibrozis, antisens oligonükleotid, FUS proteini, akciğer fibrozisi, alveolar onarım