Clear Sky Science · sv
Multimodala sensorsystem för biosövervakning av HPAI i fjäderfäproduktionssystem
Varför fågelinfluensa på gårdar berör alla
Högpatogen fågelinfluensa, ofta kallad HPAI eller fågelinfluensa, är inte längre bara ett problem för höns på avlägsna gårdar. Nyliga vågor av H5N1-stammen har utplånat mer än 168 miljoner fåglar i USA, pressat upp äggpriserna kraftigt och till och med spridit sig till mjölkkor och människor. Denna översiktsartikel förklarar hur nya ”smarta” sensortekniker—att lyssna på djurläten, provta ladugårdens luft och köra snabba genetiska test på plats—kan upptäcka utbrott tidigare, skydda livsmedelsförsörjningen och minska risken att ett farligt influensavirus anpassar sig för att lätt spridas bland människor.
Det växande hotet på gårdar och bland människor
Under de senaste åren har en ny gren av H5N1-viruset (klan 2.3.4.4b) spridit sig i stor utsträckning bland amerikanskt fjäderfä och, mer nyligen, i mjölkboskap. Varje utbrott tvingar bönder att avliva hela flockar, vilket driver förluster över 1,4 miljarder dollar och skapar plötsliga brister i ägg- och köttutbudet. Samtidigt har mer än 70 mänskliga infektioner registrerats i USA, främst bland lågavlönade arbetare som hanterar infekterade djur och ofta har begränsad tillgång till vård. Kartor och övervakningsdata visar att vågor av H5N1 hos fåglar ofta överlappar med de vanliga vintertopparna för säsongsinfluensa hos människor, vilket skapar ett gemensamt risklandskap vid gränsen mellan djur och människa. Denna överlappning gör det särskilt viktigt att följa vad som händer i ladugårdar och betesmarker liksom på kliniker.
Hur detta virus fungerar och varför det sprids så lätt
Fågelinfluensavirus är små, omslutna partiklar som bär sitt genetiska material i åtta separata RNA-segment. Två ytproteiner, hemagglutinin (H) och neuraminidas (N), ger upphov till välkända beteckningar som H5N1 eller H3N2 och avgör vilka arter viruset kan smitta och hur allvarlig sjukdomen kan bli. Lågpatogena stammar håller sig mest i en fågels tarm och luftvägar och orsakar ofta få synliga tecken. I kontrast har högpatogena stammar som dagens H5N1 en särskild ”klyvningsplats” på H-proteinet som tillåter viruset att föröka sig i hela kroppen, vilket leder till plötslig död hos upp till 90–100% av de drabbade fåglarna. Det segmenterade genomet gör det också lätt för influensavirus från olika värdar att byta delar och utvecklas, vilket är anledningen till att överföring mellan arter som kor, katter eller vilda djur är så oroande: varje ny värd är en möjlighet för viruset att förändras.
Begränsningar i dagens biosäkerhet och testning
Fjäderfäindustrin följer redan strikta biosäkerhetsregler, inklusive kontrollerad åtkomst, desinfektion och visuella hälsokontroller. Ändå har stora HPAI-utbrott inträffat även på gårdar som uppfyller dessa standarder. En anledning är hastighet: traditionell övervakning bygger på att upptäcka sjuka fåglar, ta provpinnar och skicka dem till ett avlägset laboratorium för PCR-testning, en process som kan ta två eller tre dagar. Eftersom H5N1 kan döda en flock på ungefär 48 timmar lämnar denna fördröjning ett fönster för viruset att svepa igenom ladugårdarna och spridas mellan gårdar. Att provta tillräckligt många fåglar från gigantiska flockar är också svårt, och rutinprotokoll testar sällan damm, vatten eller ytor där virus kan finnas kvar osett. Som ett resultat slinker tidiga infektioner, lindriga fall och låga nivåer av kontamination ofta förbi försvaren.
Lyssna, sniffa och se: nya sätt att upptäcka utbrott
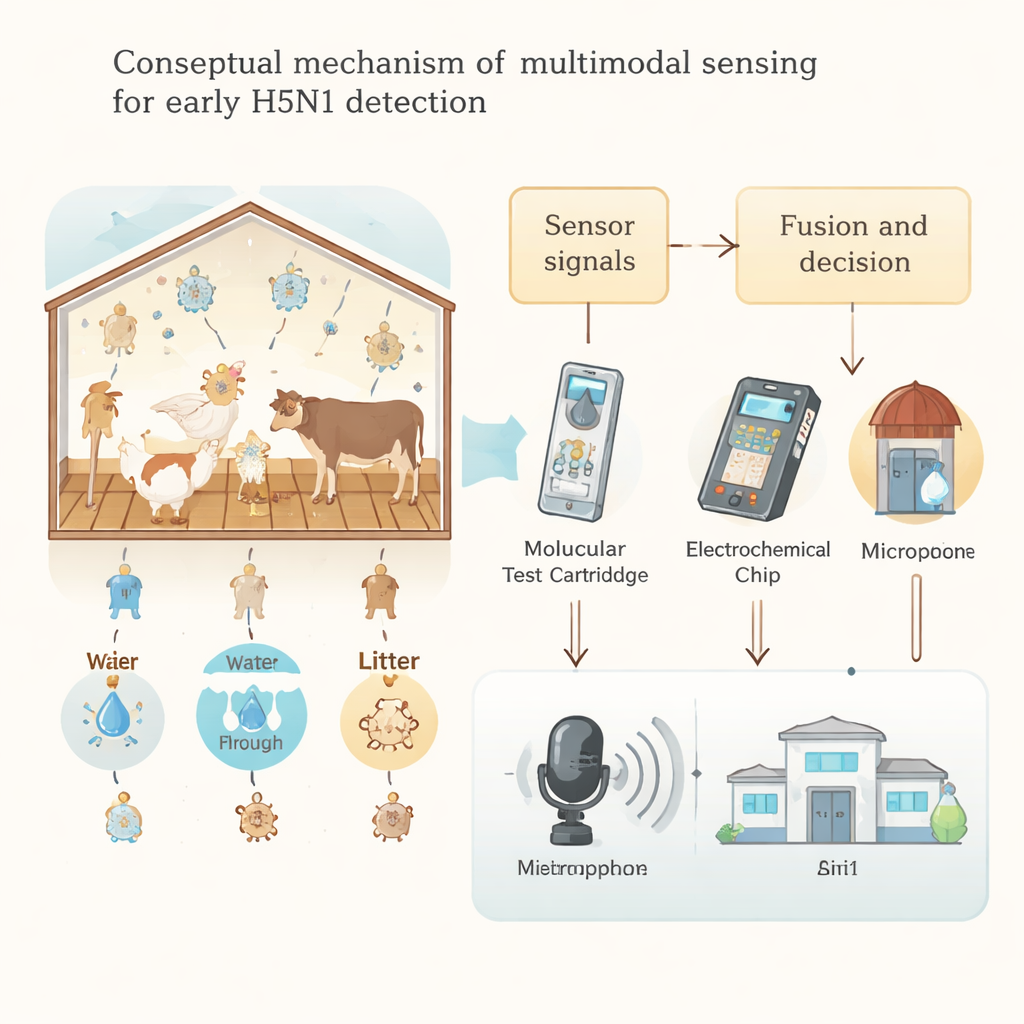
Författarna argumenterar för att gårdar behöver multimodala sensorer—flera, kompletterande sätt att bevaka problem. På den riktade sidan finns verktyg som söker direkt efter viruset eller dess komponenter: bärbara metoder som amplifierar virus-RNA vid en enda temperatur, programmerbara CRISPR-baserade tester som ger svar på under en timme, och kompakta elektro-kemiska och optiska biosensorer som kan upptäcka virusproteiner i luft, vatten eller provpinnar. På den icke-riktade sidan finns metoder som letar efter allmänna tecken på sjukdom utan att bry sig om vilken mikrob som orsakar det, såsom termiska kameror som detekterar feber, lasrar som läser kemiska fingeravtryck från ladugårdsdamm och mikrofonsystem som lär sig ljudmönstren hos friska och sjuka flockar. Till exempel kan djupinlärningsmodeller upptäcka subtila förändringar i hönsläten en till två dagar före uppenbar sjukdom, medan avancerade ljusspridningsmetoder kan särskilja virusrelaterade molekyler i aerosolblandningar med vanligt ladugårdsdamm.
Bygga ett flerstegs tidigt varningssystem
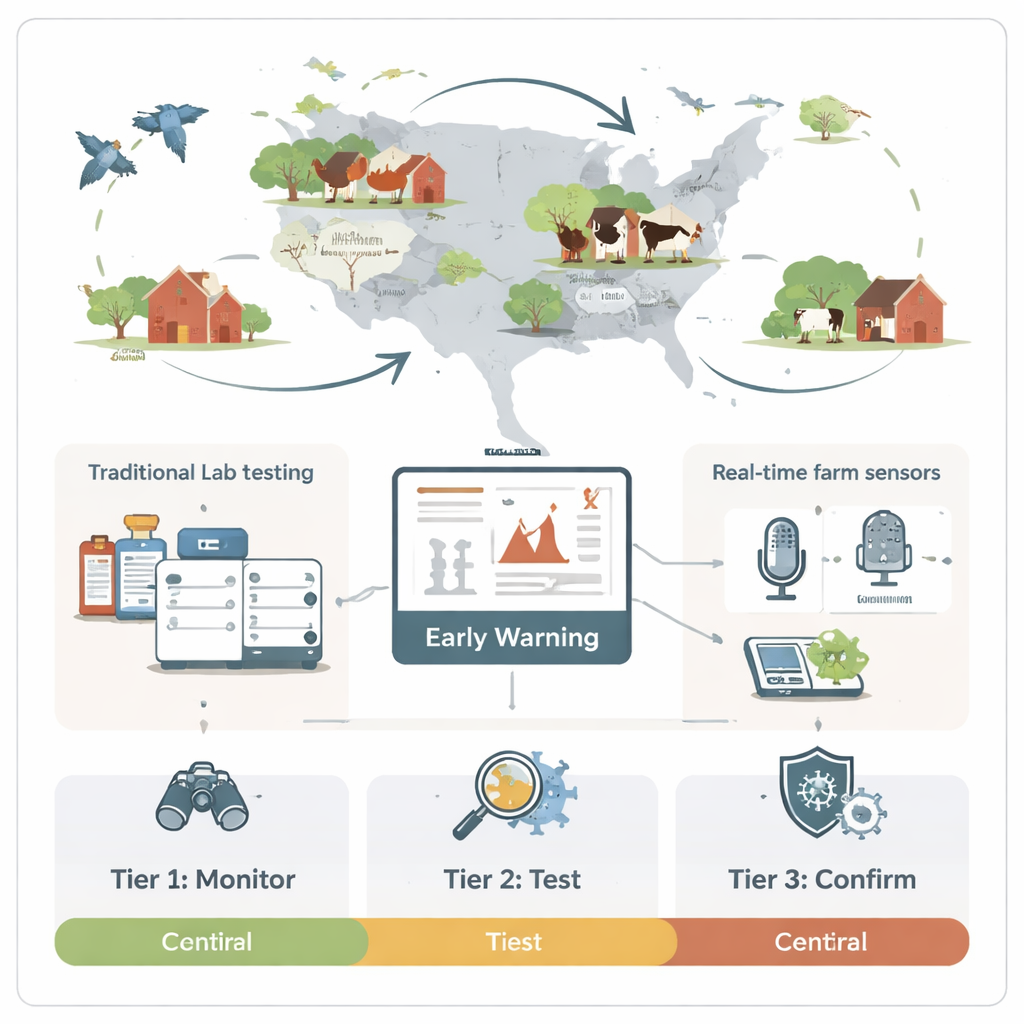
I stället för att använda alla verktyg överallt föreslår översikten ett treskiktsystem. I Skikt 1 körs lågkostnadssensorer kontinuerligt i bakgrunden och lyssnar efter onormalt hostande, spårar luftburna partiklar eller skannar damm efter misstänkta kemiska signaturer. Om dessa breda larm passerar en tröskel aktiveras Skikt 2: snabba molekylära tester och biosensorer på gården kontrollerar riktade prover som luftkoncentrat eller provpinnar, vanligtvis inom 30–60 minuter. Först när dessa snabbare screeningar antyder verklig fara startar Skikt 3, med bekräftande laboratorietester som fullständiga PCR-paneler eller virusisolering som tar en dag eller mer. Detta stegvisa förhållningssätt balanserar hastighet och tillförlitlighet, minskar panik över falsklarm samtidigt som det vinner dyrbar tid jämfört med att vänta på att fåglar ska dö eller att arbetare ska bli tydligt sjuka.
Vad detta betyder för livsmedels- och hälsosäkerhet
Enkelt uttryckt sluter artikeln att bekämpning av modern fågelinfluensa kräver att gårdar beter sig mer som smarta fabriker och mindre som isolerade skjul. Genom att kombinera öron (akustisk övervakning), näsor (kemiska och molekylära sensorer) och hjärnor (datafusionsalgoritmer) över djur-, miljö- och människohälsosektorer kan jordbruket gå från att reagera på katastrofer till att förutse dem. Tidigare upptäckt innebär färre massavlivningar, stabilare priser på ägg, kött och mjölk och lägre sannolikhet att H5N1 får de mutationer som krävs för att starta en mänsklig pandemi. Det finns fortfarande hinder—teknikkostnader, behovet av utbildning för arbetare och utmaningen att kombinera brusiga data från mycket olika sensorer—men multimodal sensing erbjuder en realistisk väg till säkrare gårdar och starkare One Health-övervakning för alla.
Citering: Ali, M.A., Ataei Kachouei, M., Jacobs, L. et al. Multimodal sensing technologies for HPAI biosurveillance in poultry production systems. npj Biosensing 3, 11 (2026). https://doi.org/10.1038/s44328-025-00075-6
Nyckelord: fågelinfluensa, biosensorer, gårdsövervakning, CRISPR-diagnostik, akustisk övervakning