Clear Sky Science · sv
Perkutan nefrostomivägledning med ett optiskt koherenstomografi-endoskop baserat på konvolutionsneuronätverk
Varför säkrare tillgång till njuren spelar roll
Njursjukdomar med stenar blir allt vanligare, och många patienter behöver ett litet rör placerat direkt i njuren för att dränera urin eller avlägsna stenar. Denna procedur, kallad perkutan nefrostomi, utförs genom att en nål styrs från patientens rygg in i njurens ihåliga mitt. Även om punktionen är liten kan fel väg riva sönder känsliga njurstrukturer eller skada blodkärl, vilket leder till blödning och andra komplikationer. Denna studie presenterar en ny högupplöst bildgivande sond, kombinerad med artificiell intelligens, som sitter i nålspetsen för att hjälpa läkare att se exakt vart de går och undvika skada.
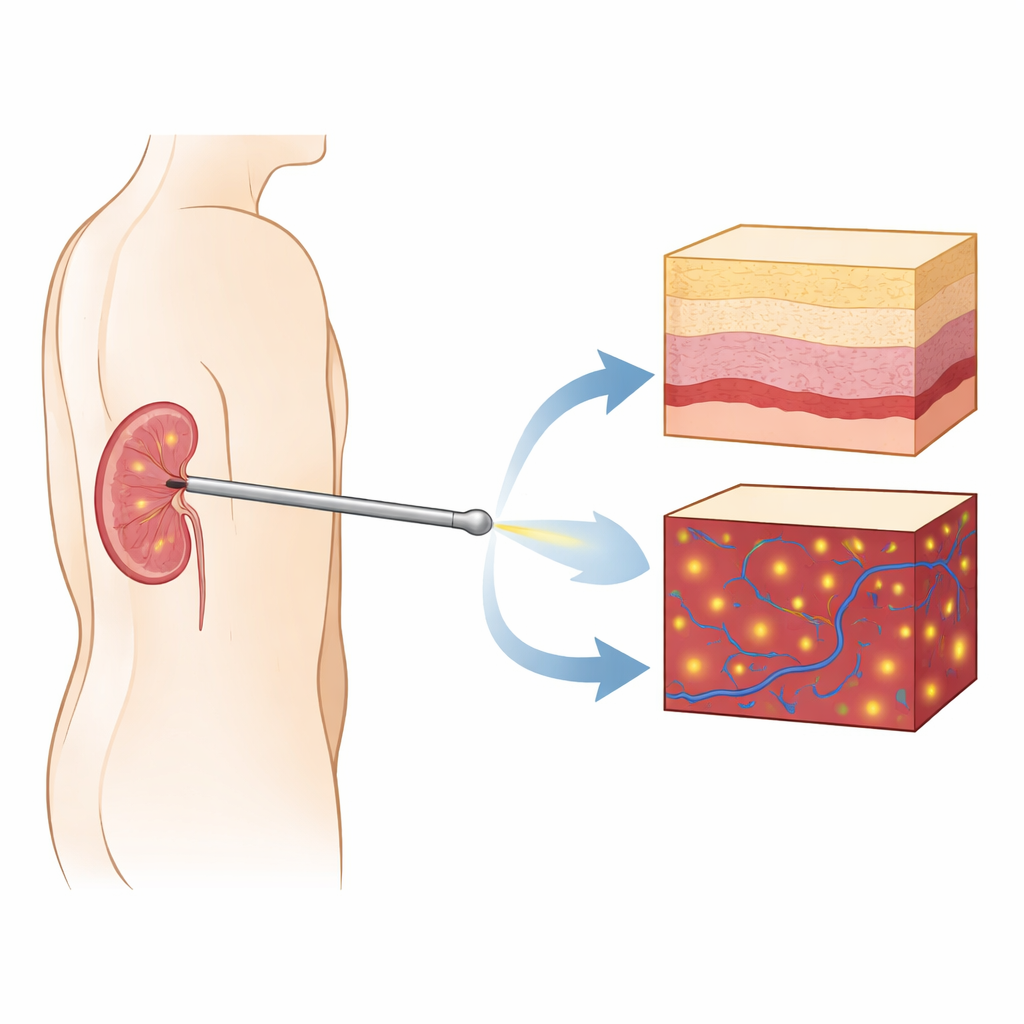
En pytteliten kamera inne i nålen
Forskarna byggde en framåtvänd bildgivande sond baserad på optisk koherenstomografi (OCT), en ljusbaserad metod som kan fånga tvärsnittsliknande “skivor” av vävnad med mikrometerupplösning—ungefär tio gånger finare än standard medicinsk ultraljudsbildgivning. De lade in en tunn gradientindexlins i en standardnefrostominål så att sonden under införandet kan titta rakt fram in i njuren. Till skillnad från vanliga endoskop som främst visar ytor, ger detta system djupupplösta bilder som visar hur vävnadsstrukturen förändras under spetsen. Samma sond kan också användas i Doppler‑läge, vilket lyfter fram rörliga röda blodkroppar och därmed avslöjar blodkärl framför nålen innan de punkteras.
Att känna igen njurlager i realtid
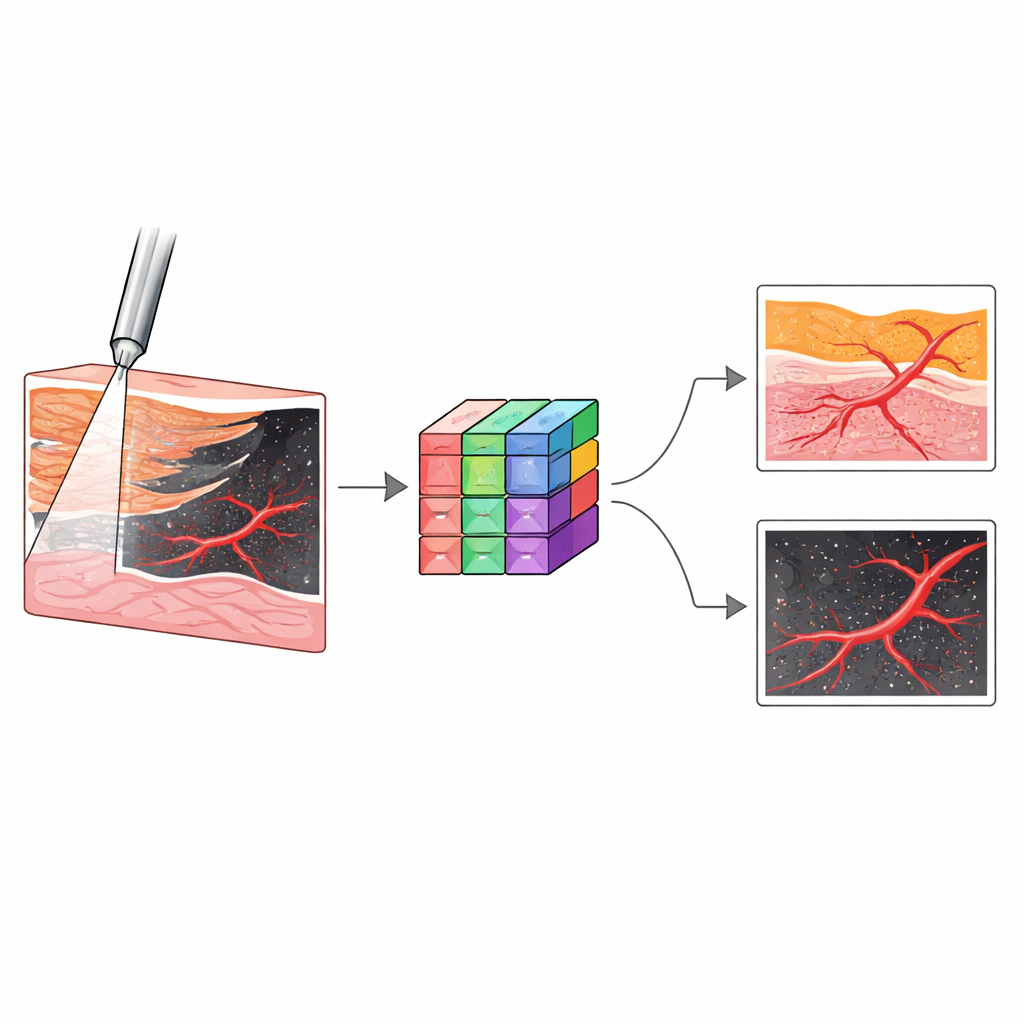
För att testa om systemet kunde skilja mellan olika njurvävnader utförde teamet experiment på 31 donerade humana njurar som hölls under när‑normala förhållanden. Vid verkliga ingrepp bör nålen passera genom yttre barken (cortex) och inre märgen (medulla), därefter in i en bägarliknande region kallad calyx och slutligen ut i det centrala urinuppsamlingssystemet (pelvis). Att avvika från banan riskerar att passera genom fettfyllda utrymmen mellan strukturer och riva tunna väggar. Forskarna rörde systematiskt sonden mot fem vävnadstyper—cortex, medulla, calyx, sinusfett och pelvis—och fångade miljontals OCT‑bilder som visade deras karakteristiska mönster. Till exempel såg cortex och medulla släta ut men skiljde sig i djupstruktur, calyx visade randiga övergångar, sinusfett gav ljusa korniga nätverk och pelvis framträdde som ett tomrum under sonden.
Att lära ett smart system att upptäcka fara
Eftersom mänskliga experter skulle behöva tid och träning för att tolka dessa nya bilder under en operation, vände sig teamet till djupinlärning. De tränade flera konvolutionsneuronät för att klassificera varje OCT‑bildruta som en av de fem vävnadstyperna, och valde sedan en arkitektur kallad Inception som bästa kandidat. I interna tester identifierade denna modell vävnader med en noggrannhet på ungefär 99,6 % och bibehöll hög prestanda på ytterligare njurar den aldrig sett tidigare. I en separat uppgift använde de en annan neuronnätsdesign, nnU‑Net, för att markera blodkärl i Doppler‑OCT‑bilder. Denna modell lärde sig skilja flödande blod från bakgrundsvävnaden med mycket hög överensstämmelse med expertens handritade etiketter, även för kärl mindre än 0,2 millimeter i diameter som är svåra att se med standardverktyg.
Hur det står sig mot dagens verktyg
Idag förlitar sig läkare vanligtvis på ultraljud eller röntgenbaserad flouroskopi för att vägleda nefrostominålar. Dessa tekniker visar njurens övergripande läge och nålens ungefärliga bana, men deras relativt grova upplösning gör det svårt att veta exakt vilken vävnad som sitter vid spetsen eller hur nära ett blodkärl är. I kontrollförsök hade erfarna radiologer som arbetade med strukturellt och Doppler‑ultraljud svårt att identifiera den precisa vävnaden vid nålspetsen och kunde inte pålitligt visualisera små kärl. Däremot erbjöd OCT‑systemet en detaljerad lokal bild plus automatiserad analys som körs på en bråkdel av en sekund på moderna grafiska processorer, tillräckligt snabbt för att ge återkoppling medan nålen avancerar.
Vad detta kan innebära för patienter
Studien tyder på att kombinationen av en nålmonterad OCT‑sond och djupinlärning skulle kunna göra ingrepp för tillgång till njuren både säkrare och mer effektiva. I framtiden skulle en läkare kunna föra in den vanliga nålen med sonden inuti, se finskaliga bilder i realtid och förlita sig på mjukvaran för att signalera när spetsen nått rätt hålighet eller närmar sig ett blodkärl. Färre punkteringsförsök skulle innebära mindre vävnadstrauma, lägre blödningsrisk och potentiellt kortare ingrepp och sjukhusvistelser. Även om arbetet genomfördes på donerade njurar snarare än levande patienter, lägger det grunden för kliniska system som också skulle kunna vägleda andra nålbaserade ingrepp, från biopsier och anestesiblocker till målinriktad läkemedelsleverans.
Citering: Wang, C., Calle, P., Yan, F. et al. Percutaneous nephrostomy guidance by a convolutional-neural-network-based optical coherence tomography endoscope. Commun Eng 5, 47 (2026). https://doi.org/10.1038/s44172-026-00613-8
Nyckelord: njurstenskirurgi, nålvägledning, optisk koherenstomografi, AI för medicinsk bildbehandling, detektion av blodkärl