Clear Sky Science · sv
Encellsinblick i trophoblastheterogenitet och adaptiv dysfunktion vid selektiv fostertillväxthämning
När en tvilling hamnar efter
För föräldrar som väntar tvillingar kan det vara djupt oroande när en av bebisarna slutar växa lika bra som den andra, trots att de delar samma livmoder och placenta. Detta tillstånd, kallat selektiv fostertillväxthämning, hotar inte bara den mindre tvillingens hälsa före födseln utan kan också påverka långsiktig utveckling. I denna studie används avancerad enkellscellanalys för att kika in i den delade placentan hos sådana tvillinggraviditeter och visa hur små förändringar i specifika placentaceller och immunsvar kan rubba balansen mellan hälsosam tillväxt och farlig brist.
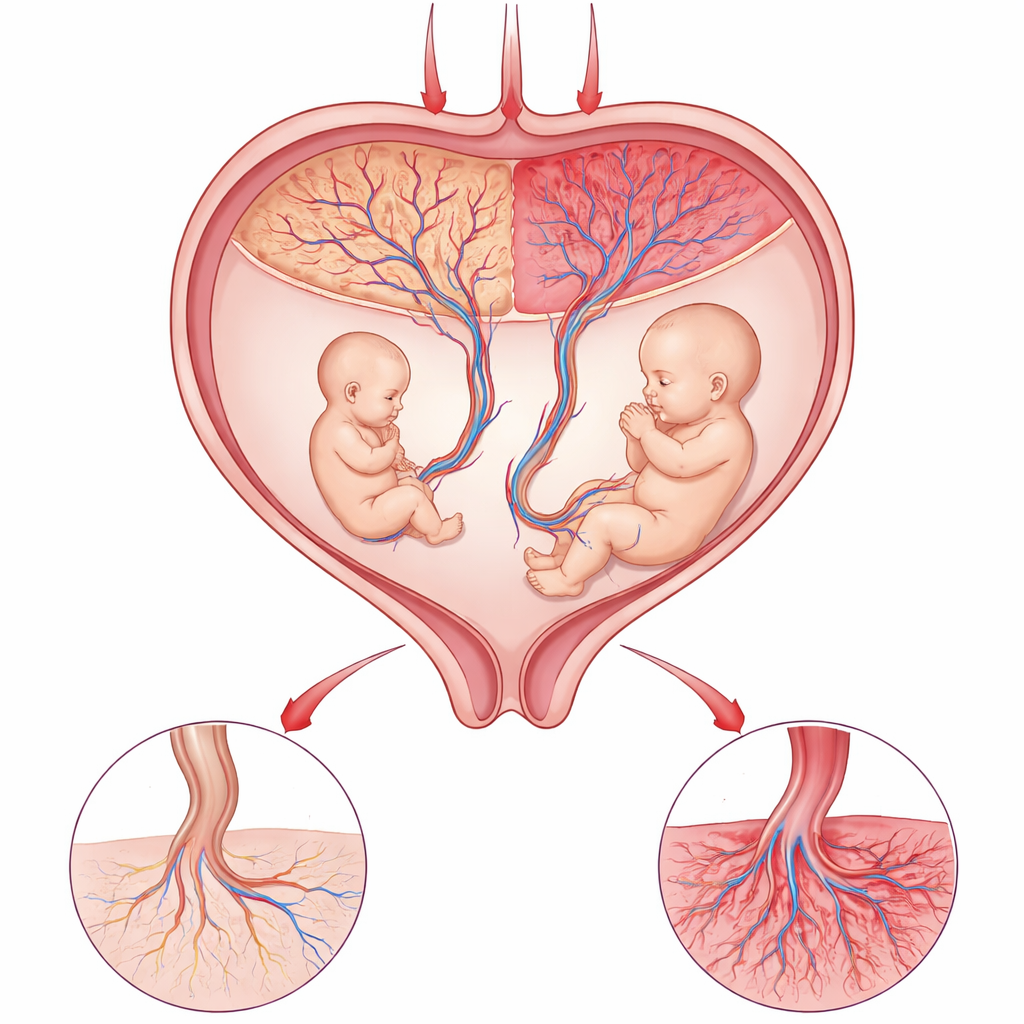
Placentans ömtåliga balansakt
Placentan är livlinan mellan mor och barn, som levererar syre och näring samtidigt som avfall avlägsnas. I vissa enäggstvillinggraviditeter delar båda fostren en enda placenta men upptar olika områden inom den. När en tvilling blir mycket mindre än den andra vet läkare att något har gått fel lokalt i det delade organet. Eftersom tvillingarna har samma mor och nästan samma gener utgör de ett kraftfullt naturexperiment: större skillnader i tillväxt beror troligtvis på hur deras respektive delar av placentan fungerar, snarare än på skillnader hos fostren själva.
Zooma in på enskilda placentaceller
Forskarna samlade placentaprover från tre graviditeter där en tvilling var avsevärt mindre än den andra. Med enkellscell-RNA-sekvensering—en metod som läser aktiviteten hos tusentals gener i enskilda celler—profilerade de mer än 175 000 celler från olika placentaregioner. Detta gjorde det möjligt att dela in cellerna i distinkta typer, inklusive stödjeceller, blodkärlsceller och flera slags immunceller. De fokuserade på en nyckelgrupp kallad villösa cytotrofoblaster, ett cellager som bekläder de små fingerlika utväxterna där maternell blodström möter fostrets cirkulation och som kontinuerligt förnyar och reparerar placentans yta.
Två viktiga celltillstånd: struktur kontra överlevnadsläge
Inom dessa villösa cytotrofoblaster upptäckte teamet två stora tillstånd med mycket olika roller. En grupp, markerad av molekylen TP63, fungerade som strukturella vårdare: de stödde barriären mellan mor och barn, upprätthöll cell‑till‑cell‑kontakter och hjälpte till att hålla vävnaden organiserad. Den andra gruppen, markerad av enzymet LDHA, var inriktad på intensiv energiproduktion och stresshantering och aktiverade vägar kopplade till mitokondrier, oxidativ stress och proteinkvalitetskontroll. I den mindre tvillingens placentaterritorier var de skyddande TP63‑cellerna uttömda, medan de stressdrivna LDHA‑cellerna expanderade och delade sig mer aktivt. Datorbaserad ”trajektori”‑analys antydde att celler pressades längs en bana från hälsosamma strukturella roller mot ett överlevnadsläge, med färre celler som nådde det fullfusionsstadium som normalt upprätthåller en slät, effektiv utbytesyta.
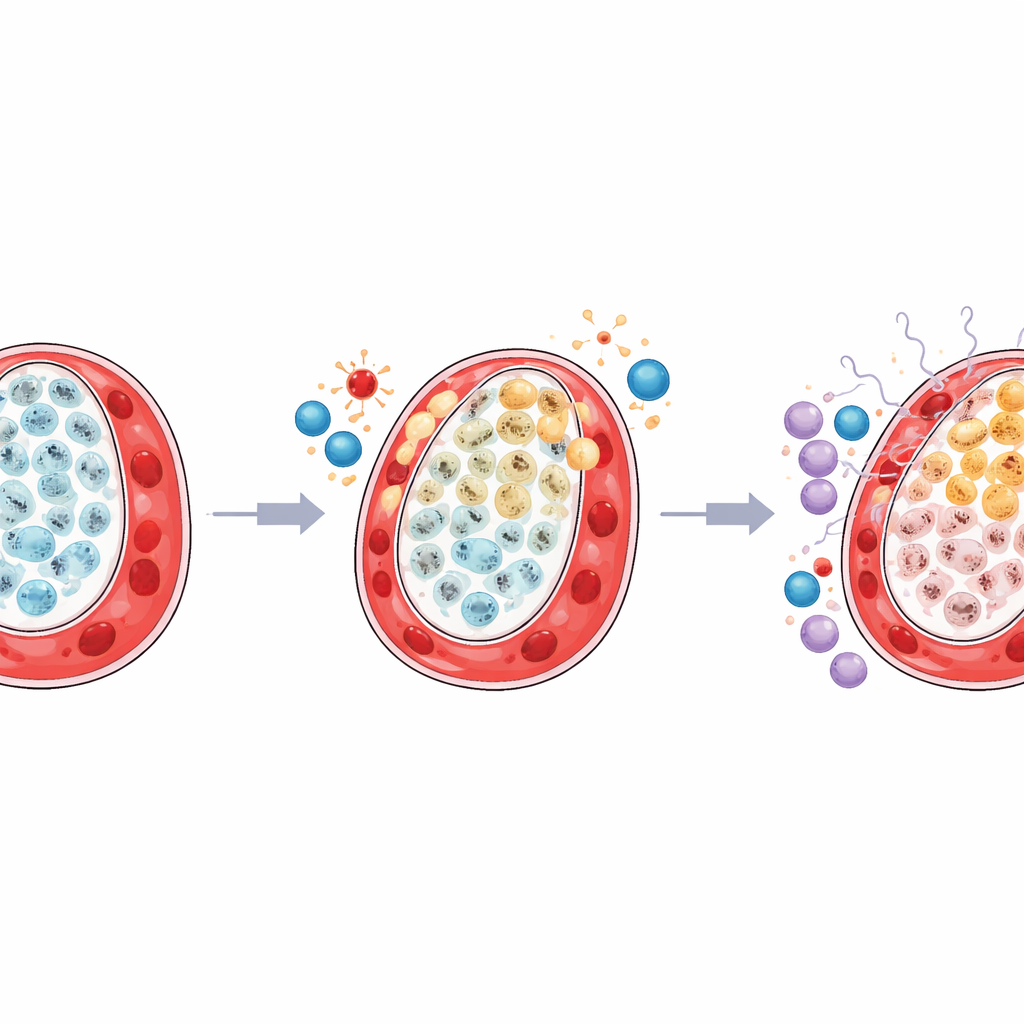
Inflammerat kvarter kring stressade celler
Studien fann också att den omgivande immummiljön i den mindre tvillingens placentaterritorium omformades på ett skadligt sätt. En hjälpsam typ av resident makrofag, känd som Hofbauer‑celler, som normalt stödjer vävnadshälsa och hanterar metabolism, var reducerad. Samtidigt blev vissa natur‑killer‑celler, programmerade för antiviral och inflammatorisk respons, mer talrika och mer aktiva. Detaljerad kartläggning av signaler som utbyts mellan celler visade att de stressade LDHA‑typ trofoblaster engagerade sig starkare med immunceller genom signalvägar drivna av interferon och närliggande alarmsubstanser. Under tiden försvagades kommunikationen mellan de strukturella TP63‑cellerna och stödjande stromaceller och blodkärlsceller, vilket tyder på att både fysisk support och lugnande immunreglering gick förlorad.
Tresidig kollaps som begränsar fostertillväxt
Tillsammans målar arbetet upp en tydlig, lättillgänglig bild av vad som går fel i placentan när en tvilling hamnar efter. Strukturella stödjeceller som håller utbytesytan tät och ordnad blir uttömda, energikrävande stressceller tar över, och immunsystemet skiftar mot ett mer inflammatoriskt tillstånd. Dessa tre trådar—förlust av struktur, metabol överbelastning och kronisk inflammation—förstärker varandra och underminerar gradvis placentans förmåga att leverera tillräckligt med syre och näring till den mindre babyn. Genom att identifiera de specifika celltyperna och signalvägarna som är involverade ger denna studie en färdplan för framtida tester och behandlingar inriktade på att upptäcka placentaproblem tidigare och kanske styra dessa celler tillbaka mot en hälsosammare balans.
Citering: Bi, Y., Yang, J., Li, X. et al. Single-cell insights into trophoblast heterogeneity and adaptive dysfunction in selective fetal growth restriction. Commun Biol 9, 387 (2026). https://doi.org/10.1038/s42003-026-09798-2
Nyckelord: placenta, tvillinggraviditet, fostertillväxthämning, single-cell RNA-sekvensering, trofoblastceller