Clear Sky Science · sv
Kvantisering av mikronukleus från helbildshematologibilder med AI fungerar som en översättbar farmakodynamisk biomarkör för hämmare av DNA-skaderesponsen
Varför små prickar i blodet kan berätta stora historier
Läkare och forskare söker ständigt enkla sätt att avgöra om ett cancerläkemedel gör vad det ska i kroppen. Denna studie visar att små partiklar i röda blodkroppar, kallade mikronuklei, kan fungera som naturliga indikatorer på DNA-skada orsakad av vissa cancerbehandlingar. Genom att kombinera helbildsscanning under mikroskop med artificiell intelligens (AI) förvandlade forskarna ett par droppar blod till en rik, automatiserad avläsning av hur kraftfullt DNA‑riktade läkemedel verkar.
Små öar av DNA i röda blodkroppar
Mikronuklei är små blåsor av DNA som ligger åtskilda från cellens huvudkärna. De bildas när kromosomer går sönder eller fördelas fel vid celldelning, händelser som är vanliga i cancer och efter exponering för DNA‑skadande ämnen. I de flesta vävnader är det svårt att säkert känna igen verkliga mikronuklei i mikroskopet eftersom tunna vävnadssnitt kan vilseleda ögat. Röda blodkroppar erbjuder en lösning: under mognaden stöter de normalt ut sin huvudkärna, men eventuella mikronuklei som bildats tidigare kan bli kvar som små, välavgränsade prickar. Dessa länge kända strukturer, historiskt kallade Howell–Jolly‑kroppar, är alltså praktiska, äkta mikronuklei som cirkulerar i blodbanan och kan avslöja hur mycket DNA‑skada som nyligen inträffat.
Att omvandla blodutstryk till data med AI
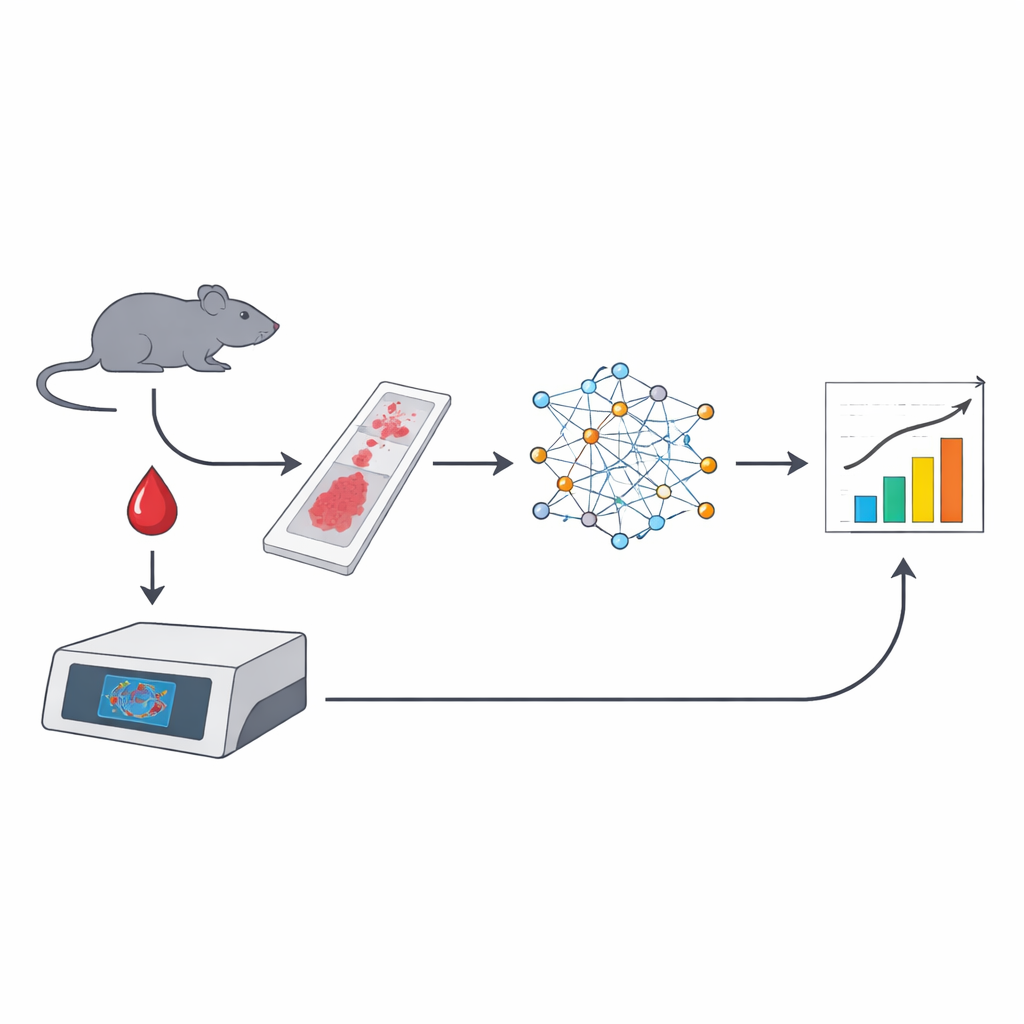
Teamet byggde en automatiserad pipeline som börjar med standardblodutstryk från möss, färgade antingen med ett fluorescerande DNA‑färgämne eller med vanliga May–Grünwald–Giemsa‑färger som används i sjukhuslaboratorier. Hela objektglas skannades i hög upplösning och övervakade djupinlärningsmodeller tränades för att känna igen röda blodkroppar, plocka ut mikronuklei och skilja omogna retikulocyter från mogna erytrocyter baserat på subtila skillnader i storlek och färg. Från en enda bild kunde systemet analysera mer än 100 000 celler, markera de som bar mikronuklei och till och med räkna celler som innehöll mer än ett mikronukleus — något konventionell flödescytometri har svårt att göra.
Att koppla små förändringar i blod till läkemedelsstyrka
Forskarna undrade sedan om frekvensen av mikronukleus‑positiva röda blodkroppar korrelerade med exponering för DNA‑skadande cytostatika och med läkemedel som blockerar DNA‑skaderesponsen, såsom PARP‑hämmare. Hos möss behandlade med cisplatin eller paklitaxel fångade de AI‑baserade räkningarna de förväntade ökningarna av mikronukleära celler. Hos tumörbärande möss behandlade med PARP‑hämmarna olaparib eller saruparib gav högre doser större ökningar av celler med mikronuklei och starkare tumörinvolution. Under flera veckors daglig dosering tillät små serielprov av blod (bara cirka 5 mikroliter vardera) teamet att följa hur mikronuklei långsamt ackumulerades och sedan minskade efter att behandlingen avbröts. När de jämförde sin glidmetod med standardflödescytometri stämde de två tillvägagångssätten väl överens, vilket visar att den nya arbetsflödet är både exakt och robust.
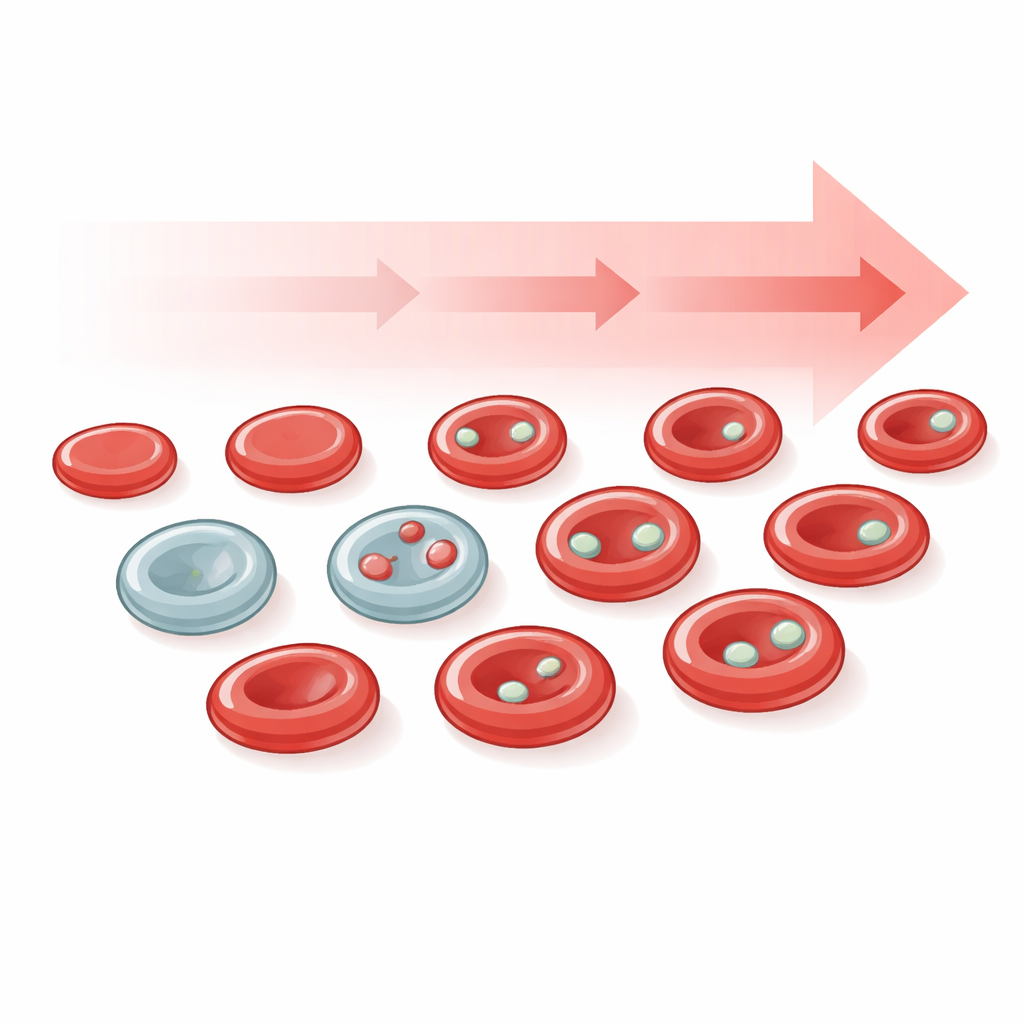
Att zooma in på unga blodkroppar för skarpare signaler
Där unga röda blodkroppar (retikulocyter) särskilt ofta innehåller färska mikronuklei tränade undersökarna sina algoritmer att dela upp den röda cellpopulationen i omogna och mogna celler på rutinmässigt färgade preparat. Denna förfining visade att mikronuklei var mycket mer förhöjda och mer dynamiska i retikulocyter än i äldre celler, vilket gav en känsligare och snabbare förändrande signal för läkemedelsaktivitet. Helbildsbilderna gjorde det också möjligt att övervaka provkvaliteten i sig — till exempel att upptäcka röda celler som blivit missformade efter dålig förvaring — så att undermåliga objektglas kunde flaggas före analys, ett viktigt steg för framtida klinisk användning.
Vad detta kan innebära för framtidens cancervård
Studien visar att ett litet blodprov, en standardfärgning av objektglas och en AI‑driven bildpipeline tillsammans kan ge en skalbar, minimalt invasiv mätning av hur kraftigt DNA‑riktade läkemedel påverkar kroppen. Även om arbetet gjordes på möss och röda blodkroppar bara är en proxy för vad som händer inne i tumörer, tyder den starka kopplingen mellan mikronuklei‑signaler och tumörsvar på att denna metod kan bli ett praktiskt verktyg i läkemedelsutveckling och så småningom i kliniska prövningar. Enkelt uttryckt kan räkning av dessa mikroskopiska DNA‑"prickar" i blod hjälpa forskare och kliniker att ställa in doser, jämföra nya läkemedel och följa behandlingseffekter över tid — utan upprepade, invasiva biopsier.
Citering: Yong, K.H.R., Robak, W.S., Mulderrig, L. et al. Micronucleus quantification from whole-slide haematology images using AI serves as a translatable pharmacodynamic biomarker for DNA damage response inhibitors. Sci Rep 16, 11437 (2026). https://doi.org/10.1038/s41598-026-41458-7
Nyckelord: mikronuklei, röda blodkroppar, PARP-hämmare, digital patologi, DNA-skaderespons