Clear Sky Science · sv
Utveckling och karakterisering av en inducerbar Tensin1-bristande transgen musmodell
Varför det spelar roll att kunna slå på och av gener hos möss
Våra kroppar är beroende av otaliga proteiner som hjälper celler att fästa vid sin omgivning, känna mekaniska krafter och reagera på skador. Ett sådant protein, kallat Tensin1, har kopplats till njursjukdom, lungsjukdomar och cancer, men forskare har saknat ett precist sätt att studera dess funktion i vuxna vävnader utan att störa utvecklingen. Denna artikel beskriver en ny typ av laboratoriemus där Tensin1 kan stängas av på kommando, vilket låter forskare se hur vuxna organ och immunceller reagerar när detta viktiga strukturella protein saknas.
En reglerbar brytare för ett klibbigt cellprotein
Tensin1 sitter där celler greppar den omgivande stödmatrisen och kopplar cellens inre fibrer till molekyler utanför. För att studera dess roll på ett säkrare sätt konstruerade forskarna möss så att en avgörande del av Tensin1-genen flankeras av speciella DNA‑ställen som kan klippas bort när ett annat protein, aktiverat av läkemedlet tamoxifen, är närvarande. Genom att föra ihop dessa komponenter skapade de möss där en kort kur med tamoxifen i vuxen ålder effektivt tar bort Tensin1, samtidigt som närliggande proteiner lämnas intakta. Tester av lungvävnad visade cirka 95 procents nedgång i Tensin1‑genaktivitet och en dramatisk förlust av Tensin1‑protein efter behandling, vilket bekräftar att den genetiska brytaren fungerar som avsett.
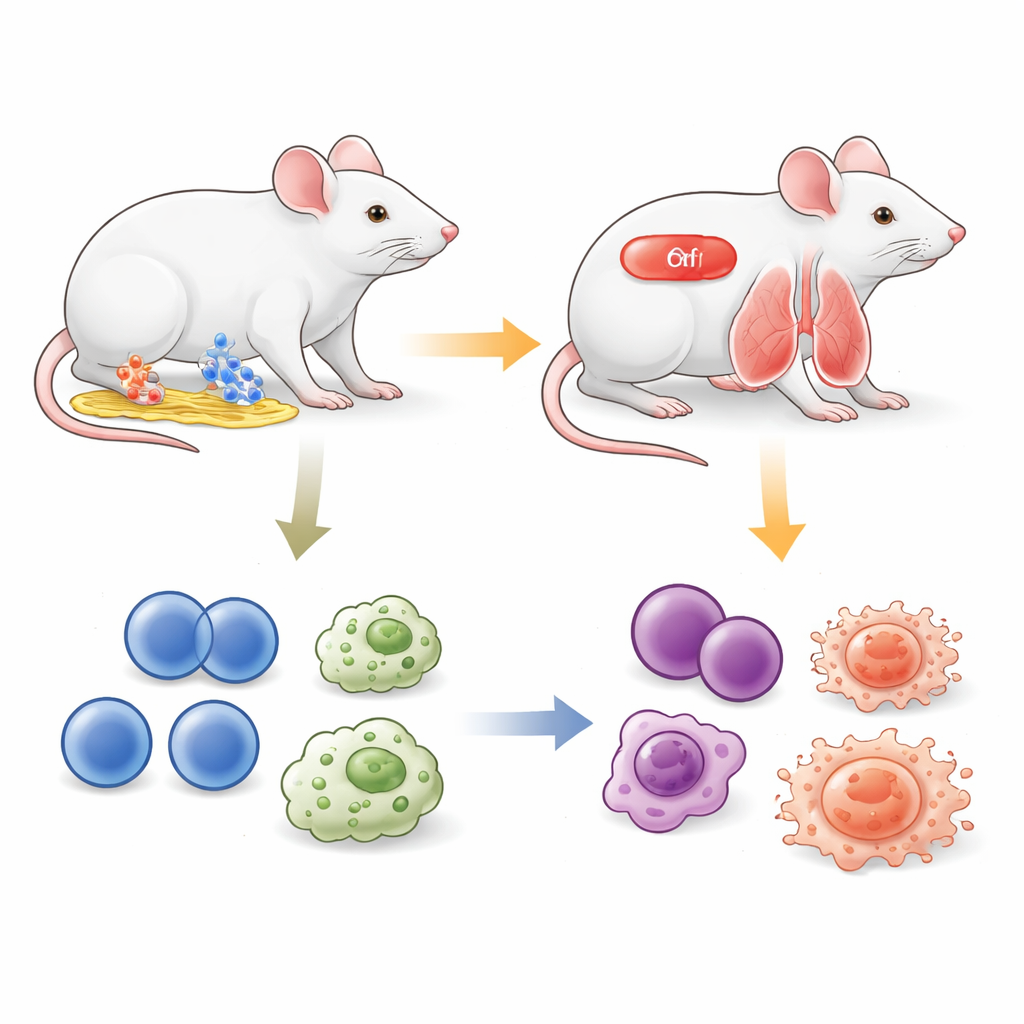
Frisk yttre framhäver subtila interna förändringar
Man skulle kunna förvänta sig att borttagandet av ett strukturellt protein kopplat till allvarlig njursjukdom snabbt skulle göra djuren sjuka. Överraskande nog förblev dessa inducerbara Tensin1‑defekta möss yttre sett friska. Före tamoxifenbehandling avlades de normalt och hade kullstorlekar liknande standardstammar. Efter att Tensin1 stängts av i vuxna bibehöll djuren normal kroppsvikt jämfört med behandlade kontrollmöss. Detaljerad undersökning av stora organ såsom hjärta, lever, mjälte, lungor och njurar under ett år visade endast milda, spridda förändringar som sågs både hos normala och Tensin1‑defekta möss. Många av dessa fynd, inklusive lokal inflammation i buken och förtjockning av livmoderslemhinnan, stämde överens med kända biverkningar av tamoxifen i sig snarare än med förlust av Tensin1. Blodprover visade heller inga tydliga skillnader i cellantal eller markörer för lever‑ och njurfunktion som kunde hänföras till genknockouten.
En oväntad signal från lungenes immunceller
Även om mössen såg friska ut misstänkte forskarna att mer subtila skift kunde ske på molekylär nivå, särskilt i lungorna där Tensin1 är känt för att påverka ärrbildande celler. De mätte genaktivitet i hela lungan och fann 171 gener som var upp‑ eller nedreglerade efter förlusten av Tensin1. Väg‑ och nätverksanalys visade att många av dessa gener inte rörde lungans strukturella stöd utan snarare immunsystemet. Genkluster kopplade till infektionssvar, immuncellsutveckling och kommunikation mellan immunceller påverkades kraftigt. Ett stort kluster av huvudsakligen nedreglerade gener var associerat med myeloida celler — immunceller som monocyter och makrofager som patrullerar vävnader och slukar skräp eller mikrober. I kontrast bar ett mindre kluster av uppreglerade gener B‑cellsignal, de immunceller som bildar antikroppar.
Hur Tensin1 formar immuncellsbeteende
För att gå djupare i vad dessa signaturer betydde använde teamet en human cellinje som efterliknar monocyter och makrofager. När de använde små RNA‑molekyler för att tysta Tensin1 i dessa celler blev cellerna mindre och spred sig mindre på ytor täckta med fibronectin, ett viktigt stödprotein. Liveavbildning visade att Tensin1‑defekta celler förflyttade sig kortare sträckor, vilket tyder på nedsatt migration. I ett fagocytosprov, där celler uppmanas att svalka lysande partiklar, slukade celler utan Tensin1 färre partiklar än kontrollceller. Tillsammans visar dessa resultat att Tensin1 hjälper myeloida celler att behålla sin form, röra sig effektivt över vävnadsyta och utföra sin städfunktion. I de levande mössen visade vätska sköljd från luftvägarna kort efter Tensin1‑knockout en tendens mot fler lymfocyter, i linje med de B‑cellsrelaterade genförändringarna som sågs i lungvävnad.
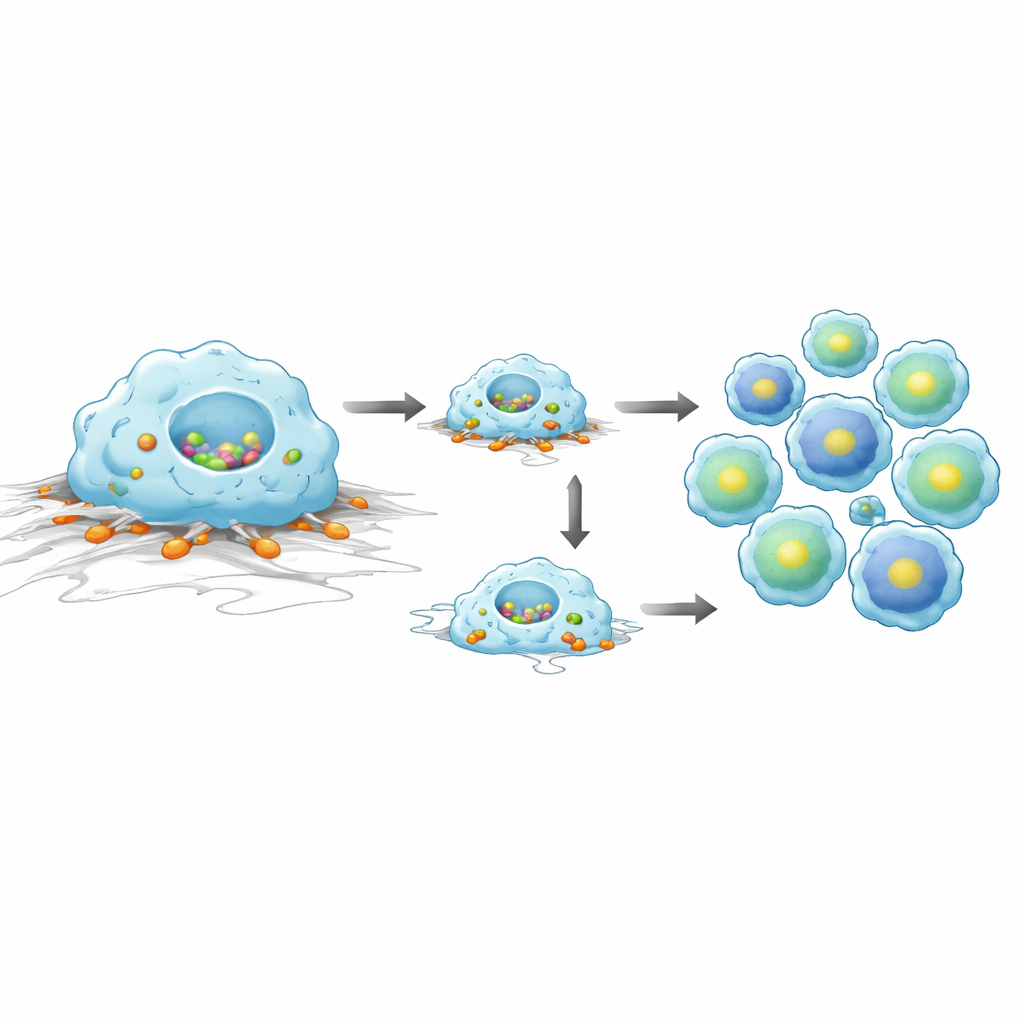
Vad detta betyder för framtida sjukdomsforskning
Enkelt uttryckt visar denna studie att borttagning av Tensin1 i vuxna möss inte dramatiskt skadar vitala organ, men att den tyst omkopplar immunaktiviteten i lungorna — försvagande signaturen hos patrullceller som rensar skräp samtidigt som antikroppsrelaterade celler stärks. Den nya musmodellen fungerar som en dimmer som kan slå av Tensin1 vid valda tidpunkter och i valda celltyper, utan de förväxlingsproblem i utvecklingen som ses när genen saknas från födseln. Detta verktyg kommer att låta forskare utforska hur Tensin1 formar svar på lungsksada, infektion och ärrbildning, och kan slutligen förtydliga varför genetiska förändringar i Tensin1 kopplas till mänskliga lungsjukdomar och cancer.
Citering: Bernau, K., Holbert, K., McDermott, I.S. et al. Development and characterization of an inducible Tensin1 deficient transgenic murine model. Sci Rep 16, 8639 (2026). https://doi.org/10.1038/s41598-026-41319-3
Nyckelord: Tensin1, transgen musmodell, lungimmunitet, makrofagfunktion, villkorlig genknockout