Clear Sky Science · sv
Personaliserat ramverk med multi-agent förstärkningsinlärning för adaptiv hantering av kroniska sjukdomar
Varför smartare vård för långvarig sjukdom spelar roll
Miljontals människor lever under lång tid med tillstånd som diabetes, hjärtsjukdom och kronisk njursjukdom. Att hantera dessa sjukdomar är en daglig balansgång som involverar läkemedel, kost, motion, sömn och stress. Läkare förlitar sig ofta på korta klinikbesök och spridda journaler, vilket gör det svårt att skräddarsy behandling när en persons liv och kropp förändras. Denna artikel undersöker hur en ny typ av integritetsvänlig artificiell intelligens kontinuerligt kan lära sig från många patienter samtidigt samtidigt som den ger högst personlig vägledning till varje individ.
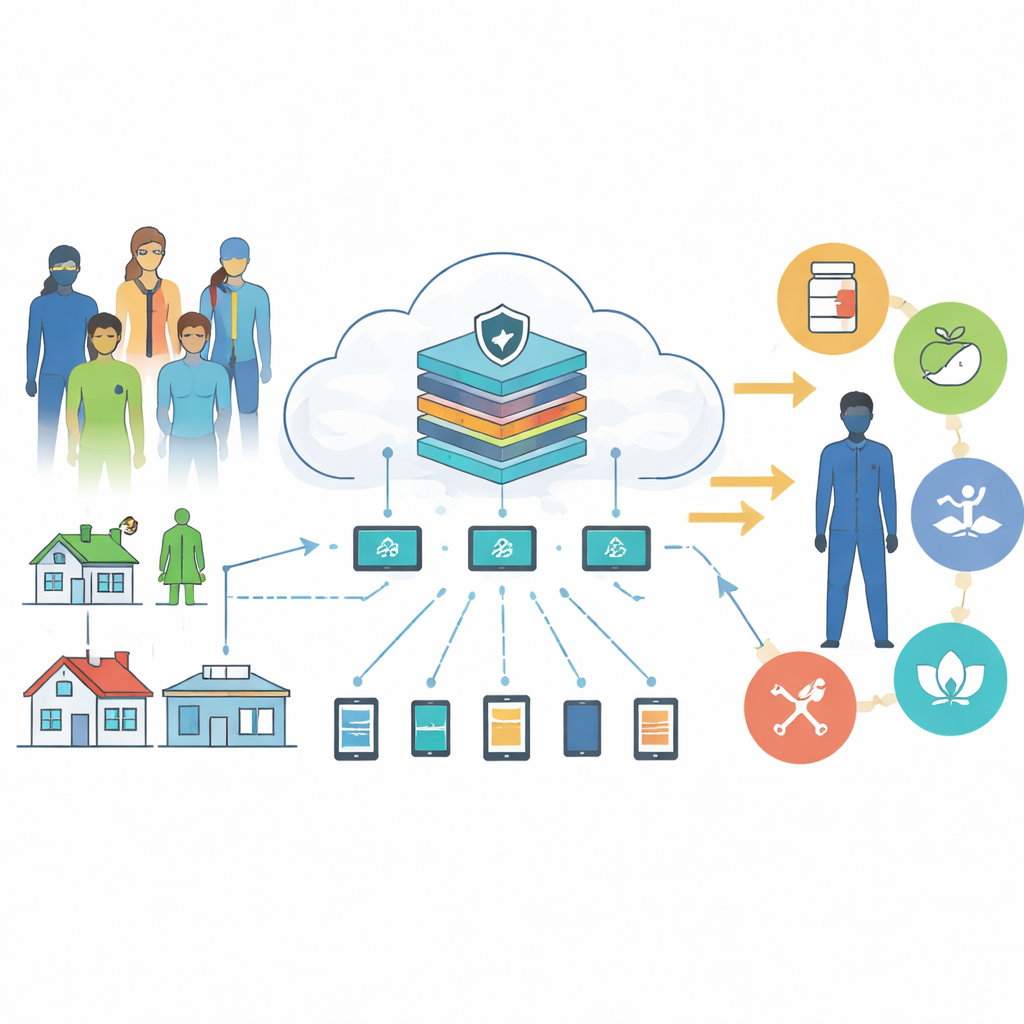
Många patienter, många datakällor, en gemensam intelligens
Författarna utgår från en enkel idé: personer med kronisk sjukdom genererar en konstant ström av ledtrådar om sin hälsa—blodtrycksmätningar, glukosnivåer, aktivitetsdata från wearables, laboratorietester från kliniker och till och med sömn- eller humörloggar. Idag ligger det mesta av den informationen i separata sjukhus, appar och enheter. Det föreslagna systemet kopplar ihop dessa källor genom det som kallas ett federerat lärandenätverk. Istället för att skicka rå patientdata till en central server tränar varje sjukhus eller hemmarenhet sin egen lokala prediktionsmodell och delar endast modellens parameteruppdateringar. En central dator genomsnittar sedan dessa uppdateringar till en starkare "global" modell. Detta tillvägagångssätt låter systemet lära mönster från stora, mångsidiga populationer samtidigt som personliga journaler hålls lokalt, vilket minskar integritetsrisk och kommunikationskostnader.
En kraftfull prediktor som förstår förändringar över tid
För att tolka rörig hälsodata från verkligheten använder ramverket en djupinlärningsmodell som kombinerar två styrkor. En del, inspirerad av bildigenkänningsnätverk, är bra på att plocka ut viktiga signaler ur komplexa indata, till exempel kombinationer av laboratorieresultat och sensormätningar. Den andra delen, lånad från moderna språkmodeller, är utformad för att följa hur saker förändras över tid—om blodtrycket till exempel gradvis stiger eller hur glukos svarar över flera dagar. Tillsammans förvandlar denna hybrida modell varje persons historik till en kompakt "embedding", ett numeriskt fingeravtryck som sammanfattar deras nuvarande hälsotillstånd och framtida risk. I tester på två publika dataset—ett som täcker ett brett spektrum av kroniska tillstånd och ett annat med fokus på njursjukdom—nådde denna prediktor mycket hög noggrannhet, omkring 98–99 %, och överträffade flera nyare AI-verktyg.

Digitala lagkamrater som samadministrerar daglig behandling
Endast prediktion förbättrar inte hälsan; behandlingsbeslut måste också anpassas över tid. För att möta detta lägger författarna till ett personaliserat lager med multi-agent förstärkningsinlärning ovanpå prediktorn. Istället för en enda beslutsfattare använder systemet flera samverkande mjukvaru"agenter", var och en inriktad på en aspekt av vården som medicinering, kost, fysisk aktivitet eller psykiskt välbefinnande. Dessa agenter övervakar det hälsofingeravtryck som prediktorn producerar, väljer åtgärder som att justera måltidsmönster eller träningsintensitet och erhåller belöningar när simulerade utfall förbättras—stabilare glukos, hälsosammare blodtryck, färre biverkningar och bättre indikatorer för livskvalitet. Över många träningsavsnitt byggda från historiska journaler lär sig agenterna koordinerade strategier som prioriterar långsiktiga fördelar snarare än kortsiktiga lösningar.
Öppna svart lådan för läkare och patienter
Eftersom medicinska beslut har höga insatser inkluderar ramverket ett förklaringslager utformat för att visa varför AI:n drar vissa slutsatser. Författarna använder en metod som tilldelar varje indataparameter—såsom ålder, kroppsvikt, blodtryck eller aktivitetsnivå—en bidragspoäng för en given prediktion eller behandlingsförslag. Kliniker kan se visuella sammanfattningar som lyfter fram vilka faktorer som mest påverkade en riskuppskattning eller en rekommenderad terapiförändring. Till exempel kan systemet betona att nyliga blodtrycksspikar och låg aktivitet driver upp riskpoängen, och att detta är skälet till att aktivitetsagenten föreslår mer promenader medan medicinagenten undviker aggressiva nyordinerade läkemedel. Denna transparens syftar till att bygga förtroende, stödja gemensamma vårdbeslut och hjälpa till att förena AI-förslag med kliniska riktlinjer.
Vad detta betyder för personer som lever med kronisk sjukdom
I experiment visade det kombinerade systemet sig vara mer exakt, snabbare att lära sig bra policyer och mer kommunikationseffektivt än befintliga djupinlärnings- eller beslutsmodeller som används på egen hand. Viktigt är att det gör detta samtidigt som rådata hålls nära där de genereras och genom att erbjuda mänskligt läsbara förklaringar till sina val. För patienter kan ett sådant ramverk så småningom upplevas som en ständigt aktiv, integritetsmedveten digital coach som hjälper till att finjustera behandling över läkemedel, måltider, rörelse och mental hälsa och uppdaterar sig i takt med att deras liv förändras. Även om den aktuella studien bygger på retrospektiva datasets och simuleringar pekar den mot framtida hälsosystem där avancerad AI tyst stödjer läkare och patienter att hantera kroniska sjukdomar mer säkert, personligt och effektivt på lång sikt.
Citering: Ahmad, F., AlGhamdi, R. Personalized multi-agent reinforcement learning framework for adaptive chronic disease therapy management. Sci Rep 16, 11025 (2026). https://doi.org/10.1038/s41598-026-41093-2
Nyckelord: hantering av kroniska sjukdomar, personlig medicin, federated learning, förstärkningsinlärning, förklarbar AI