Clear Sky Science · sv
Potentiellt gonadskyddande effekt av sitagliptin mot paclitaxel‑inducerad testikulär dysfunktion via reglering av PERK/CHOP/NLRP3/Sestrin2‑signaleringsvägen
Varför denna studie är viktig för cancerpatienter
Kemoterapi räddar liv men kan i det tysta skada fertiliteten, särskilt hos män. Ett allmänt använt cancerläkemedel, paclitaxel, är känt för att skada testiklarna och försämra spermiekvaliteten. Denna studie på råttor ställer en praktisk fråga med tydlig mänsklig relevans: kan en redan godkänd diabetesmedicin, sitagliptin, återanvändas för att skydda det manliga reproduktionssystemet mot paclitaxels biverkningar utan att störa dess cancerbekämpande effekt?
En vanlig cancerbehandling med en dold kostnad
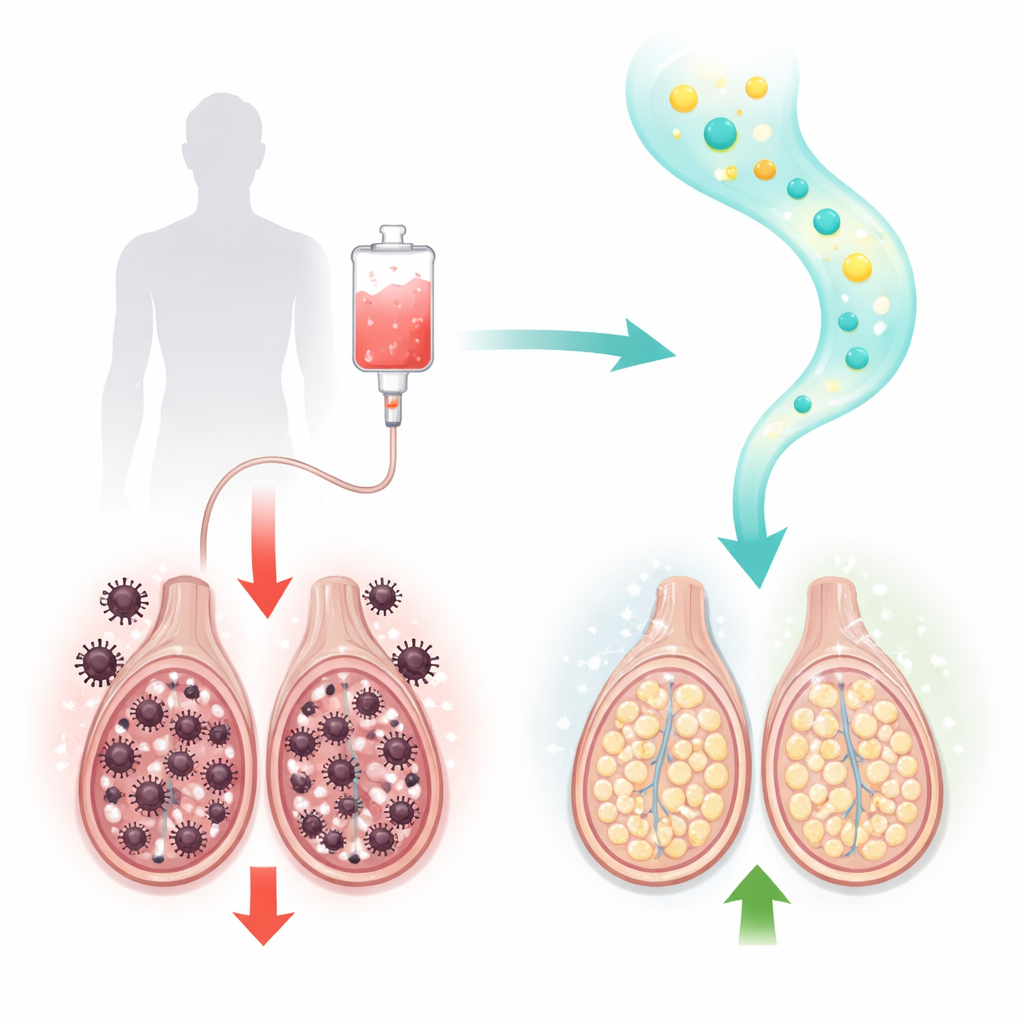
Paclitaxel är en hörnsten i behandlingen av bröst-, äggstocks-, lung- och andra solida tumörer. Den verkar genom att frysa celldelningens maskineri i snabbt växande cancerceller. Tyvärr är delande celler i friska organ också sårbara. Hos hannråttor ledde paclitaxelbehandling till klassiska tecken på testikulär skada: spermieantal, rörlighet och livskraft sjönk kraftigt, samtidigt som andelen missbildade spermier ökade. Under mikroskopet observerade forskarna skadade seminiferösa tubuli (där spermier bildas) och skadade hormonproducerande Leydig‑celler, tillsammans med förtunnade vävnadsskikt. Blodprover bekräftade att testosteron och ett nyckelenzym för dess syntes, 17β‑hydroxysteroiddehydrogenas, var kraftigt reducerade.
En diabetesmedicin som oväntad beskyddare
Sitagliptin används i stor utsträckning för att kontrollera blodsockret hos personer med typ 2‑diabetes. Tidigare studier har antytt att sitagliptin, utöver sina metabola effekter, kan dämpa skadlig oxidativ stress, inflammation och celldöd i organ som lever, njure och hjärna. Byggande på detta delade forskarna in hannråttor i fyra grupper: obehandlade kontroller, en grupp med endast paclitaxel och två grupper som fick paclitaxel plus antingen en lägre eller högre dos sitagliptin i två veckor. De jämförde därefter spermiekvalitet, hormonnivåer, vävnadsstruktur och en uppsättning molekylära ”larmsystem” i testiklarna som känner av stress och utlöser inflammation och programmerad celldöd.
Hur sitagliptin lugnade cellulär stress och inflammation
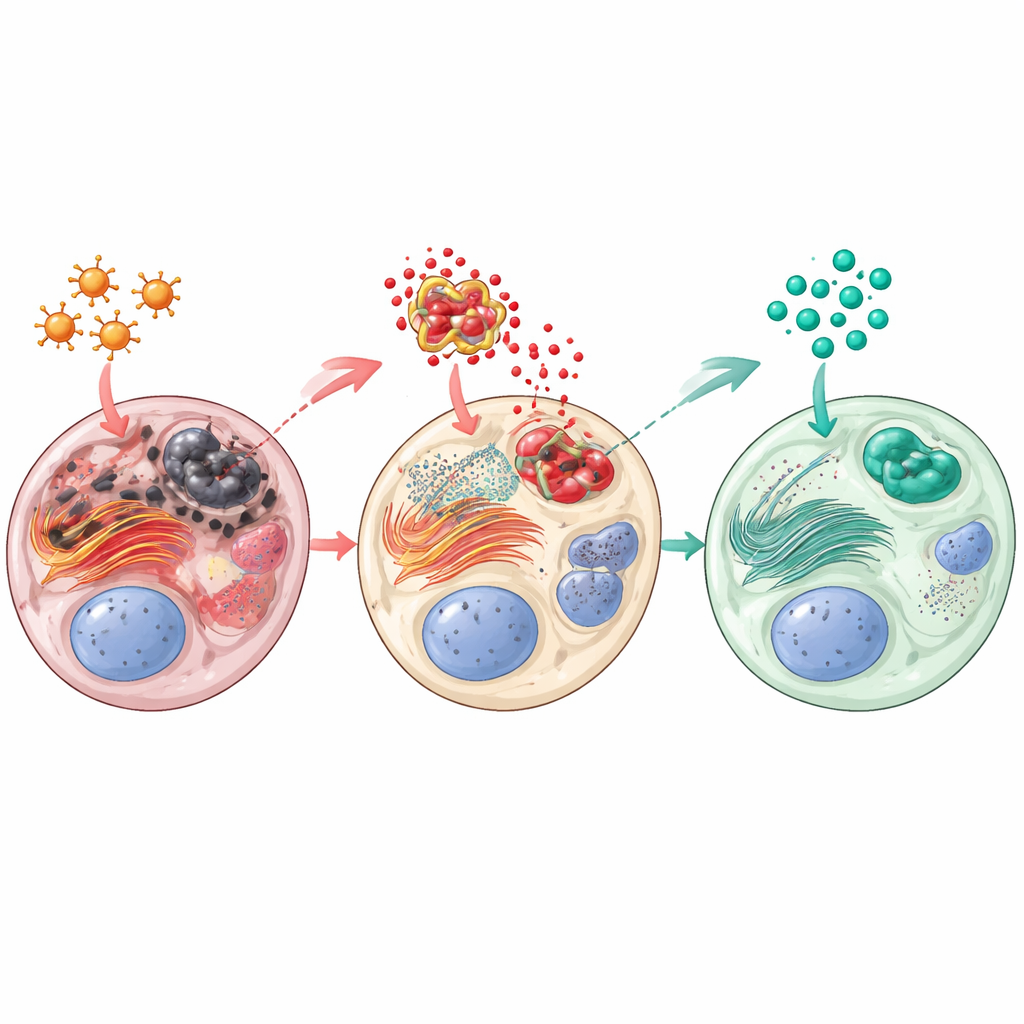
Paclitaxel tvingade testiklarna in i ett tillstånd av oxidativ och intern stress: nivåerna av skadliga biprodukter (mätt som malondialdehyd) steg, medan naturliga försvar som reducerat glutation och enzymet katalas sjönk. Djupt inne i cellerna aktiverades det proteinveckningsmaskineri som kallas det endoplasmatiska retiklet och en farosignal, PERK–CHOP, slog på — ett tecken på att långvarig stress driver celler mot död. Samtidigt blev ett inflammatoriskt proteinkomplex (NLRP3) starkt aktivt, vilket ökade inflammatoriska budbärare som interleukin‑1β och aktiverade en kaskad av apoptosproteiner, inklusive cytokrom c och kaspas‑3. Sitagliptin vände mycket av detta. Båda doserna minskade oxidativ skada och återställde antioxidantförsvar. De sänkte markant aktiveringen av PERK–CHOP‑stressvägen och dämpade NLRP3‑driven inflammation och apoptos. Ett skyddande protein kallat Sestrin2, som hjälper till att rensa reaktiva molekyler och har kopplats till bättre spermiekvalitet, ökade med sitagliptin både på gen‑ och proteinnivå.
Bättre spermier, friskare vävnad, starkare hormoner
De biokemiska förbättringarna översattes till konkreta funktionella vinster. Råttor som fick sitagliptin efter paclitaxel hade fler spermier, bättre rörlighet och färre onormala spermier än djur som enbart fick paclitaxel, där den högre sitagliptindosen närmade sig normalvärden. Testosteron och 17β‑hydroxysteroiddehydrogenas återhämtade sig, vilket tyder på att steroidhormonsyntesen i Leydig‑cellerna höll på att återställas. Under både ljus‑ och elektronmikroskop visade sitagliptinbehandlade testiklar mer ordnade seminiferösa tubuli, fler Leydig‑celler, tjockare och friskare cellskikt samt färre strukturella deformationer. Sammantaget hjälpte läkemedlet till att bevara den arkitektur och funktion som krävs för fortsatt spermatogenes.
Vad detta kan betyda för män som genomgår kemoterapi
Dessa djurstudier tyder på att sitagliptin kan dämpa paclitaxel‑inducerad testikulär skada genom att tysta ett nätverk av skadliga signaler — oxidativ stress, intern proteinveckningsstress, inflammation och programmerad celldöd — till stor del genom att öka Sestrin2 och nedreglera PERK/CHOP/NLRP3‑axeln. Eftersom sitagliptin redan används kliniskt vid diabetes, framstår det som en realistisk kandidat att testa som ett fertilitetsskyddande tillägg hos män som får paclitaxel, särskilt de som också är diabetiker. Författarna betonar att mänskliga studier fortfarande behövs, men deras resultat väcker ett hoppfullt scenario: en välkänd tablett kan en dag hjälpa cancerpatienter att bevara inte bara sina liv utan även möjligheten att bli fäder.
Citering: El-Beheiry, K.M., El-Shitany, N.A., El-Sayad, M.ES. et al. Potential gonadal-beneficial effect of sitagliptin against paclitaxel-induced testicular dysfunction via mediating PERK/CHOP/NLRP3/Sestrin2 signaling pathway. Sci Rep 16, 9090 (2026). https://doi.org/10.1038/s41598-026-40511-9
Nyckelord: paclitaxel, sitagliptin, manlig fertilitet, oxidativ stress, testikulär toxicitet