Clear Sky Science · sv
Störning av neutrofilhomeostas är kopplad till funktionella förändringar i mitokondrier hos kritiskt sjuka COVID-19-patienter
Varför detta är viktigt för COVID-19-patienter
De flesta vet nu att COVID-19 är mer än enbart en lungsjukdom, men hur viruset exakt vänder kroppens egna försvar mot sig håller fortfarande på att klarläggas. Denna studie granskar noggrant neutrofiler, en vanlig typ av vita blodkroppar, hos patienter med livshotande COVID-19 på intensivvård. Genom att undersöka hur dessa celler lever, dör och använder sina små interna ”kraftverk” (mitokondrier) visar forskarna ett mönster av ihållande, överaktiva neutrofiler som kan bidra till att förklara bestående inflammation, blodskador och organskador vid svår sjukdom.
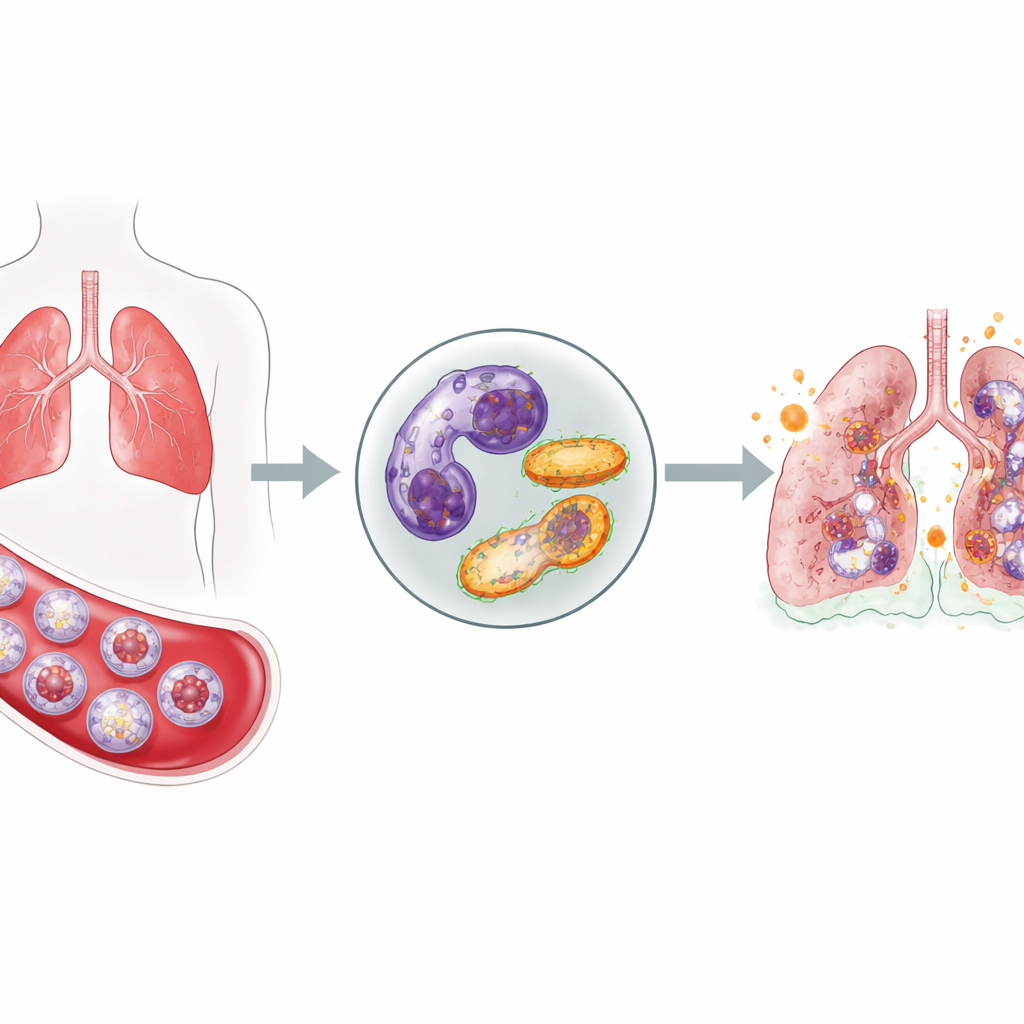
Frontlinjeceller som inte drar sig tillbaka
Neutrofiler är bland kroppens första försvarare mot infektion: de strömmar ut i blodbanan, rör sig in i vävnader och frisätter giftiga molekyler för att döda inkräktande mikrober. Normalt, efter att ha gjort sitt jobb, går de tyst i självdöd och avlägsnas, vilket förhindrar att de skadar frisk vävnad. Hos kritiskt sjuka COVID-19-patienter fann teamet en mycket annorlunda bild. Jämfört med friska frivilliga hade dessa patienter en ökning av neutrofiler i blodet och, viktigt, många av dem var omogna celler som skyndats ut från benmärgen. Samtidigt visade flera tester att färre neutrofiler genomgick sin normala programmerade död, vilket tyder på att dessa aggressiva celler dröjer sig kvar längre än de borde.
Subtila genetiska signaler men ett tydligt överlevnadsmönster
Forskarna undersökte också små regulatoriska molekyler kallade mikroRNA i neutrofiler från intensivvårdspatienter som överlevde respektive avled. Några av dessa molekyler var förändrade på sätt som, på papperet, pekar mot störda vägar som styr celldöd och kalciumbalans. Men när de mätte direkta markörer för celldöd såg de inga stora skillnader mellan överlevare och icke-överlevare—båda grupperna visade liknande minskad neutrofil-självdöd jämfört med friska personer. Det innebär att mikroRNA-mönstren mer är ledtrådar för framtida studier än fasta indikatorer på vem som överlever, och de understryker att den övergripande bristen på att neutrofiler slår av är ett gemensamt inslag vid svår COVID-19.
Kalciumbalans och överladdade kraftverk
För att förstå varför neutrofiler inte dog i tid fokuserade teamet på två nära kopplade system inne i cellerna: kalciumsignaler och mitokondrier. Kalciumjoner fungerar som små av- och på-knappar för många cellbeslut, inklusive när cellen ska gå i självdöd. Forskarna fann att neutrofiler från svåra COVID-19-fall hade mindre fritt kalcium inuti, tillsammans med reducerade nivåer av nyckelproteiner som normalt hjälper till att flytta kalcium in i mitokondrier och öppna en säkerhetsventil som kan utlösa celldöd. Samtidigt var mitokondrierna själva ovanligt ”laddade”, med en högre elektrisk gradient över membranen och ökad syreförbrukning, särskilt genom en huvudsaklig andningsväg. Istället för att stänga ner producerade dessa överaktiva mitokondrier fler reaktiva syremolekyler, som kan skada omgivande vävnad och driva på inflammation.
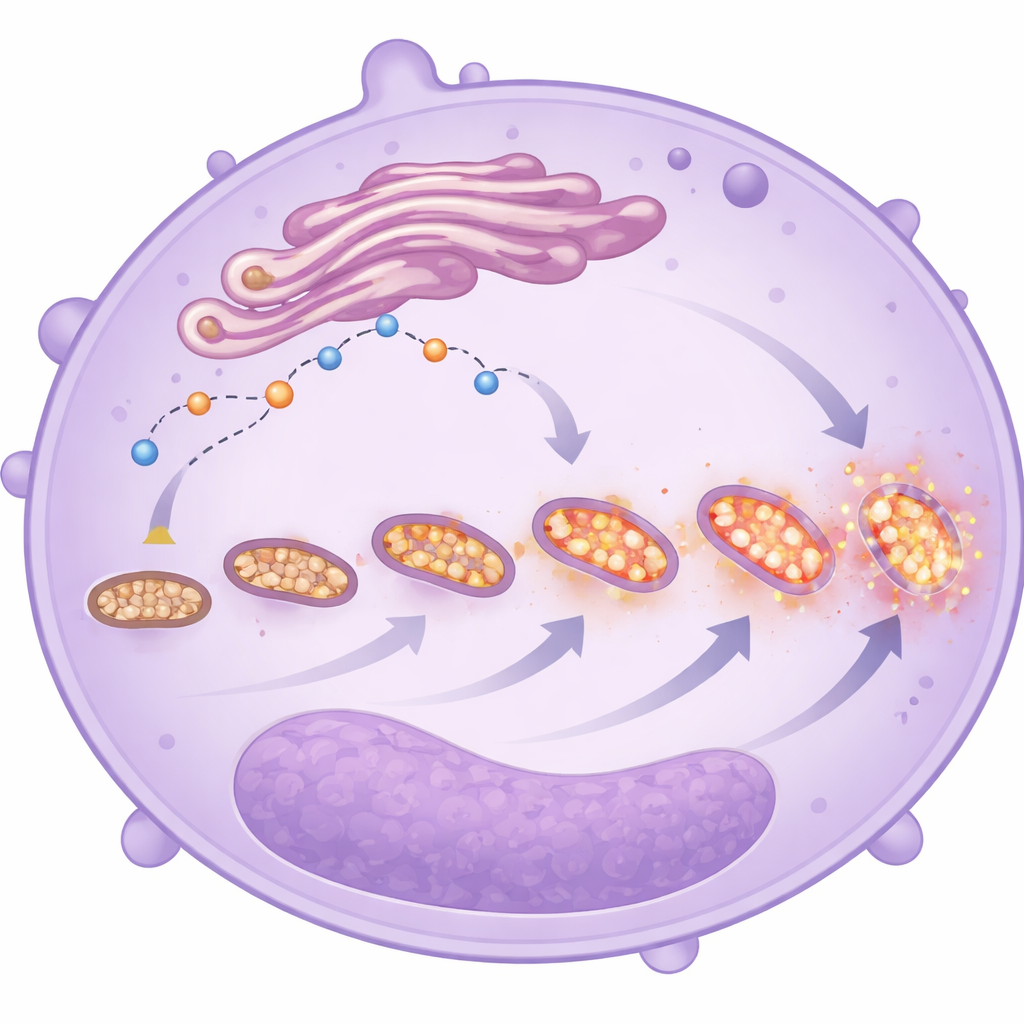
Stressade och fragmenterade mitokondrier
Elektronmikroskopbilder och fluorescerande färgämnen gav en närmare bild av mitokondriernas form och beteende. I neutrofiler från de sjukaste patienterna var mitokondrierna fler men mindre och mer fragmenterade—egenskaper som ofta signalerar stress. Dessa celler visade också högre nivåer av mitokondriella reaktiva syrer, oberoende av om patienten slutligen överlevde eller inte. Tillsammans med förändrad kalciumhantering och fördröjd celldöd målar dessa förändringar upp en bild av neutrofiler som har skiftat sin energistrategi: istället för att främst förlita sig på enkel nedbrytning av socker lutar de mer mot mitokondriell metabolism, särskilt hos omogna celler. Detta byte kan öka deras förmåga att migrera, bestå och släppa ut skadliga molekyler i lungor och andra organ, även om studien inte kan bevisa att de är den direkta orsaken till sämre utfall.
Vad detta kan betyda för framtida vård
Enkelt uttryckt antyder studien att neutrofiler i kritisk COVID-19 blir för många, för unga och för svåra att stänga av. Deras interna kalciumsignaler och mitokondrier omkopplas på ett sätt som håller dem vid liv och mycket aktiva, med utbrott av skadliga syreburna kemikalier. Även om arbetet är observationellt och inte visar orsak och verkan, lyfter det fram flera potentiella ”kontrollratten” i dessa celler—såsom kalciumregulatorer och mitokondriella kontrollpunkter—som en dag skulle kunna riktas för att varsamt få neutrofilerna tillbaka mot normalt beteende. Om framtida forskning bekräftar dessa idéer kan behandlingar som återställer korrekt neutrofilavstängning eller lugnar deras överladdade mitokondrier bidra till att minska de kollaterala skador dessa viktiga celler orsakar vid svår COVID-19 och möjligen vid andra kritiska sjukdomar.
Citering: Elkhodiry, A.A., Yasseen, B.A., El-sayed, H. et al. Disruption of neutrophil homeostasis is associated with functional alterations in mitochondria of critically ill COVID−19 patients. Sci Rep 16, 7838 (2026). https://doi.org/10.1038/s41598-026-38741-y
Nyckelord: COVID-19, neutrofiler, mitokondrier, inflammation, kritisk sjukdom