Clear Sky Science · sv
Katalytisk asymmetrisk funktionalisering av bicyclo[1.1.0]butan‑boronater möjliggjord av 1,2‑oxygenmigration
Varför små fyrhörniga ringar spelar roll
Kemister gillar att bygga nya läkemedel och material genom att sätta ihop små molekylbitar, ungefär som att använda Lego‑klossar. Fyratomiga kolringar kallade cyklobutaner är särskilt eftertraktade eftersom de packar mycket energi och form på liten yta, vilket kan förändra hur ett läkemedel beter sig i kroppen. Denna artikel beskriver ett nytt sätt att tillverka dessa ringar i en mycket kontrollerad, "enhands" (kiral) form, med en smart reaktion som tvingar en syre‑innehållande grupp att hoppa från en atom till en annan. Arbetet öppnar dörrar för att designa mer komplexa och precisa molekyler för läkemedel och avancerade material.
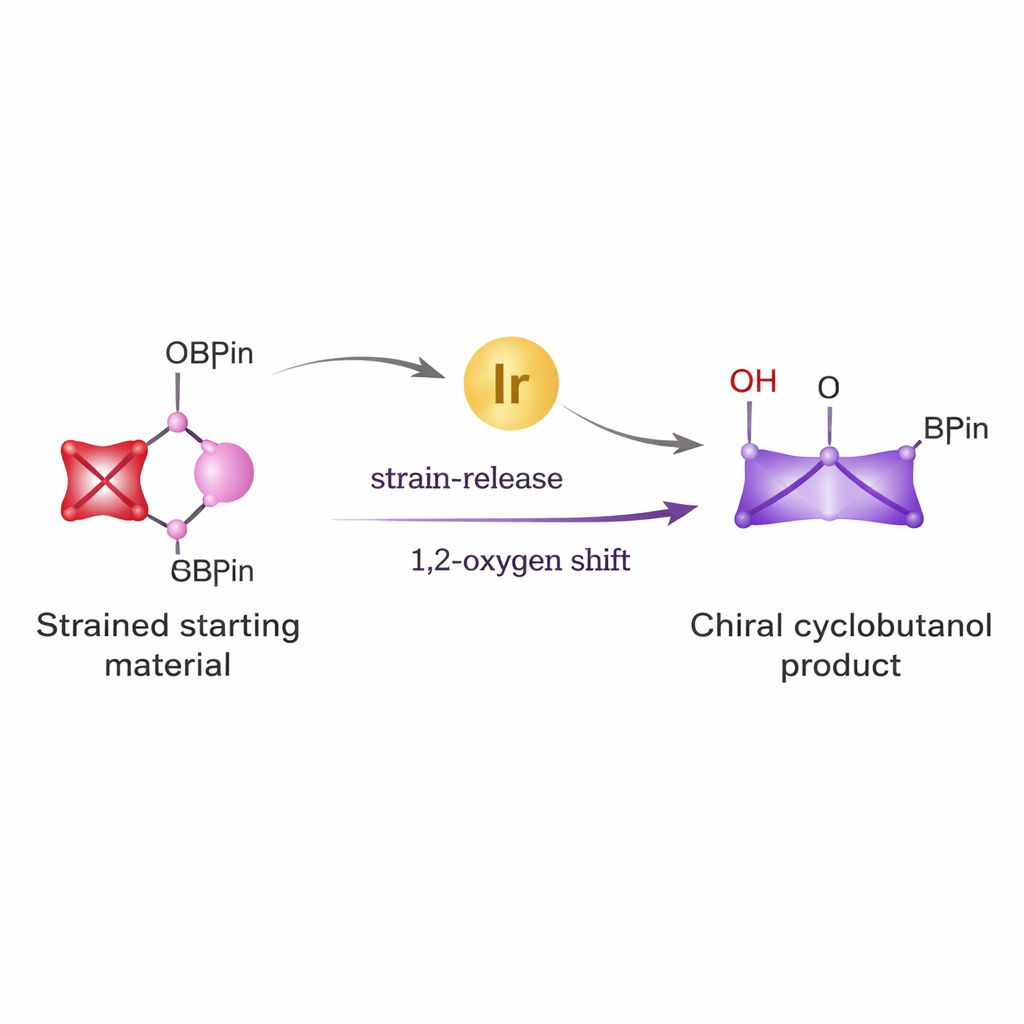
Från enkla byggstenar till kraftfulla ringar
Cyklobutaner förekommer i en mängd antiviralmedel, cancerkandidater och andra bioaktiva molekyler. Att bygga dem med exakt den tredimensionella arrangemang som krävs för läkemedel har dock varit svårt. Traditionella metoder kräver ofta hårda reagenser och ger blandningar av spegelbildsprodukter som är svåra att separera. Författarna ville lösa detta genom att kombinera två starka idéer: den ovanliga reaktiviteten hos en mycket spänd, liten ring kallad bicyclo[1.1.0]butan, och mångsidigheten hos boronater, en välkänd grupp reagenser som ofta används i korskopplingskemi för att bilda kol–kol‑bindningar.
Att vända en nackdel till en ny reaktionsväg
I vanliga metallkatalyserade kopplingsreaktioner bildar boronater ett intermediärt komplex med en alkoxid (en syrebaserad bas). Detta komplex följer nästan alltid en invand rutinväg kallad transmetallation, som sedan leder direkt till nya kol–kol‑ eller kol–halogen‑bindningar. Denna "standard"‑väg har gjort det svårt att utforska andra möjligheter, som att förflytta syregruppen själv. Teamet insåg att om de började från en ringspänd bicyclo[1.1.0]butan‑boronat, kunde den inneboende spänningen i den lilla ringen användas för att överskrida den vanliga vägen. Genom att kombinera detta spända system med en iridiumkatalysator och en noggrant utvald kiral ligand hoppades de kunna få syret att migrera kontrollerat, samtidigt som ringen öppnades och åter sluts till en cyklobutan.
En stegvis dans styrd av spänning
Experiment bekräftade att strategin fungerar. Genom att använda litiumalkoxider framställda från en mängd olika alkoholtyper — inklusive sockerarter, terpener, steroider och enkla alifatiska alkoholer — omvandlade författarna bicyclo[1.1.0]butan‑boronater till cis‑cyklobutanoler med både hög utbyte och utmärkt kontroll över kiraliteten. Iridiumkatalysatorn bildar först ett reaktivt allylkomplex från en allylkarbonatpartner. Detta komplex angriper sedan det spända bicyclo[1.1.0]butan‑systemet och bildar en ny kol–kol‑bindning när den lilla ringen öppnas. Viktigt är att det resulterande borinnehållande intermediäret, istället för att omedelbart följa den vanliga transmetallationsvägen, genomgår en subtil rotation av kol–bor‑bindningen som placerar den bundna syregruppen så att den kan förskjutas rent till en intilliggande kolatom. Denna 1,2‑oxygenmigration låser in den önskade cis‑arrangemanget i den nya cyklobutanringen.
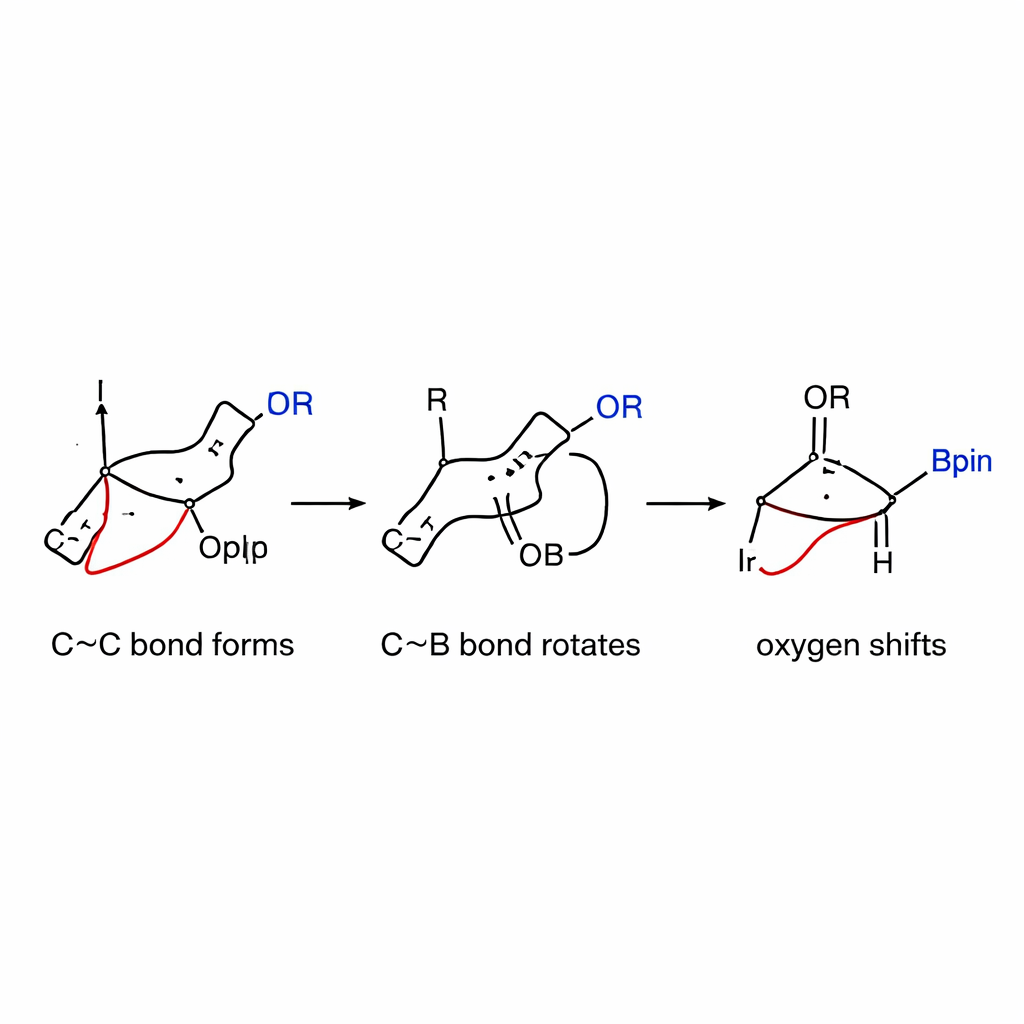
En titt under huven på mekanismen
För att förstå varför reaktionen är så selektiv kombinerade författarna kinetiska mätningar med detaljerade datorsimuleringar. De fann att det långsamma, hastighetsbestämmande steget är den initiala kol–kol‑bindningsbildningen mellan iridium–allyl‑arten och det spända boronatkomplexet, inte den tidigare aktiveringen av allylkarbonaten. Elektroniska tester visade att allylpartners som stabiliserar positiv laddning reagerar snabbare, vilket stöder en mekanism där ett delvis laddat intermediär bildas. Beräkningar visade vidare att rotation runt kol–bor‑bindningen — tidigare trodd att vara svår — har en överraskande låg energi barriär i detta system tack vare den lagrade ringspänningen. När rotationen har inriktat syregruppen fortskrider 1,2‑skiftet smidigt och föredrar cis‑produkten framför den vanligare trans‑formen.
Nya verktyg för att forma framtidens läkemedel
Utöver att bevisa en mekanistisk poäng levererar reaktionen mångsidiga produkter. Cyklobutanolerna behåller en boronatgrupp som kan omvandlas till många andra funktionella grupper med etablerad kemi. Författarna visade flera "late‑stage"‑modifieringar, som hydrering, oxidation, olefinmetates och ytterligare kopplingar, samtidigt som ringens precisa tredimensionella form bevaras. Enkelt uttryckt förvandlar detta arbete en tidigare problematisk sidoväg — oxygenmigration i boronatkomplex — till ett kraftfullt syntetiskt verktyg. Genom att utnyttja ringspänning och en finjusterad iridiumkatalysator ger forskarna kemister ett pålitligt sätt att bygga komplexa, kirala cyklobutaner som kan spela nyckelroller i nästa generations läkemedel och avancerade molekylära material.
Citering: Zhu, XY., Ji, CL., Dong, TG. et al. Catalytic asymmetric functionalization of bicyclo[1.1.0]butane boronic esters enabled by 1,2-oxygen migration. Nat Commun 17, 1941 (2026). https://doi.org/10.1038/s41467-026-69860-9
Nyckelord: cyklobutan, organobor‑kemi, asymmetrisk katalys, bicyclobutan, oxygenmigration