Clear Sky Science · sv
Tumörspecifik HORMAD1‑uttryck stör mitotisk arrest och ökar känsligheten för hämmare av mitotiska kinaser
Varför detta är viktigt för cancerbehandling
När våra celler delar sig förlitar de sig på finjusterade säkerhetskontroller för att föra vidare rätt uppsättning kromosomer. Cancer kapar ofta eller försvagar dessa skyddsmekanismer, vilket leder till kaotiska genom som både driver sjukdomen och påverkar hur tumörer svarar på läkemedel. Denna studie avslöjar hur ett ovanligt protein kallat HORMAD1, som normalt är aktivt endast i reproduktiva celler, återaktiveras i många aggressiva bröstcancerformer och andra tumörer. Genom att subtilt sabotera en viktig kontrollpunkt i celldelningen gör HORMAD1 cancerceller mer instabila — men också ovanligt sårbara för en ny klass experimentella läkemedel.
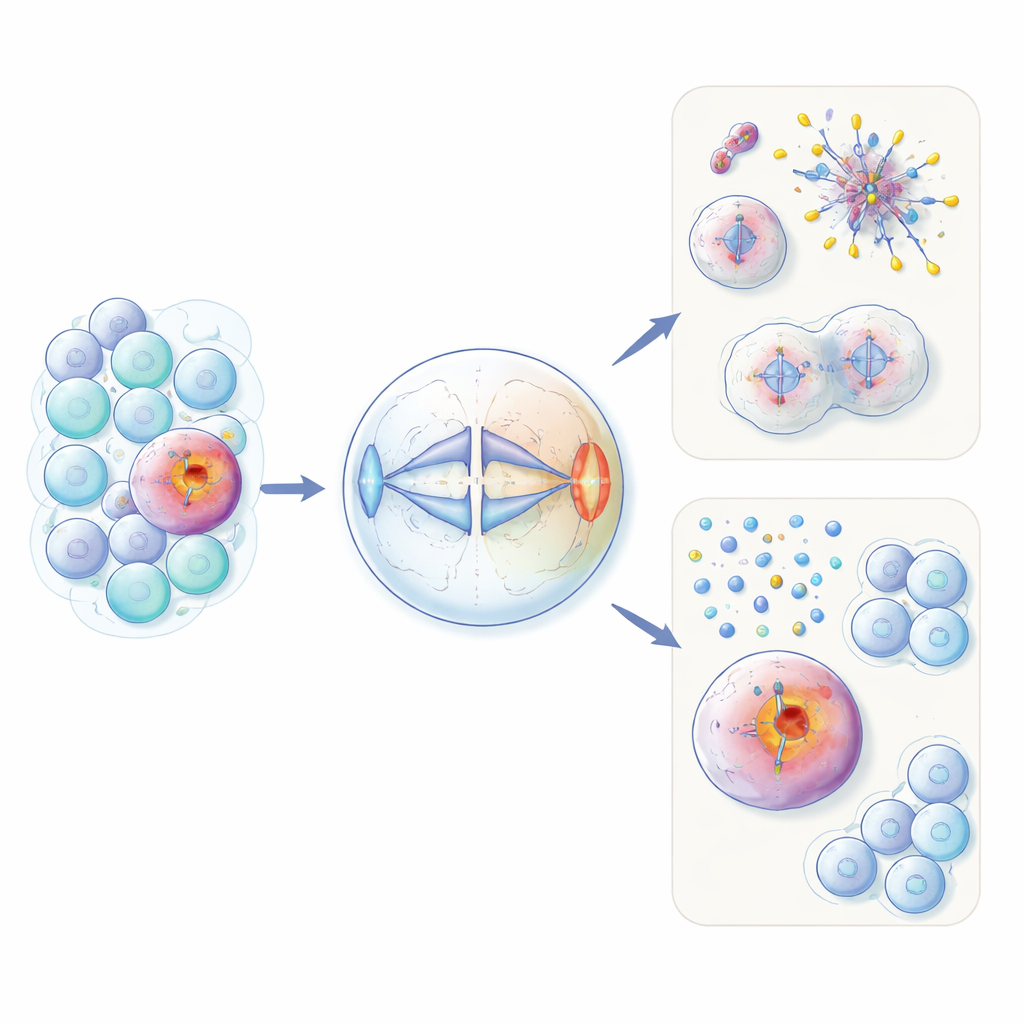
En felplacerad fertilitetsprotein i cancerceller
HORMAD1 förekommer normalt endast i germinalceller, där ägg och spermier bildas. Där hjälper det till att hantera DNA‑omstöpning och kvalitetskontroll under den speciella celldelningen meios. Författarna visar att i ungefär 60 % av trippelnegativa bröstcancerfall — och i delmängder av flera andra tumörtyper — återaktiveras detta protein på ett olämpligt sätt. Med hjälp av både konstruerade icke‑cancerösa celler och cancercellinjer fann de att överskott av HORMAD1 stör en jämn separation av kromosomer under vanlig mitos. Celler som uttryckte HORMAD1 utvecklade fler eftersläpande kromosomer, extra eller saknade kromosomer (aneuploidi) och små DNA‑innehållande «mikronukleier», alla kännetecken för genomisk oreda som ses i aggressiva cancerformer.
Hur kontrollpunkter i celldelning normalt fungerar
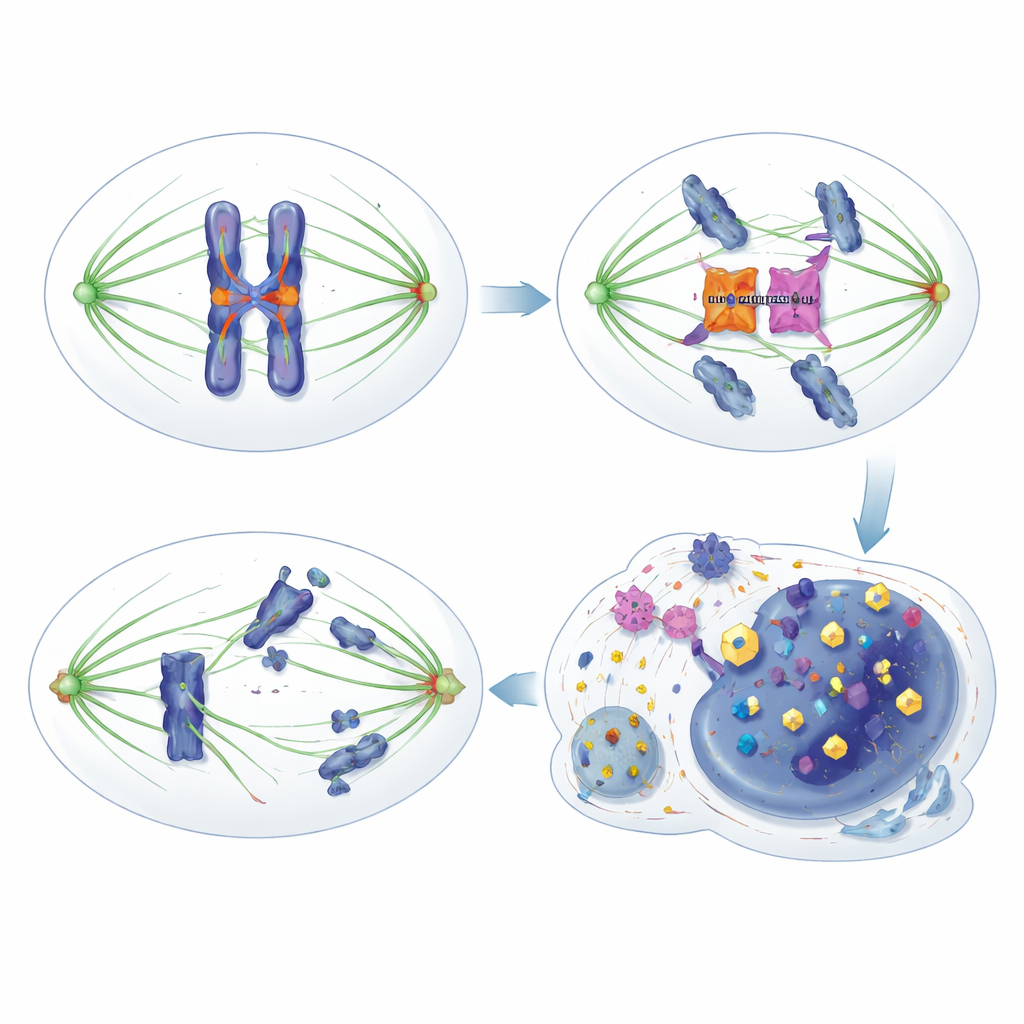
För att dela sig korrekt bygger en cell ett spindelnät av mikrotubuli som fäster vid varje kromosom. Ett övervakningssystem känt som spindelmonteringskontrollen fungerar som en spänningskänslig broms: om någon kromosom inte är korrekt fäst blockerar bromsen framsteg och förhindrar separation tills felen är rättade. Flera enzymer kända som mitotiska kinaser, inklusive MPS1, Aurora B och BUB1, hjälper till att upptäcka felaktiga fästen och främja »felkorrigering» så att varje dottercell får rätt kromosomuppsättning. Störning av detta system kan både driva cancerutveckling och skapa särskilda svagheter som vissa läkemedel kan utnyttja.
HORMAD1 försvagar diskret bromsen
Forskarna upptäckte att HORMAD1 undergräver denna säkerhetsbroms på ett subtilt men betydelsefullt sätt. Istället för att störa klassiska kontrollpunktskomponenter som HORMA‑proteinet MAD2L1 binder HORMAD1 direkt till kinasen Aurora B. Aurora B samarbetar normalt med ett annat protein, INCENP, för att bli fullt aktiv och modifiera proteiner vid centromerer och kinetokorer — kritiska platser på kromosomer där spindelfibrer fäster. När HORMAD1 finns i delande tumörceller konkurrerar det med INCENP om åtkomst till Aurora B, vilket minskar deras samarbete och dämpar Aurora B:s aktivitet. Som en följd försvagas Aurora B:s vanliga fosforyleringssignaler på flera mål, felkorrigeringen blir mindre effektiv och kontrollpunkten blir »läckande»: celler lämnar mitos för tidigt, även när fästena är felaktiga, vilket leder till felaktig fördelning av kromosomer och genomisk instabilitet.
Från svaghet till terapeutisk möjlighet
Eftersom HORMAD1 endast delvis inaktiverar Aurora B och relaterade skyddsmekanismer förblir cancercellerna precis tillräckligt livskraftiga för att växa, men blir starkt beroende av den kvarstående funktionen hos mitotiska kinaser för att överleva upprepade felaktiga delningar. Teamet testade detta genom att exponera HORMAD1‑positiva och HORMAD1‑negativa celler för experimentella hämmare av MPS1, Aurora B och BUB1. I flera modeller gjorde HORMAD1‑uttryck cellerna mycket mer känsliga för dessa läkemedel, vilket dramatiskt minskade deras förmåga att proliferera eller bilda kolonier. Genetisk utarmning av BUB1 var särskilt dödlig endast i närvaro av HORMAD1, vilket avslöjar ett starkt, selektivt beroende. I musemodeller med patient‑härledda trippelnegativa brösttumörer krympte eller växte tumörer med höga HORMAD1‑nivåer långsammare när de behandlades med en nanopartikelformulering av en Aurora B‑hämmare, medan HORMAD1‑negativa tumörer till stor del var motståndskraftiga mot samma behandling.
Vad detta betyder för patienter
För en lekmannabetraktare fungerar HORMAD1 som ett tveeggat svärd i cancer: det driver tumörceller mot större kromosomal oordning, vilket kan främja sjukdom, men i och med det gör det dem också osäkert beroende av ett fåtal kvarvarande skyddsmekanismer i celldelningen. Studien visar att detta felplacerade fertilitetsprotein försvagar en nyckelkontrollpunkt genom att felrikta Aurora B, vilket gör HORMAD1‑positiva tumörer särskilt sårbara för läkemedel som riktar sig mot Aurora B, MPS1 eller BUB1. Eftersom HORMAD1 i stort sett saknas i normala vävnader men förekommer i en tydlig delmängd av tumörer kan det fungera som en biomarkör för att identifiera patienter som sannolikt har nytta av dessa framväxande inhibitorer av mitotiska kinaser, och därigenom öppna nya riktade behandlingsvägar för svårbehandlade cancerformer som trippelnegativ bröstcancer.
Citering: Walker, C., Kollarovic, G., Weekes, D. et al. Tumour specific HORMAD1 expression perturbs mitotic arrest and drives sensitivity to mitotic kinase inhibitors. Nat Commun 17, 2157 (2026). https://doi.org/10.1038/s41467-026-69561-3
Nyckelord: HORMAD1, trippelnegativ bröstcancer, kromosomal instabilitet, Aurora B‑kinas, inhibitorer av mitotiska kontrollpunkter