Clear Sky Science · sv
Heterobifunktionella proteomimetiska polymerer för målinriktad nedbrytning av MYC och KRAS
Nya verktyg för att fälla cancerns svåraste proteiner
Många av de farligaste cancerdrivande proteinerna, som MYC och KRAS, har länge benämnts ”obehandlingsbara” eftersom läkemedel inte lätt kan fästa vid dem. Denna studie presenterar en ny typ av mjukt, syntetiskt material—kallat HYDRAC-polymerer—som kan fånga dessa svårgreppade proteiner och skicka dem till cellens sophanteringssystem. För läsaren ger arbetet en inblick i hur kemi och nanoteknik kan öppna behandlingsmöjligheter för cancerformer som stått emot traditionella läkemedel.
Ett flexibelt ramverk i stället för en enda tablett
De flesta målinriktade cancerläkemedel är små molekyler som passar i fickor på ett proteins yta, ungefär som en nyckel i ett lås. Men proteiner som MYC är sladdriga och saknar bra fickor, medan KRAS ofta muterar på sätt som gör klassiska läkemedel verkningslösa. Författarna designade i stället långa, kedjeliknande polymerer byggda av upprepade enheter. Längs dessa kedjor fäster de två slags komponenter: korta proteinbindande segment som känner igen ett mål som MYC eller RAS, och ”degron”-segment som rekryterar cellens eget nedbrytningsmaskineri. Eftersom många kopior av varje komponent pryder samma kedja kan en enda HYDRAC-molekyl nå ut till flera proteiner och enzymer samtidigt—något som är svårt att åstadkomma med en enda, stel läkemedelsmolekyl.
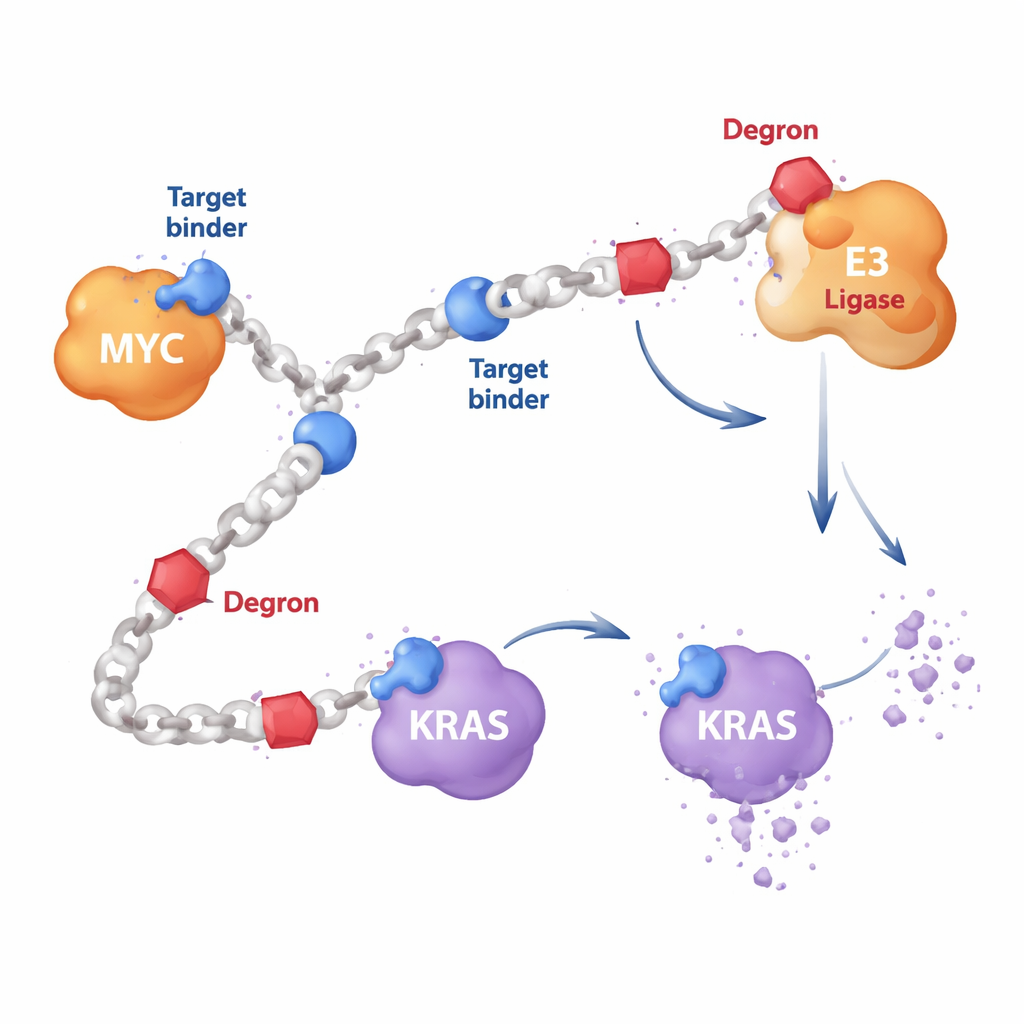
Att lära celler att tugga upp MYC
Som ett första test fokuserade forskarna på MYC, en huvudregulator som driver tillväxt i många cancerformer men som i årtionden motsatt sig direkt angrepp. De byggde HYDRAC-polymerer som visade upp en känd MYC-bindande peptid tillsammans med ett enkelt degronmotiv som märker proteiner för förstörelse av cellens proteasom, dess huvudsakliga proteinskärare. I provrörsexperiment vecklade dessa polymerer ihop sig till kompakta, proteinlika former och band tätt till MYC men inte till orelaterade proteiner. I cancerceller tog HYDRACs sig lätt in, störde MYC-styrda genprogram och utlöste celldöd—effekter som beroende av att både target- och degron-komponenterna fanns på samma polymerkedja.
Från cellkultur till krympande tumörer
I celler ledde HYDRAC-behandling till att MYC-proteinnivåerna föll kraftigt utan att MYC:s RNA minskade, vilket tyder på verklig nedbrytning snarare än enkel nedreglering. Blockering av proteasomen eller nyckelenzymer som aktiverar vissa nedbrytningsvägar återställde MYC-nivåerna, vilket visar att polymererna fungerar genom att omdirigera cellens egna sophanteringssystem. Proteomövergripande analyser visade att mycket få andra proteiner påverkades, vilket tyder på anmärkningsvärd selektivitet. I musemodeller med MYC-drivna tumörer ansamlades fluorescerande märkta HYDRACs i tumörer efter injektion och blev kvar där i flera dagar. Upprepad dosering bromsade tumörtillväxt utan större viktnedgång eller uppenbara vävnadsskador, och tumörprover visade färre delande celler och fler tecken på programmerad celldöd.
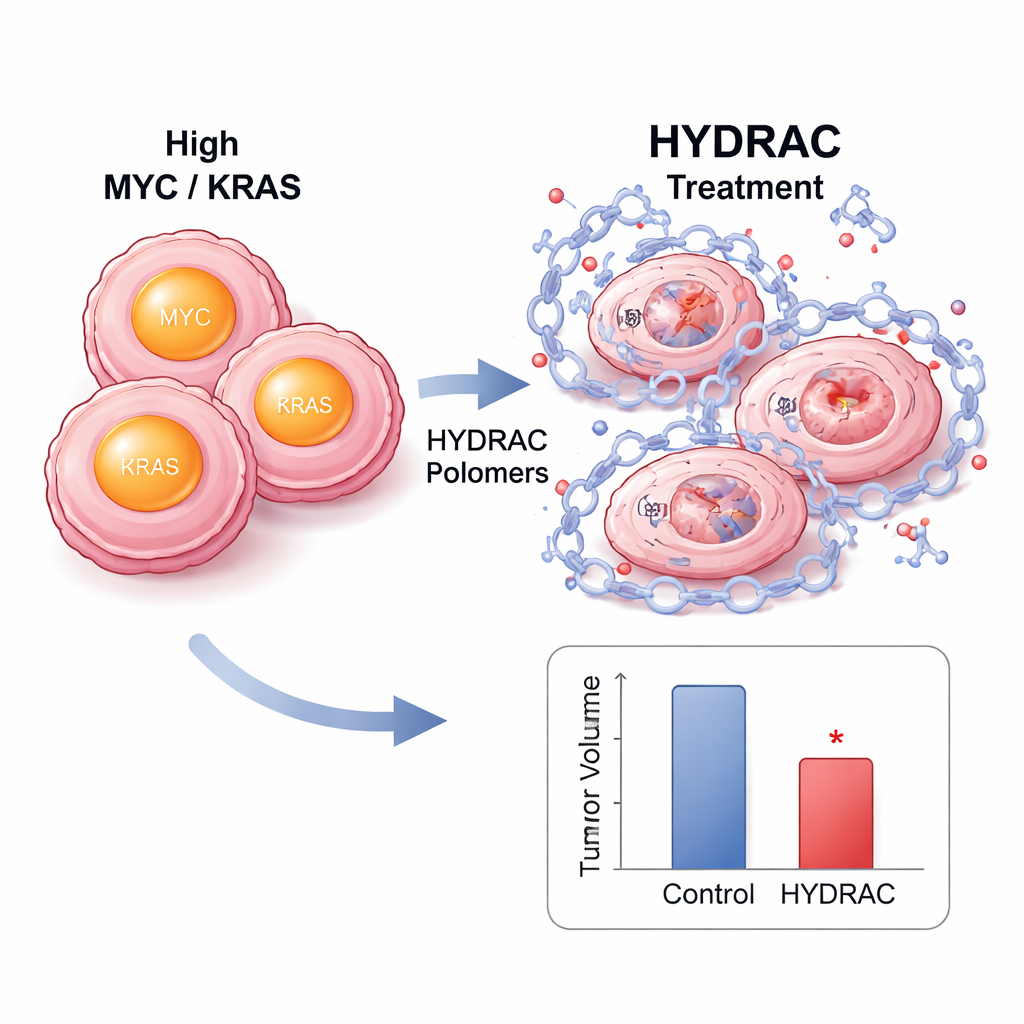
En plug-and-play-plattform för många sjukdomsmål
En styrka med HYDRAC-konceptet är att dess sidogrupper kan bytas ut som utbytbara delar. Teamet ersatte det ursprungliga degronet med andra rekryteringselement som anropar olika cellulära enzymer, inklusive de som känner igen läkemedlet talidomid. Varje version degraderade MYC endast när det avsedda enzymet var närvarande och funktionellt, vilket bekräftar att polymererna kan ställas in för att använda skilda cellulära vägar. För att testa generell tillämpbarhet byggde forskarna sedan RAS‑riktade HYDRACs med en peptid som känner igen RAS‑proteiner. Dessa konstruktioner degraderade framgångsrikt mutant KRAS i två olika cancercellinjer, vilket antyder en potentiell ”pan‑KRAS”-effekt som inte är beroende av en specifik mutation—ett viktigt steg för cancerformer där många KRAS‑varianter samexisterar.
Varför detta spelar roll för framtidens cancerbehandling
Detta arbete introducerar HYDRACs som en ny klass programmerbara material som inte bara blockerar besvärliga proteiner—de hjälper celler att radera dem. Genom att kombinera många mål- och nedbrytningsenheter på en flexibel polymer kringgår HYDRACs designbegränsningarna hos traditionella småmolekylära läkemedel och PROTACs, som vanligtvis bara kan bära en av varje. Mycket återstår innan dessa material når kliniken, men resultaten i MYC‑ och KRAS‑drivna modeller tyder på att länge ansedda ”obehandlingsbara” cancerproteiner faktiskt kan vara sårbara när medicin ser mer ut som en skräddarsydd molekylär borste än en enda liten tablett.
Citering: Wang, M.M., Truica, M.I., Gattis, B.S. et al. Heterobifunctional proteomimetic polymers for targeted degradation of MYC and KRAS. Nat Commun 17, 1706 (2026). https://doi.org/10.1038/s41467-026-68913-3
Nyckelord: målinriktad proteinnedbrytning, MYC, KRAS, polymerterapeutika, cancernanomedicin