Clear Sky Science · sv
Integrativ epigenomisk karta över Alzheimer‑hjärnor avslöjar oligodendrocyt‑molekylära störningar kopplade till tau
Varför denna hjärnforskning är viktig
Alzheimers sjukdom är mest känd för minnesförlust och ansamlingen av två problematiska proteiner i hjärnan: amyloid och tau. Ändå kan personer med Alzheimer uppvisa mycket olika skademönster, även vid samma diagnos. Denna studie ställer en central fråga: vilka omkopplare inne i hjärnceller hjälper till att bestämma hur mycket av dessa skadliga proteiner som byggs upp, och hur de påverkar olika celltyper? Genom att undersöka kemiska markörer på DNA i hundratals hjärnor avslöjar forskarna en överraskande koppling mellan tau och de celler som får hjärnans ledningsnät att fungera.
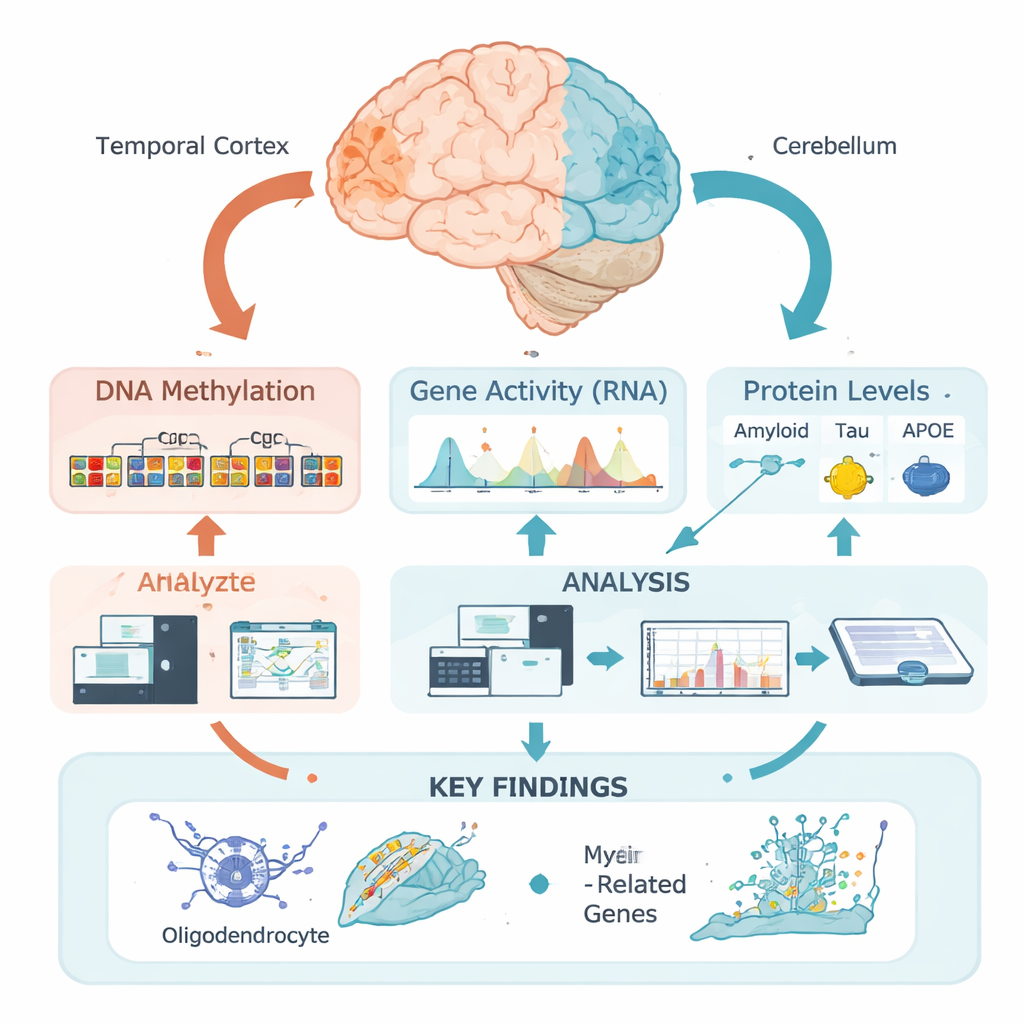
Kemiska märken på DNA som dolda omkopplare
Vårt DNA bär de grundläggande instruktionerna för att bygga och driva hjärnceller, men dessa instruktioner styrs av epigenetiska markörer—kemiska etiketter som kan skrälla upp eller ner närliggande gener utan att förändra den genetiska koden. En av de viktigaste markörerna är DNA‑metylering, där små kemiska grupper fäster vid specifika DNA‑platser. Istället för att undersöka enstaka platser isolerat använde detta team ett nytt ”regionalt” förhållningssätt: de grupperade många närliggande platser i funktionella zoner baserat på hur DNA är paketerat i temporalloben, en region som är starkt påverkad vid Alzheimer, och i lillhjärnan, som är relativt sparad. Detta gjorde det möjligt för dem att fråga var, i biologisk mening, metyleringsmönster förändras i relation till sjukdomsdrag.
Att koppla DNA‑märken till Alzheimers proteiner
Forskarna analyserade hjärnvävnad från 472 personer som hade Alzheimer bekräftat efter döden. För varje prov från temporalloben mätte de detaljerade nivåer av amyloid, tau och APOE‑proteiner i olika biokemiska former, liksom klassiska mikroskopiska poäng för amyloidplack och tau‑trassel. De utförde sedan epigenom‑omfattande associationsstudier för att testa om regionala DNA‑metyleringsnivåer korrelerade med dessa mätningar. Slående nog var nästan alla starka associationer de fann kopplade inte till amyloid, utan till tau—särskilt till totalt lösligt tau och en membranbunden fosforylerad (kemiskt modifierad) form som anses särskilt toxisk.
En stark signal i hjärnans ledningsceller
Många av de DNA‑regioner som var kopplade till tau låg i ”aktiva” delar av genomet som påverkar närliggande gener. Genom att kombinera metyleringsdata med genaktivitetsmätningar från samma hjärnor visade teamet att dessa regioner ofta styrde gener som används av oligodendrocyter—cellerna som sveper nervfibrer i isolerande myelin och möjliggör snabba och pålitliga elektriska signaler. Viktiga myelinrelaterade gener såsom MBP, MAG och MYRF, tillsammans med Alzheimers riskgen BIN1 och en nyare kandidatgen kallad LDB3, dök upp i denna uppsättning. Högre nivåer av toxiskt fosforylerat tau tenderade att sammanfalla med mer metylering i dessa regioner och lägre uttryck av de relaterade oligodendrocyt‑ och myelingenerna, medan den mindre skadliga poolen av lösligt totalt tau visade motsatt mönster.
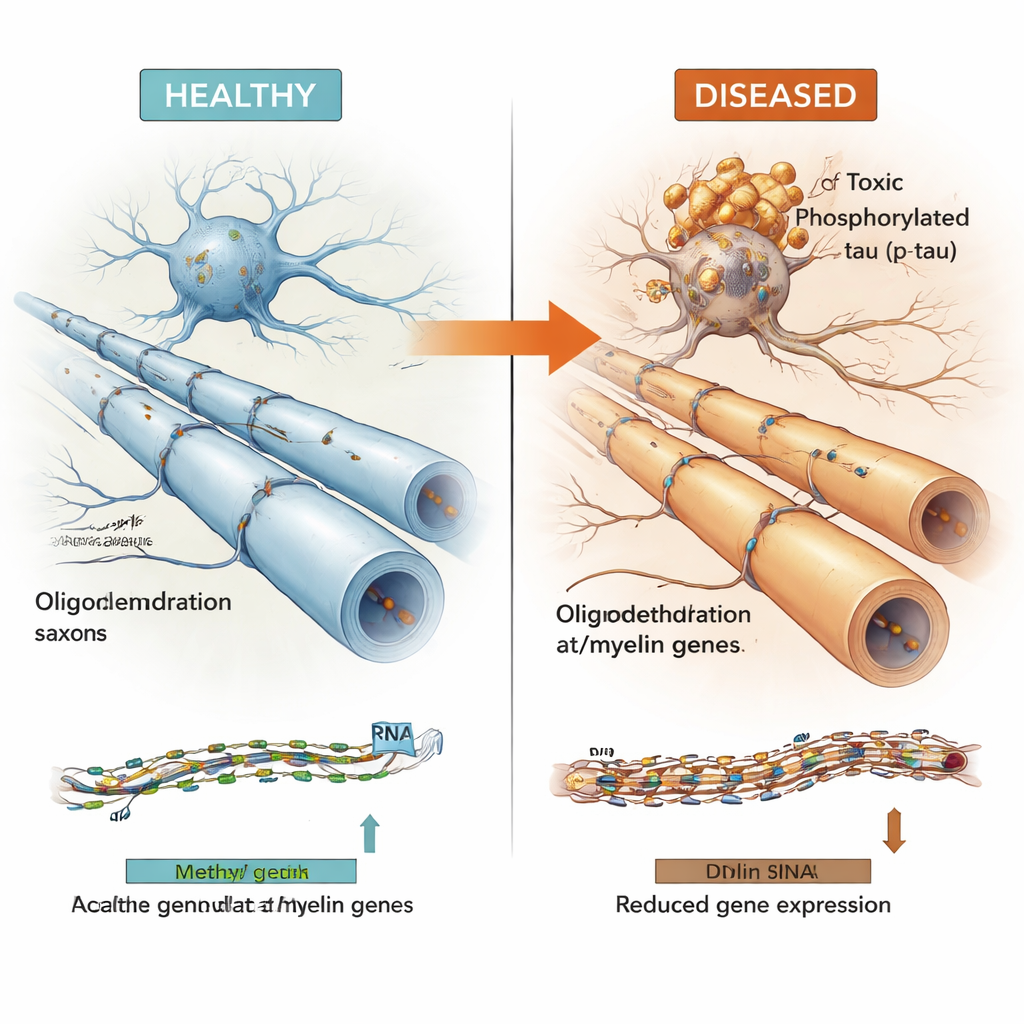
Ett mönster som ses över flera hjärnsjukdomar
För att pröva om dessa fynd var robusta och generella granskade författarna stora, oberoende dataset från andra Alzheimer‑hjärnsamlingar och från hjärnor drabbade av primära ”tauopatier” som progressiv supranukleär paralys och Picks sjukdom. Trots att dessa kohorter mättes med olika teknologier och ofta i andra hjärnregioner visade många av samma DNA‑regioner och oligodendrocytgener konsekvent beteende: deras metyleringsnivåer relaterade till tau‑trasselbörda, och deras uttryck var reducerat i sjuka hjärnor och i single‑cell‑studier som särskilt fokuserade på oligodendrocyter. Viktigt är att dessa mönster inte verkade förklaras enbart av genetik eller av en generell celldöd, vilket tyder på ett genuint epigenetiskt skifte i hur oligodendrocyter fungerar.
Vad detta betyder för förståelsen av Alzheimer
Tillsammans stödjer resultaten en modell där stigande nivåer av skadligt tau är nära kopplade till epigenetiska förändringar i oligodendrocyter som dämpar myelin‑relaterade gener, vilket potentiellt försvagar hjärnans ledningsnät och bidrar till kognitiv försämring. Det är fortfarande oklart vad som kommer först—tau‑ansamling eller störning av dessa myelingener—men de täta, upprepade associationerna över tusentals prover och flera sjukdomar pekar mot en delad mekanism. Genom att kartlägga dessa DNA‑omkopplare och integrera dem i en offentlig ”Multiomic Atlas” framhäver detta arbete oligodendrocyter och deras epigenetiska reglering som lovande mål för framtida terapier som syftar till att stabilisera hjärnans kretsar, i stället för att enbart fokusera på neuroner eller amyloidplack.
Citering: Oatman, S.R., Reddy, J.S., Atashgaran, A. et al. Integrative epigenomic landscape of Alzheimer’s Disease brains reveals oligodendrocyte molecular perturbations associated with tau. Nat Commun 17, 2116 (2026). https://doi.org/10.1038/s41467-026-68864-9
Nyckelord: Alzheimers sjukdom, tau‑protein, DNA‑metylering, oligodendrocyter, myelin