Clear Sky Science · sv
Strukturell grund för mänsklig zink‑aktiverad kanal (ZAC) signalering och modulering
Hur ett spårmetall hjälper nervceller att kommunicera
Zink är mest känt som ett näringsämne i multivitamintabletter, men i kroppen fungerar denna metall också som en snabb kemisk budbärare i hjärnan. Den här studien avslöjar, med atomupplösning, hur ett relativt okänt protein kallat zink‑aktiverad kanal (ZAC) känner av zink utanför cellerna och omvandlar den signalen till ett elektriskt svar. Att förstå denna speciella grind i cellmembranet kan klargöra hur zink formar hjärnans aktivitet och ge ledtrådar till nya sätt att finjustera nervsignaler i hälsa och sjukdom.
En särskild grind för zinksignaler
Många snabba meddelanden mellan nervceller förs av välkända kemikalier som serotonin eller acetylkolin, vilka öppnar ringformade kanaler i cellmembranet. ZAC är en avlägsen släkting till dessa receptorer, men istället för att reagera på ett organiskt ämne aktiveras den av metalljoner som zink, koppar och protoner. ZAC finns i många mänskliga vävnader, inklusive hjärnan, men saknas hos vanliga försöksdjur som möss och råttor, vilket har bromsat framstegen. Detta arbete använder högupplöst kryo‑elektronmikroskopi för att fånga flera tredimensionella ögonblicksbilder av mänsklig ZAC: i dess vilotillstånd, med zink bunden och med två olika läkemedel som stänger kanalen. Tillsammans visar dessa strukturer hur zink fäster vid kanalens topp, hur joner passerar och hur blockare klämmer igen grinden eller kilas in i ett icke‑ledande tillstånd.
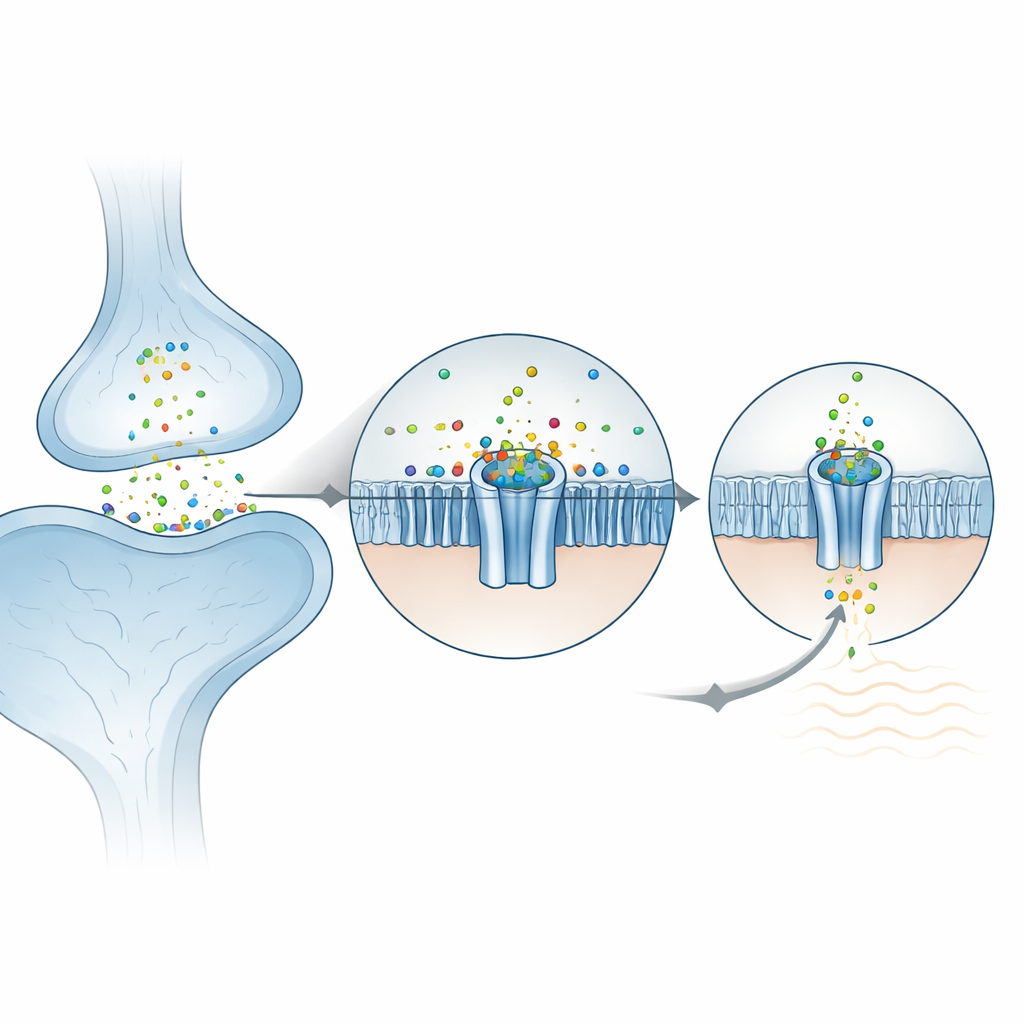
Hur zink låser sig i kanalen
På cellens yta bygger ZAC upp sig av fem identiska subenheter som bildar en rosett. Forskarnas data visar att zinkjoner lägger sig i fem motsvarande fickor, vardera belägen mellan två närliggande subenheter i den yttre domänen. Överraskande nog hålls inte zinket av de vanliga "greppande" aminosyrorna som vanligtvis binder metaller (såsom histidin eller cystein). Istället vilar det huvudsakligen mot två ringformade, aromatiska sidokedjor som stabiliserar den positivt laddade jonen genom så kallade kation–π‑interaktioner. När dessa nyckelresiduers byttes ut i grodäggsceller som användes för elektriska mätningar blev kanalen oresponsiv mot zink, vilket bekräftar deras centrala roll. Den omgivande miljön är redan förorganiserad, vilket hjälper förklara varför ZAC uppvisar märkbar spontan aktivitet även utan zink: proteinet ligger nära balanspunkten mellan stängt och öppet och zink skjuter helt enkelt över växeln.
Jonernas väg och en vanlig genetisk variant
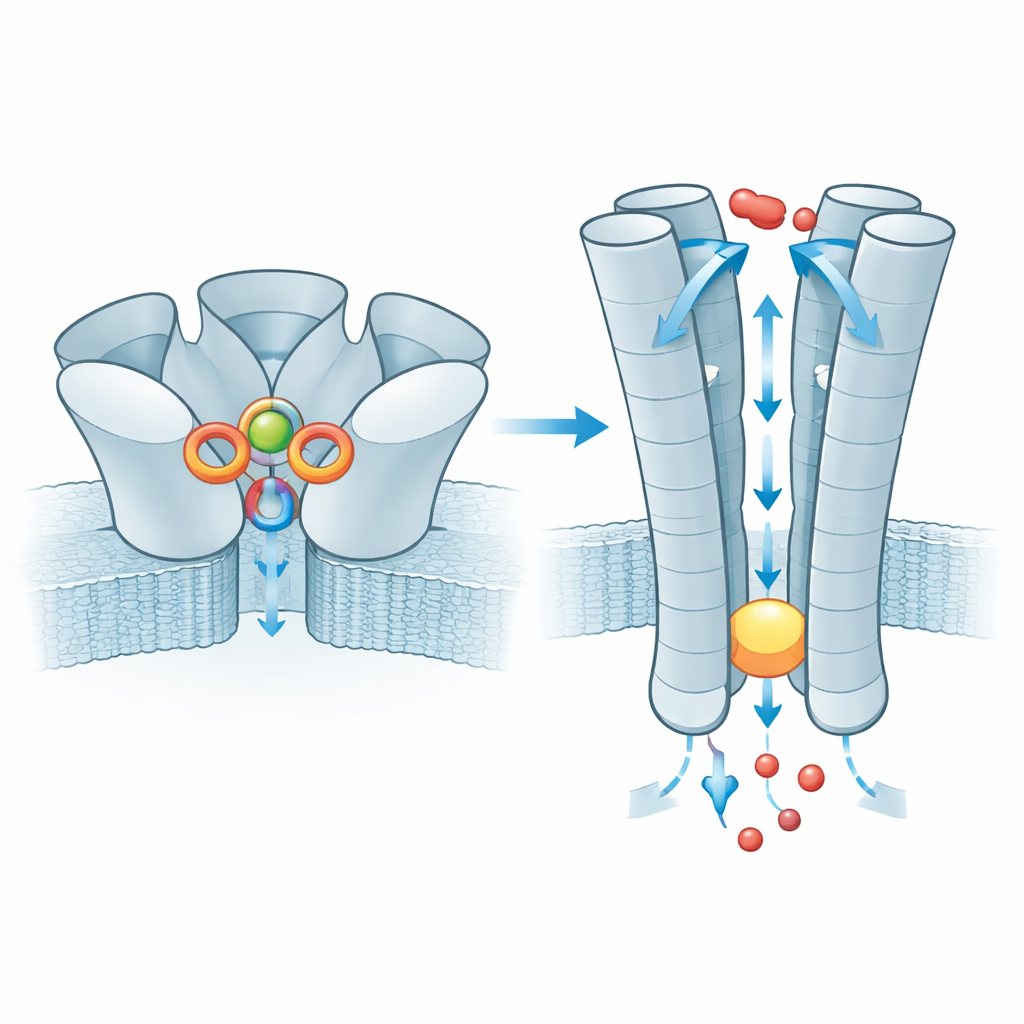
När zink bundit vidareförmedlas effekten ned till den membran‑genomgående delen av ZAC, där fem inre helixar bildar poren. I vilotillståndet smalnar detta rör av vid en ring av leucinresiduer och bildar en hydrofob plugg som blockerar jonflödet. Med zink bundet vidgas pluggen precis så mycket att små positiva joner, som natrium och kalium, kan glida igenom, medan porens laddade inneryta hjälper till att selektera dessa joner. Teamet undersökte också en mycket vanlig mänsklig variant av ZAC där en enda aminosyra (treonin) ersatts av alanin i en kort sträng ovanför pluggen. Denna lilla förändring försvagar ett interaktionsnätverk mellan intilliggande subenheter som normalt hjälper till att vidarebefordra zinkbindningen till grinden, och elektriska mätningar visar att kanaler byggda av denna variant leder mycket mindre ström. Varianten fungerar därför som en mindre effektiv signalomvandlare, även om dess påverkan på mänsklig fysiologi fortfarande är okänd.
Hur två läkemedel tystar kanalen
Förutom zink utforskar studien också hur två antagonister, TTFB och d‑tubokurarin (d‑TC), stänger av ZAC. TTFB är en specialdesignad liten molekyl som visar sig lägga sig djupt i membrandomänen, mellan två av de porbildande helixarna strax ovanför grinden. Där interagerar den med en tajt hydrofob ficka och närliggande polära rester och fungerar i praktiken som ett stöd som hindrar helixarna från att röra sig in i ett fullständigt öppet ledande tillstånd. d‑TC, ett äldre läkemedel som tidigare användes som muskelavslappnande medel, verkar mer brett. En d‑TC‑molekyl binder i samma yttre ficka som normalt rymmer zink, efterliknande zinkets positiva laddning men hindrande äkta zink från att binda korrekt. En andra d‑TC‑molekyl sitter i själva porens ingång och täpper fysiskt till tunneln. Tillsammans fångar dessa bindningar ZAC i en desensitiserad, icke‑ledande konformation medan proteinets form förblir relativt öppen.
Vad fynden betyder för zink och hälsa
Detta strukturella arbete visar i klar molekylär detalj att ZAC är en verklig zinksensor, som använder en ovanlig aromatisk vagga för att upptäcka metallen på samma typ av plats där andra familjemedlemmar binder neurotransmittorer. Det identifierar också specifika interaktionsnätverk som justerar hur lätt kanalen öppnas och stängs, och kartlägger två distinkta läkemedelsbindningsställen som antingen kan kilas fast grinden eller täppa igen poren. För icke‑specialister är huvudbudskapet att zink inte bara är ett statiskt näringsämne utan en aktiv signal, och att ZAC är en av dess dedikerade mottagare. När forskare söker efter ZAC:s roller i människokroppen och i neurologiska störningar kopplade till zinkobalans, ger dessa atomnivå‑ritningar en vägkarta för att designa mer precisa molekyler för att modulera denna kanal och potentiellt korrigera störd zinksignalering.
Citering: Zhou, Z., Long, Y., Chao, Y. et al. Structural basis of human zinc-activated channel (ZAC) signaling and modulation. Cell Discov 12, 23 (2026). https://doi.org/10.1038/s41421-026-00878-5
Nyckelord: zinksignalering, ligandstyrda jonkanaler, neurovetenskap, kryo‑EM‑struktur, kanalmodulation