Clear Sky Science · sv
ASCT2-palmitoylering reglerad av JNK1–ZDHHC14-axeln orkestrerar glutaminmetabolism och NSCLC-progress
Matning av lungcancerelden
Många snabbväxande lungtumörer är beroende av glutamin, en vanlig aminosyra som fungerar både som viktig bränslekälla och byggsten. I denna studie avslöjas hur tumörceller fintunear en större glutamingräns på sin yta och hur störning av detta kontrollsystem kan bromsa tumörtillväxt. Att förstå denna dolda bränsleventil förklarar varför vissa tumörer är svåra att svälta ut och pekar på nya läkemedelskombinationer som kan skära av deras energiförsörjning mer effektivt.
En cellulär grind för glutamin
Glutamin tar sig in i celler huvudsakligen via en transportörsprotein kallat ASCT2, som sitter i cellmembranet och för glutamin in. Icke-småcellig lungcancer (NSCLC), den vanligaste formen av lungcancer, är ofta starkt beroende av glutamin för snabb delning och överlevnad. Höga nivåer av ASCT2 i tumörer kopplas till aggressiv sjukdom och sämre patientutfall. Samtidigt syntetiseras, modifieras och bryts ASCT2 hela tiden ner, vilket väcker frågan: vad avgör hur mycket av denna grindvakt som finns kvar på cellytan vid varje given tidpunkt?
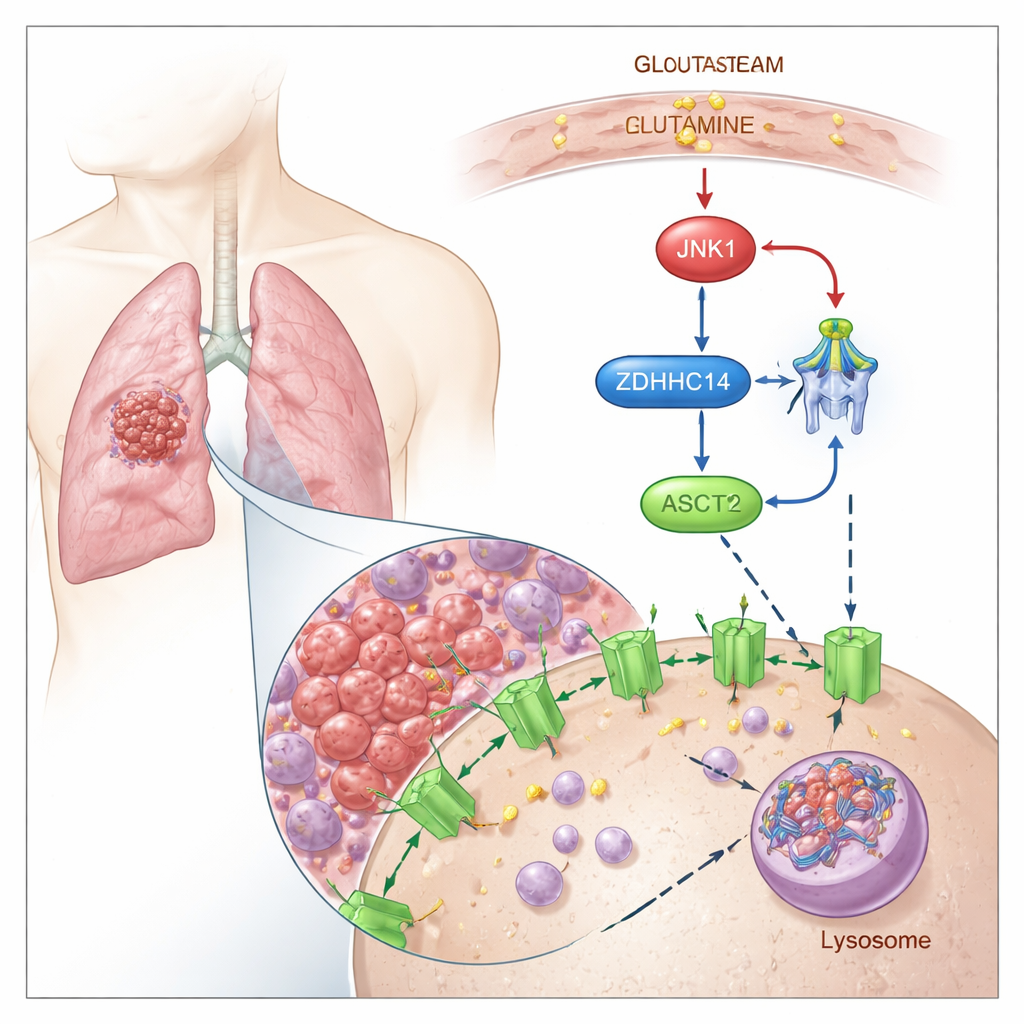
Markerar ASCT2 för nedbrytning
Forskarna visar att ASCT2 styrs av en kemisk ”märkning” kallad palmitoylering, där en fettsyra fästs vid specifika cysteinrester i proteinet. De finner att ett enzym kallat ZDHHC14 lägger till denna lipidmärkning vid två bevarade platser på ASCT2 (Cys39 och Cys48). När ASCT2 blivit märkt omdirigeras det från cellytan till cellens återvinningscentraler, lysosomerna, där det bryts ner. Att blockera palmitoylering förhindrar att ASCT2 märks och degraderas, vilket leder till högre ASCT2-proteinnivåer och ökat glutaminupptag utan att ändra den underliggande genaktiviteten.
Ett motverkande enzym som skyddar grinden
Motsatsen till ZDHHC14 är ett annat enzym, ABHD17B, som tar bort fettmärket från ASCT2. När ABHD17B är aktiv blir ASCT2 mindre palmitoylerat, mer stabilt och mer benäget att återföras till cellytan istället för att skickas till lysosomen. Detta fram-och-tillbaka av märkning fungerar som en finjusterad ratt för glutaminflödet: ZDHHC14 skjuter ASCT2 mot nedbrytning, medan ABHD17B räddar det och upprätthåller glutamintransport. I lungceller skiftar en förskjutning mot mindre palmitoylering balansen mot ökat glutaminupptag och stödjer tumörtillväxt i odlingsskålar och hos möss.
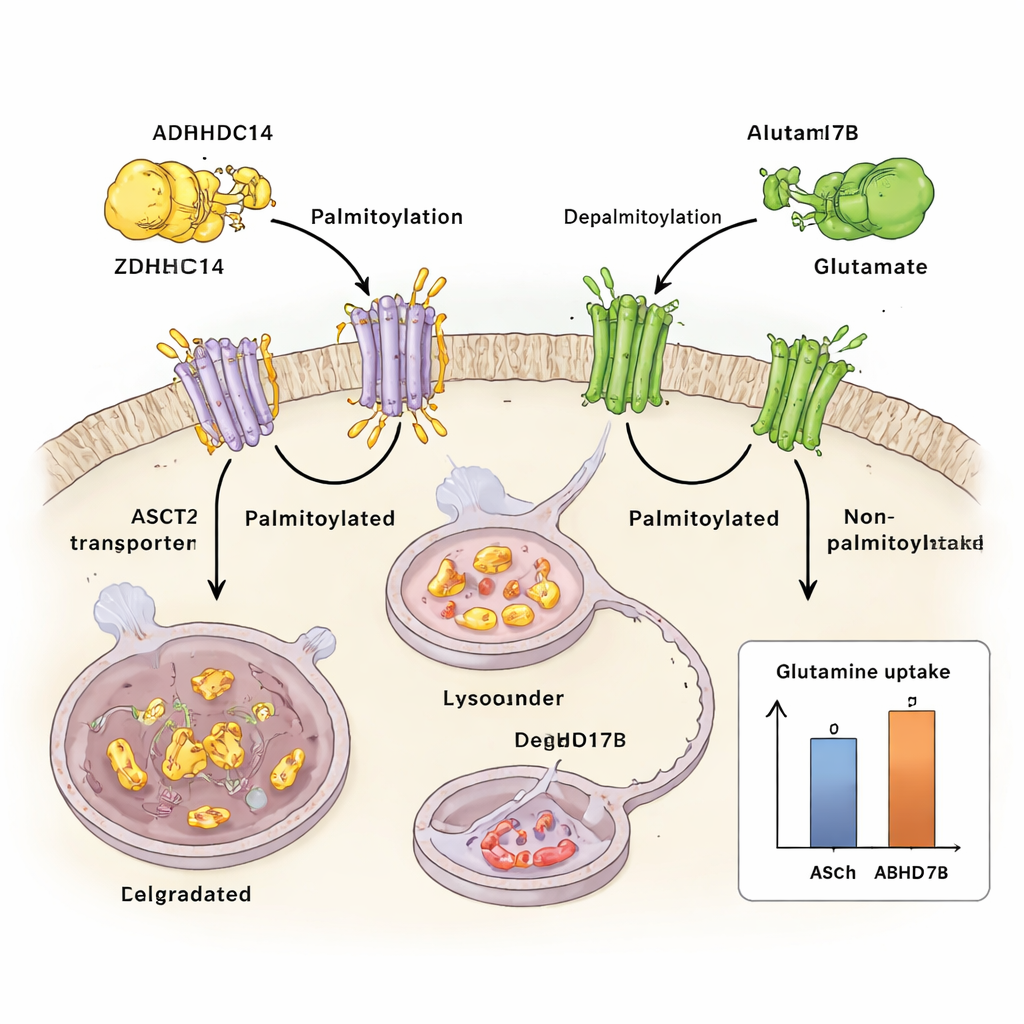
Hur näringsstress omprogrammerar systemet
Teamet undersökte sedan vad som händer när tumörceller får slut på glutamin. Vid glutaminbrist aktiveras ett stresskänsligt signalprotein kallat JNK1. JNK1 binder fysiskt till ZDHHC14 och sätter på en fosfatgrupp vid en specifik plats (Thr440), vilket markerar ZDHHC14 för lysosomal nedbrytning. När ZDHHC14-nivåerna sjunker får ASCT2 färre palmitoyleringsmärken, undviker nedbrytning och byggs upp på cellytan — precis när cellen mest behöver skaffa sig knappa glutaminresurser. Mutation av denna enda JNK1-känsliga plats stabiliserar ZDHHC14, återställer ASCT2-märkningen och minskar glutaminupptaget, vilket understryker hur tätt näringsstress är kopplat till denna kontrollloop.
Översättning av mekanism till terapi
Eftersom ASCT2 är så viktigt för tumörens metabolism undersöks läkemedel som blockerar det, såsom det experimentella ämnet V9302, som potentiella cancerbehandlingar. Denna studie visar att JNK1-signalering kan motverka ASCT2-nedbrytning och därmed skydda glutamingrinden. I cell- och musmodeller av NSCLC minskade en kombination av en JNK-hämmare och V9302 glutaminupptag, tumörcellstillväxt och tumörstorlek starkare än något av läkemedlen ensam. Patientprover och publika dataset visar dessutom att låg ZDHHC14 och hög ASCT2 är vanligt i NSCLC och kopplat till sämre överlevnad, vilket tyder på att detta molekylära mönster kan hjälpa till att identifiera patienter som sannolikt får störst nytta av att rikta in sig på denna väg.
Vad detta betyder för patienter
I vardagliga termer visar arbetet att vissa lungtumörer kontrollerar sitt favoritbränsle genom att justera en molekylär ventil på sin yta. En trio aktörer — JNK1, ZDHHC14 och ABHD17B — bestämmer om glutamingrinden ASCT2 märks för destruktion eller hålls öppen. När glutamin är knappt skiftar systemet för att bevara ASCT2 och hålla bränsleflödet igång, vilket hjälper tumörer att överleva under svåra förhållanden. Genom att gemensamt blockera ASCT2 och den JNK-väg som skyddar det kunde forskarna svälta ut cancerceller mer effektivt i laboratorie- och djurmodeller. Trots att ytterligare tester krävs erbjuder denna fosforylerings–palmitoylerings-axel en lovande ny inriktning för terapier som syftar till att kapa näringslivlinorna till glutaminhungriga lungtumörer.
Citering: Chen, X., Ke, Z., Wei, S. et al. ASCT2 palmitoylation regulated by JNK1-ZDHHC14 axis orchestrates glutamine metabolism and NSCLC progression. Cell Discov 12, 13 (2026). https://doi.org/10.1038/s41421-026-00870-z
Nyckelord: glutaminmetabolism, icke-småcellig lungcancer, ASCT2-transportör, proteinpalmitoylering, JNK-signalering