Clear Sky Science · sv
De molekylära mekanismerna och potentiella terapeutiska implikationer av samspelet mellan DNA-metylering och metabol omprogrammering vid sköldkörtelcancer
Varför denna forskning betyder mer än laboratoriet
Sköldkörtelcancer är en av de snabbast ökande cancerformerna globalt. Även om många fall är behandlingsbara, slutar de mest aggressiva varianterna ofta att svara på radioaktivt jod, en grundpelare i behandlingen, vilket lämnar patienterna med få bra alternativ. Denna översiktsartikel förklarar hur två osynliga krafter i cellerna — kemiska markeringar på DNA och förändringar i hur tumörceller använder bränsle — samarbetar för att driva sköldkörtelcancer och behandlingsresistens. Att förstå detta dolda partnerskap kan öppna dörren för mer precisa och hållbara behandlingar.
Hur cancerceller skriver om sin instruktionsbok
Varje cell bär samma DNA, men kemiska markörer kallade metylgrupper kan slå på eller av gener utan att ändra den genetiska koden. Vid sköldkörtelcancer är denna DNA‑"markup" kraftigt förvriden. Stora partier av genomet förlorar metylmärken, vilket kan destabilisera kromosomer, medan viktiga tillväxthämmare och gener för sköldkörtelfunktion blir övermärkta och tysta. Dessa inkluderar tumörsuppressorgener och sköldkörtelspecifika gener som normalt hjälper celler att ta upp jod. Resultatet är en instruktionsbok där många säkerhetskapitel är överstrukna, vilket gynnar okontrollerad tillväxt och förlust av normal sköldkörtelidentitet.
Hur cancerceller kopplar om sina bränslelinjer
Samtidigt bygger sköldkörteltumörceller om hur de skaffar och använder energi. Istället för att främst förbränna bränsle effektivt i mitokondrierna lutar de tungt mot snabb men ineffektiv nedbrytning av socker, vilket genererar sura restprodukter som hjälper dem att undkomma immunsystemet. De ökar också produktionen och nedbrytningen av fetter, och omdirigerar aminosyror såsom serin och glutamin för att stödja snabb delning. Dessa skiften är inte slumpmässiga: de styrs av cancertillväxtsignaler och skapar ett flexibelt metabolt nätverk som låter tumörceller överleva låg syretillgång, motstå läkemedel och växa på nya platser.
Tvåvägstrafik mellan DNAs markeringar och cellmetabolism
En central poäng i artikeln är att DNA‑märkning och bränsleanvändning inte är separata berättelser — de bildar en självförstärkande loop. Å ena sidan producerar tumörcellernas förändrade metabolism specifika småmolekyler som fungerar som brytare för de enzymer som sätter eller tar bort metylmärken på DNA. När nivåerna av dessa molekyler ändras kan de skjuta genomet mot mer eller mindre metylering på känsliga platser. Å andra sidan kan DNA‑metylering direkt tysta eller öka gener som kontrollerar sockeranvändning, fettmetabolism och aminosyratransport. Med tiden låser denna tvåvägstrafik in ett cancer‑vänligt tillstånd där onormala DNA‑markeringar och förvrängd metabolism ständigt stärker varandra.
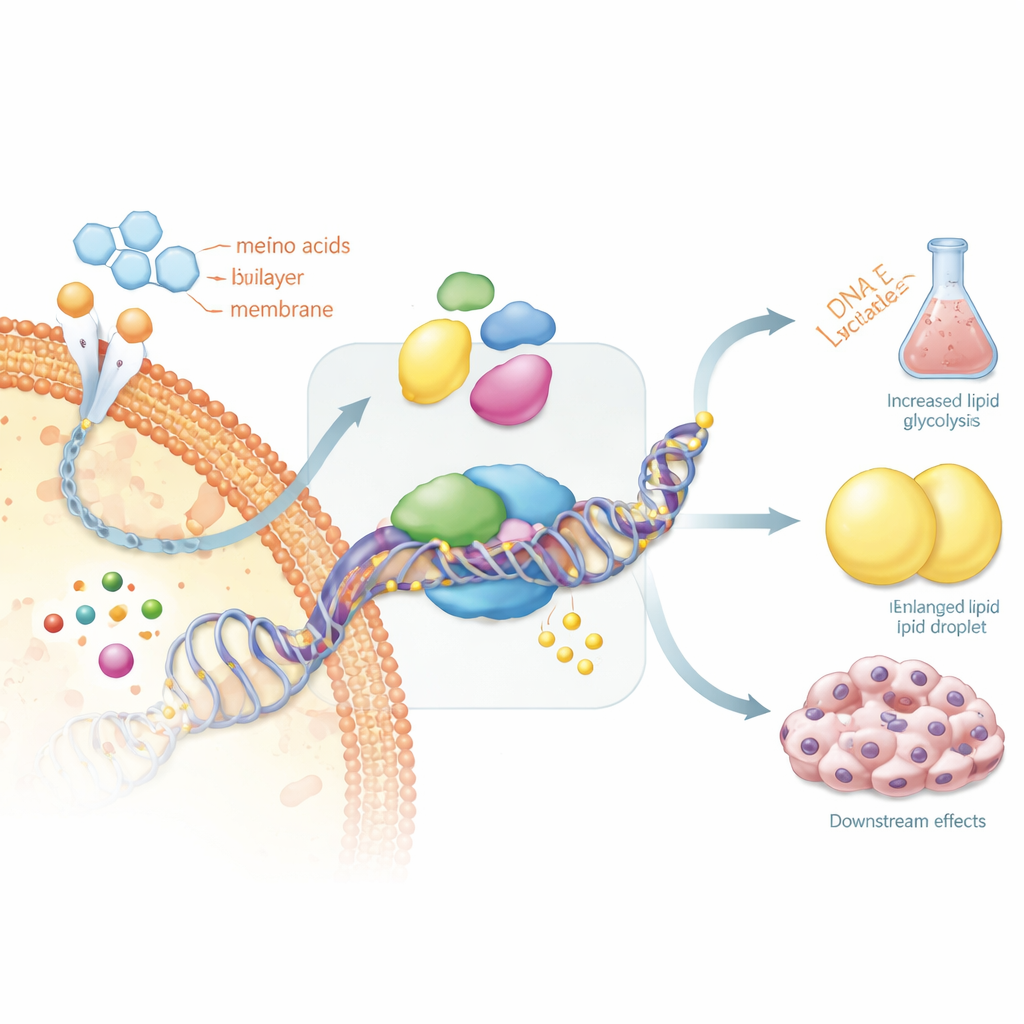
Varför vissa sköldkörtelcancer slutar ta upp jod
Denne återkopplingsslinga har mycket praktiska konsekvenser för patienter. Radioaktiv jodterapi fungerar bara om tumörcellerna behåller den molekylära maskineri som behövs för att föra in jod. Översikten framhåller att nyckelgener för sköldkörtelfunktionen, inklusive receptor för sköldkörtelstimulerande hormon och natrium–jod‑transportören, ofta stängs av genom tung metylering av deras kontrollregioner. När detta sker "glömmer" cancercellerna att de är sköldkörtelceller och absorberar inte längre jod, vilket gör standardbehandlingen verkningslös. Författarna föreslår att en noggrant kontrollerad återställning av dessa DNA‑märken, eller blockering av de metabola vägar som upprätthåller dem, skulle kunna återväcka jodupptaget och återställa känsligheten för behandlingen.
Nya behandlingsidéer baserade på en integrerad bild
Att se sköldkörtelcancer som en sjukdom i en "DNA‑metylering–metabolism‑axel" leder till nya terapeutiska strategier. Istället för att förlita sig på enstaka läkemedel argumenterar författarna för kombinationsmetoder som angriper flera delar av loopen samtidigt — epigenetiska läkemedel som lossar skadliga DNA‑märken, metabola läkemedel som skär av viktiga bränslevägar, och signalblockerande läkemedel som dämpar huvuddrivande cancermekanismer. Att lägga till moderna immunterapier och avancerade läkemedelsleveranssystem, som intelligenta nanopartiklar, kan ytterligare förskjuta balansen genom att omforma tumörens immummiljö samtidigt som biverkningar begränsas. Tidiga laboratorie‑ och kliniska data tyder på att sådana koordinerade angrepp kan bromsa sjukdomen, återställa radiojodupptag hos vissa patienter och fördröja resistens.
Vad detta betyder för framtida vård
För en lekmannaläsare är slutsatsen att aggressiva sköldkörtelcancer kanske inte botas med en enda mirakelkur, utan genom att förstå och störa den destruktiva cykeln mellan DNA‑markeringar och cellmetabolism. Genom att kartlägga denna axel i detalj och följa förändringarna i blod‑ och tumörprover kan läkare en dag matcha patienter med skräddarsydda kombinationer av epigenetiska, metabola, riktade och immunterapier. Om detta lyckas kan denna integrerade strategi förvandla dagens mest svårbehandlade sköldkörtelcancer till tillstånd som återigen är behandlingsbara — och eventuellt förhindra att de blir så aggressiva från början.
Citering: Zhang, T., Han, H., Zhang, Y. et al. The molecular mechanisms and potential therapeutic implications of the crosstalk between DNA methylation and metabolic reprogramming in thyroid cancer. Cell Death Discov. 12, 110 (2026). https://doi.org/10.1038/s41420-026-02981-8
Nyckelord: sköldkörtelcancer, DNA-metylering, cancermetabolism, radiojodresistens, riktad terapi