Clear Sky Science · sv
AdipoR1–AMPK-axeln undertrycker bröstcancer över molekylära subtyper via multimodala celldödsvägar, inklusive ferroptos och apoptos
Varför fettceller spelar roll för bröstcancer
De flesta av oss tänker på kroppsfett som ett passivt energilager, men fettceller är aktiva fabriker som släpper ut hormoner och signalmolekyler i blodomloppet. Denna studie undersöker hur en av dessa fettsignaler, som verkar via en molekyl kallad AdipoR1 på bröstcancerceller, kan bromsa tumörtillväxt. Arbetet är viktigt eftersom det föreslår ett nytt sätt att behandla många former av bröstcancer genom att utnyttja kommunikationen mellan fettvävnad och tumörer, vilket potentiellt kan förstärka effekten av befintliga läkemedel.
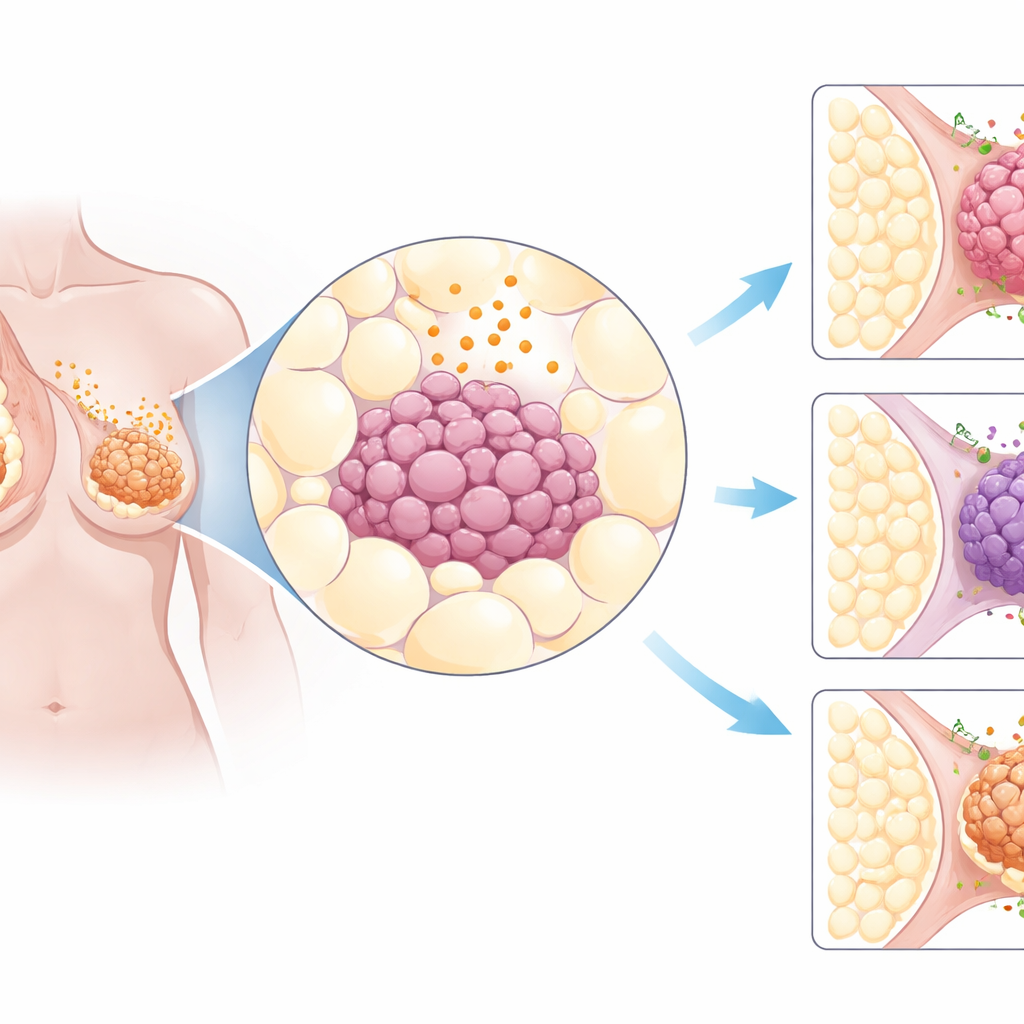
Undersökt över många cancerformer
Forskarna började med att granska stora offentliga cancer databaser som innehåller genetisk information från tusentals patienttumörer. De koncentrerade sig på ett trettiotal gener som är involverade i signaler från fettvävnad och de cellstrukturer som tar emot dessa signaler. När de jämförde tumörer från 31 olika organ med frisk vävnad framträdde ett mönster: bröstcancer uppvisade särskilt kraftiga förändringar i dessa fettrelaterade signaler. Särskilt stod receptorn AdipoR1 ofta på högre än normala nivåer i brösttumörer, oavsett om de var hormonstyrda, HER2-positiva eller den mer aggressiva trippelnegativa typen. Vävnadsprover från mer än 600 bröstcancerfall bekräftade att AdipoR1-proteinet var allmänt närvarande i tumörcellerna.
Test av ett fettsignal-läkemedel på cancerceller
För att se vad AdipoR1 faktiskt gör inne i tumörer använde teamet bröstcancercellinjer odlade i labbet, som representerar flera vanliga subtyper. De behandlade dessa celler med AdipoRon, en liten molekyl som aktiverar AdipoR1. AdipoRon aktiverade snabbt en känd energikänslig växel i celler kallad AMPK, vilket visar att signalen tog sig igenom. När dosen AdipoRon ökade delade cancercellerna sig långsammare, rörde sig mindre i sår-återbildningsförsök och många genomgick programmerad självdestruktion. När forskarna medvetet minskade AdipoR1-nivåerna i cellerna förlorade AdipoRon mycket av sin effekt, medan ökad uttryck av AdipoR1 gjorde läkemedlet mer verksamt, vilket knöt effekten direkt till denna receptor.
Flera sätt att driva cancerceller mot död
Genom att analysera genaktivitet efter behandling fann forskarna att AdipoRon slog på stressreaktioner inne i bröstcancercellerna. Det aktiverade gener kopplade till klassisk programmerad celldöd såväl som de som är involverade i en nyare identifierad form av järnavhängig celldestruktion kallad ferroptos. Nyckelmarkörer för denna process ökade både på RNA- och proteinnivå, särskilt i hormonkänsliga bröstcancerceller, och kemiska mätningar av skadade celllipider stödde denna slutsats. Samtidigt minskade AdipoRon nivåerna av proteiner som normalt hjälper cancerceller att överleva, inklusive DNA-reparationshjälpare (BRCA1 och BRCA2), östrogenreceptorn som driver tillväxt i många tumörer, och TROP2, ett ytprotein kopplat till aggressivt beteende.
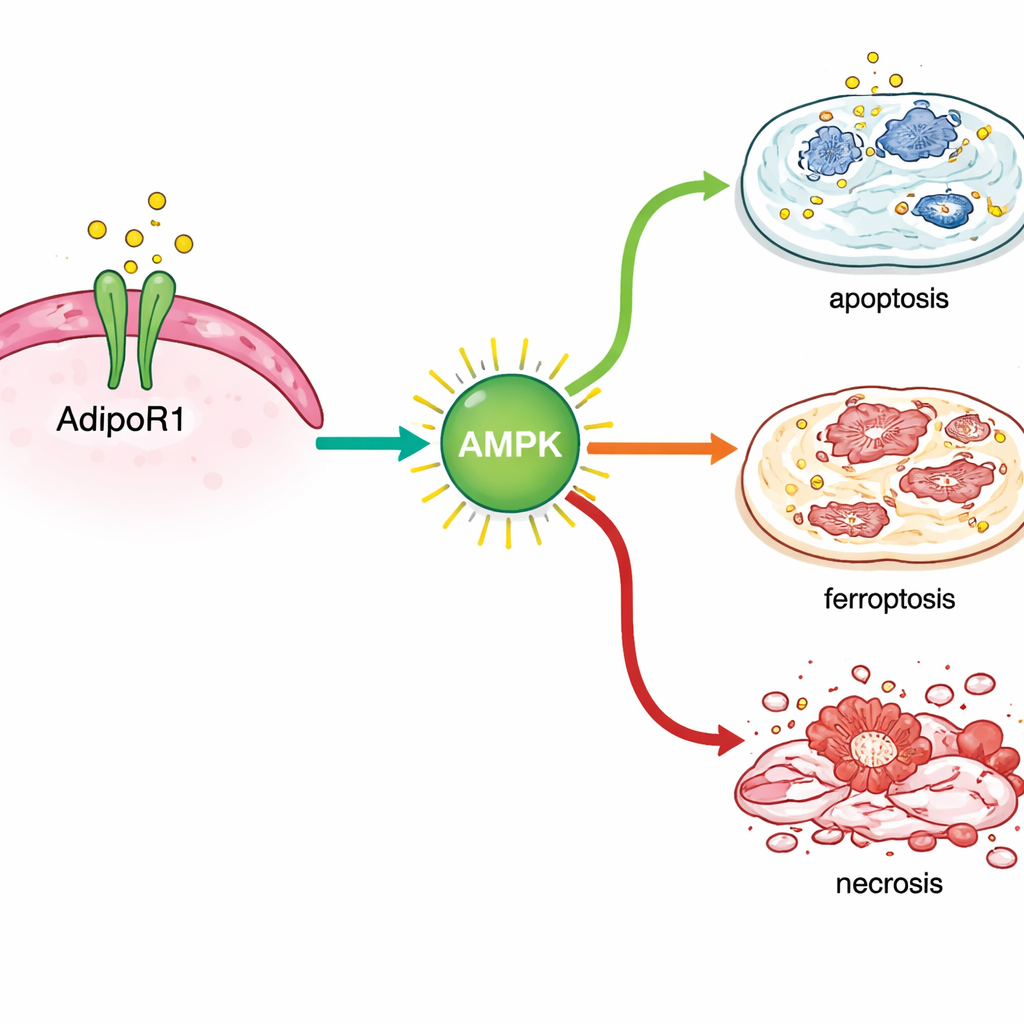
Samverkan med nuvarande behandlingar snarare än konkurrens
Teamet frågade sedan om aktivering av AdipoR1 kunde komplettera standardläkemedel. I hormonkänsliga bröstcancerceller gav AdipoRon i kombination med tamoxifen en större tillväxtdämpning än något av läkemedlen ensamt. I trippelnegativa cellinjer förstärkte AdipoRon effekterna av vanliga cellgifter såsom paklitaxel och doksorubicin. I försök på möss med hormonkänsliga brösttumörer gav forskarna AdipoRon i dricksvattnet. Tumörer hos behandlade djur växte långsammare och innehöll större nekrotiska (döda) områden vid mikroskopisk undersökning. Viktigt är att mössen inte uppvisade tydliga biverkningar i beteende, vikt eller leverhälsa under behandlingsperioden.
Vad detta kan betyda för patienter
Sammantaget tyder fynden på att aktivering av AdipoR1 i bröstcancerceller engagerar flera överlappande vägar till celldöd samtidigt som viktiga överlevnadssystem försvagas, och att denna strategi fungerar över olika genetiska former av sjukdomen. Snarare än att ersätta befintliga terapier skulle AdipoR1-riktade läkemedel som AdipoRon kunna fungera som tillägg som gör tumörer mer sårbara för hormonbehandling, cytostatika eller framtida målriktade medel. Innan denna strategi kan nå kliniken behöver forskare utveckla mer potenta och selektiva AdipoR1-aktivatorer, klargöra vilka patienters tumörer som uttrycker receptorn starkast och noggrant utvärdera säkerheten. Ändå pekar detta arbete på en intressant idé: signaler från vår egen fettvävnad skulle kunna omdirigeras för att hjälpa till att bekämpa bröstcancer istället för att mata den.
Citering: Sato, S., Yamanaka, T., Komori, Y. et al. AdipoR1–AMPK axis suppresses breast cancer across molecular subtypes via multimodal cell death pathways, including ferroptosis and apoptosis. Cell Death Dis 17, 384 (2026). https://doi.org/10.1038/s41419-026-08583-7
Nyckelord: bröstcancer, adipokiner, AdipoR1, celldödsvägar, cancermetabolism